Clear Sky Science · sv
RASSF1C–HIF-1α-axeln styr makrofagers lipidmetabolism för att främja bukspottkörtelcancer
Varför denna cancerberättelse är viktig
Bukspottkörtelcancer är en av de dödligaste cancersjukdomarna, delvis eftersom tumören ligger djupt i kroppen och ofta upptäcks sent. Men dess aggressivitet handlar inte bara om tumörcellerna själva. Denna studie visar hur syrebrist inne i bukspottkörteltumörer omprogrammerar både cancerceller och närliggande immunceller på ett sätt som främjar tumörtillväxt och spridning. Genom att avslöja denna händelsekedja pekar forskarna ut nya angreppspunkter för att bekämpa sjukdomen genom att rikta in sig både på tumörens metabolism och immunsystemet.
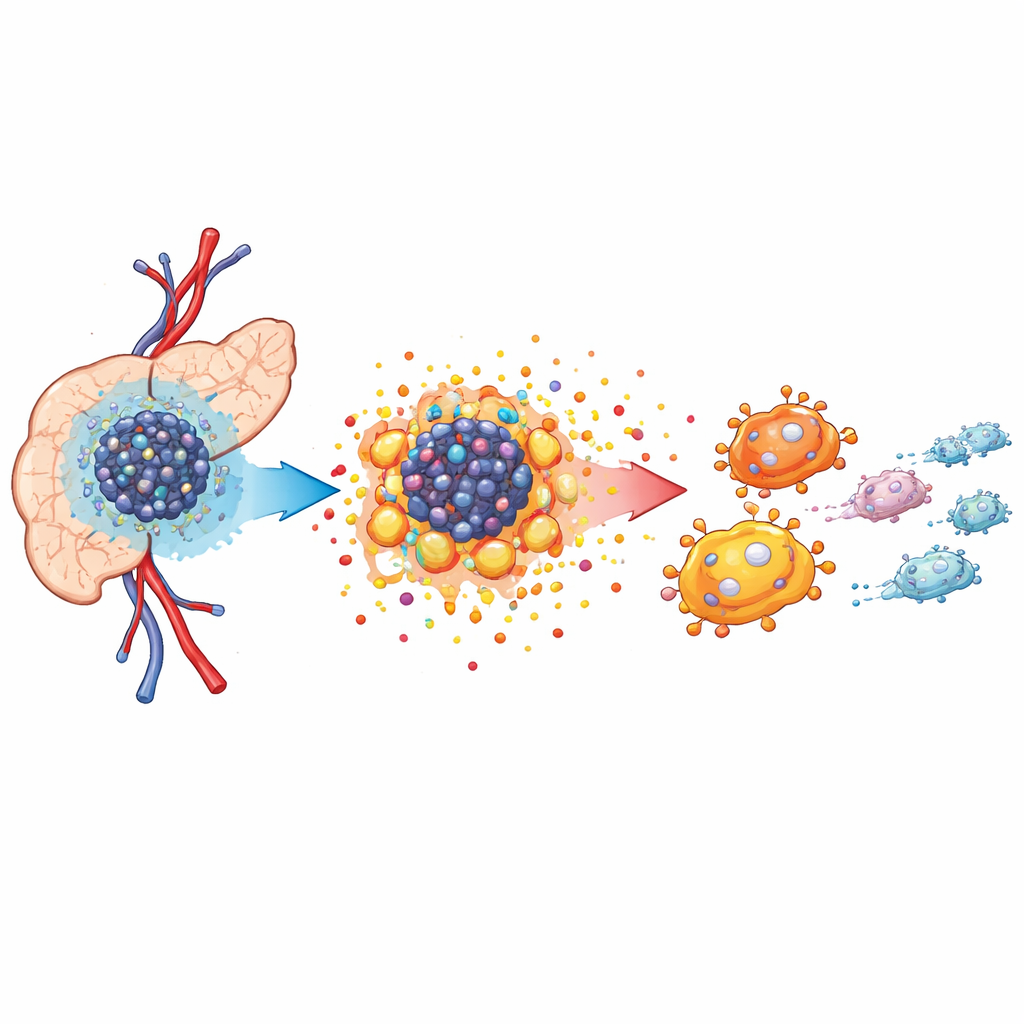
Lågt syre och en hungrig tumörnärmiljö
Bukspottkörteltumörer växer i en trång, fientlig miljö som kallas tumörmikromiljön. Blodtillförseln är dålig, så syrehalten sjunker, vilket tvingar cancerceller att ändra hur de skaffar energi. Med hjälp av enkelcells-RNA-sekvensering och rumslig kartläggning i musmodeller visade författarna att tumörvävnaden är fylld av cancerceller, cancerassocierade fibroblaster och specialiserade immunceller kallade tumörassocierade makrofager. Dessa makrofager klustrar nära cancerceller och antar ofta en roll som stödjer tillväxt snarare än att bekämpa tumören. Analysen visade att cancerceller är starkt beroende av omställd metabolism för att driva snabb tillväxt, vilket lägger grunden för en vidare omgestaltning av vävnadsmiljön.
Att driva cancer med socker och syra
När syre är knapphändigt förlitar sig cancerceller på en process som liknar snabb, ineffektiv sockerförbränning, ofta kallad Warburg-effekten. Forskarna fann att en proteinarternativ form kallad RASSF1C, tidigare kopplad till cancerbeteende, blir starkt aktiverad vid låga syrenivåer. Drivet av ett annat syreföljande protein, HIF-1α, ökar RASSF1C glykolysen, vilket leder till hög produktion av laktat och en surare omgivning. I cell- och djurförsök minskade nedreglering av RASSF1C syrabildningen och saktade ner tumörtillväxten, medan överuttryck gav motsatt effekt. Viktigt är att hämning av laktatbildning med ett läkemedel dämpade den tillväxtfördel som RASSF1C gav, vilket visar att denna metaboliska omställning inte bara är en bieffekt — den driver aktivt sjukdomens progression.
Hur tumörens biprodukter omprogrammerar immunceller
Det laktat som tumörceller släpper ut förändrar mer än bara lokal kemi; det fungerar som en signal. När forskarna exponerade makrofager för konditionerad vätska från laktatrika bukspottkörtelcancerceller skiftade makrofagerna mot ett M2-liknande, tumörstödjande tillstånd. De producerade fler antiinflammatoriska faktorer och färre molekyler kopplade till attacker och rensning av cancerceller. I möss innehöll tumörer med höga RASSF1C-nivåer fler av dessa protumörska makrofager, en effekt som kunde dämpas genom att blockera laktatproduktionen. Ytterligare tester visade att laktat också omprogrammerade hur makrofager hanterar fetter och kolesterol, vilket ökade lipiduppbyggnad på sätt som överensstämmer med en mer stödjande nisch för tumörtillväxt och spridning.
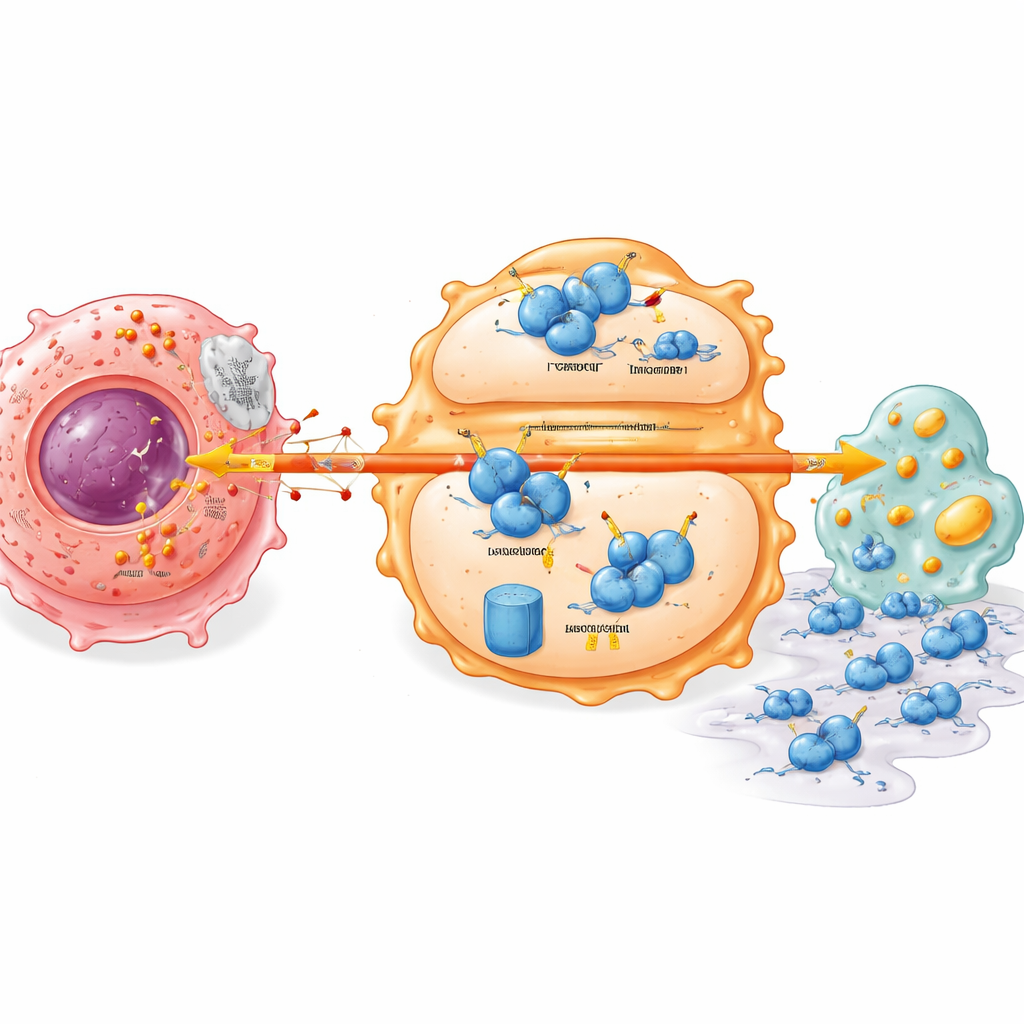
En dold stabilitetsknapp inne i immuncellerna
Vid fördjupade studier upptäckte man en molekylär omkopplare som kopplar tumörmetabolism till immuncellsbeteende. En viktig immunregulator kallad IRF7, som normalt stödjer ett mer vaksamt, anfallsredo makrofagläge och hälsosam lipidomsättning, fanns på låga nivåer i bukspottkörteltumörer. Laktat från cancerceller gjorde IRF7-proteinet i makrofager instabilt och fick det att brytas ner snabbare. Detta var beroende av ett annat protein, UFL1, som fäster en liten märkning (UFM1) som skyddar IRF7 från att bli utpekad för nedbrytning. Laktat undertryckte UFL1 i makrofager och försköt balansen mot ett märkningssystem som skickar IRF7 till cellens proteinnedbrytare. Utan stabilt IRF7 samlar makrofager på sig metabola defekter och hjälper lättare tumörceller att migrera och invadera omgivande vävnad.
Vad detta betyder för framtida behandlingar
I tumörprover från personer med bukspottkörtelcancer såg forskarna ett tydligt mönster: högre nivåer av RASSF1C och HIF-1α i tumörceller, och lägre nivåer av UFL1 och IRF7 i omkringliggande vävnad. Dessa mönster korrelerade med mer avancerad sjukdom och tecken på metastasering. Tillsammans beskriver fynden en kedja där lågt syre aktiverar RASSF1C och HIF-1α, driver överproduktion av laktat och i sin tur inaktiverar den skyddande UFL1–IRF7-bromsen inne i makrofager. För den allmänna läsaren är slutsatsen att bukspottkörtelcancer utnyttjar sina egna avfallsprodukter som vapen för att avväpna närliggande immunceller. Att bryta denna kedja — genom att begränsa laktat, blockera RASSF1C–HIF-1α-signalering eller stabilisera IRF7 — kan öppna nya vägar för behandlingar som kombinerar metabola läkemedel med immuninriktade strategier.
Citering: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Nyckelord: bukspottkörtelcancer, tumörmikromiljö, tumörmetabolism, makrofager, laktat