Clear Sky Science · nl
De RASSF1C–HIF-1α-as draait de lipidenstofwisseling van macrofagen aan om alvleesklierkanker te bevorderen
Waarom dit kankerverhaal ertoe doet
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker, deels omdat de tumor diep in het lichaam verscholen zit en vaak laat wordt ontdekt. Maar de agressiviteit is niet alleen te wijten aan de tumorcellen zelf. Deze studie toont aan hoe zuurstoftekort binnen alvleesklier tumoren zowel kankercellen als nabije immuuncellen zodanig herschakelt dat het de groei en uitzaaiing van de kanker bevordert. Door deze keten van gebeurtenissen bloot te leggen, wijzen de onderzoekers op nieuwe manieren om de ziekte aan te pakken door zowel het tumormetabolisme als het immuunsysteem te richten.
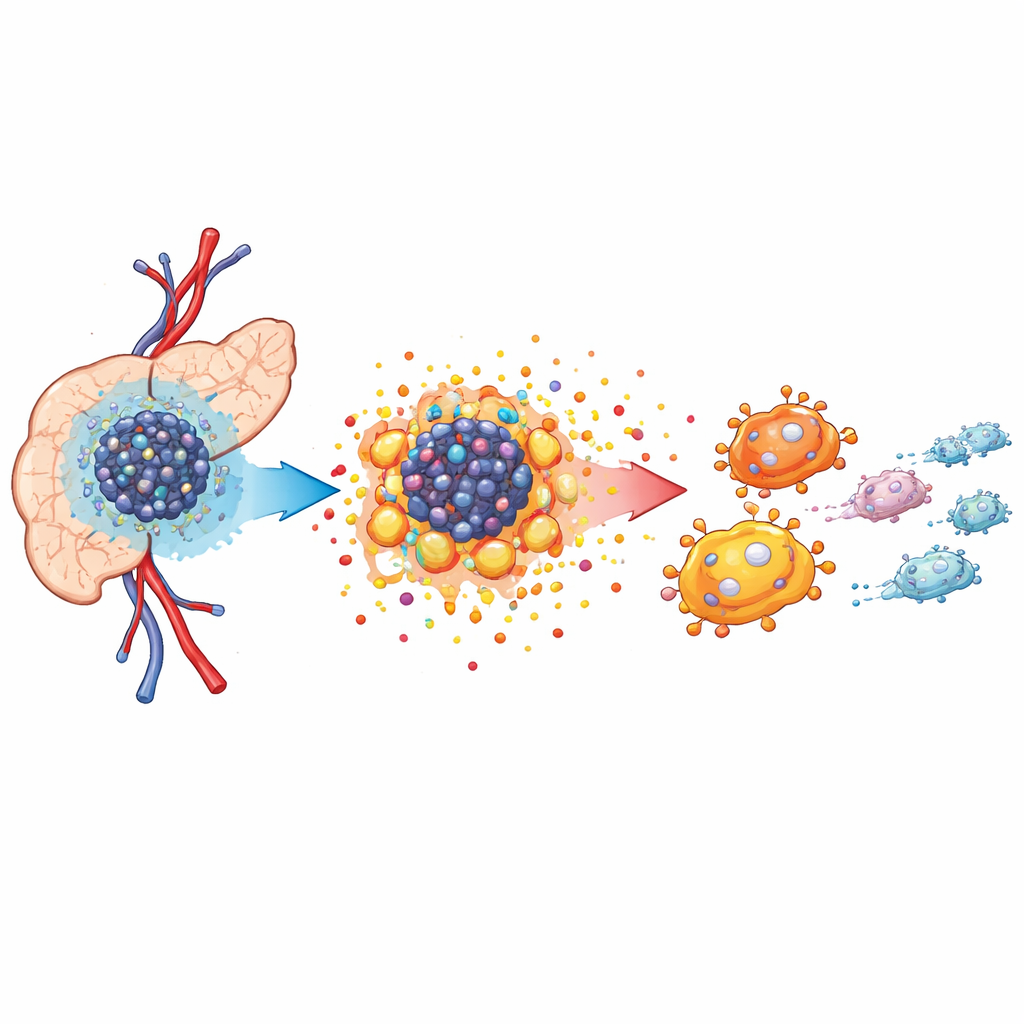
Weinig zuurstof en een hongerige tumornebuurt
Alvleeskliertumoren groeien in een drukke, vijandige omgeving die bekendstaat als het tumormicro-omgeving. De bloedvoorziening is slecht, waardoor de zuurstofniveaus dalen en kankercellen gedwongen worden hun energiehuishouding te veranderen. Met single-cell RNA-sequencing en ruimtelijke kaartvorming in muismodellen lieten de auteurs zien dat tumoren vol zitten met kankercellen, kanker-geassocieerde fibroblasten en gespecialiseerde immuuncellen die tumor-geassocieerde macrofagen worden genoemd. Deze macrofagen clusteren dicht bij kankercellen en nemen vaker een groei-ondersteunende dan een kanker-bestrijdende rol aan. De analyse toonde aan dat kankercellen sterk steunen op afwijkend metabolisme om hun snelle groei te voeden, wat de basis legt voor een bredere herschikking van het weefselmilieu.
Kanker voeden met suiker en zuur
Als zuurstof schaars is, leunen kankercellen op een proces dat lijkt op snel, inefficiënt verbranden van suiker, vaak het Warburg-effect genoemd. Het team vond dat een eiwitvariant genaamd RASSF1C, eerder gekoppeld aan kankergedrag, sterk wordt geactiveerd bij lage zuurstof. Aangestuurd door een ander zuurstof-sensor-eiwit, HIF-1α, stimuleert RASSF1C glycolyse, wat leidt tot hoge productie van lactaat en verzuring van de omgeving. In cel- en proefdierexperimenten verminderde het terugschakelen van RASSF1C de zuurproductie en vertraagde het de tumor Groei, terwijl het verhogen van RASSF1C het tegenovergestelde effect had. Belangrijk is dat het blokkeren van lactaatvorming met een middel het groeivoordeel dat RASSF1C geeft afzwakte, wat aantoont dat deze metabole verschuiving niet slechts een neveneffect is, maar actief de ziekteprogressie voedt.
Hoe tumorbijproducten immuuncellen herprogrammeren
Het door tumorcellen uitgestoten lactaat doet meer dan de lokale chemie veranderen; het fungeert ook als signaalmolecuul. Wanneer de onderzoekers macrofagen blootstelden aan geconditioneerd medium van lactaat-rijke alvleesklierkankercellen, verschoof het macrofaagprofiel richting een M2-achtig, tumor-ondersteunend stadium. Ze produceerden meer ontstekingsremmende factoren en minder moleculen die gekoppeld zijn aan de aanval en opruiming van kankercellen. In muizen bevatten tumoren met hoge RASSF1C-niveaus meer van deze pro-tumor macrofagen, een effect dat kon worden verminderd door het blokkeren van lactaatproductie. Verdere testen lieten zien dat lactaat ook de manier waarop macrofagen vetten en cholesterol verwerken herschakelde, waardoor lipide-opslag toenam op manieren die overeenkomen met een meer ondersteunende niche voor tumor Groei en uitzaaiing.
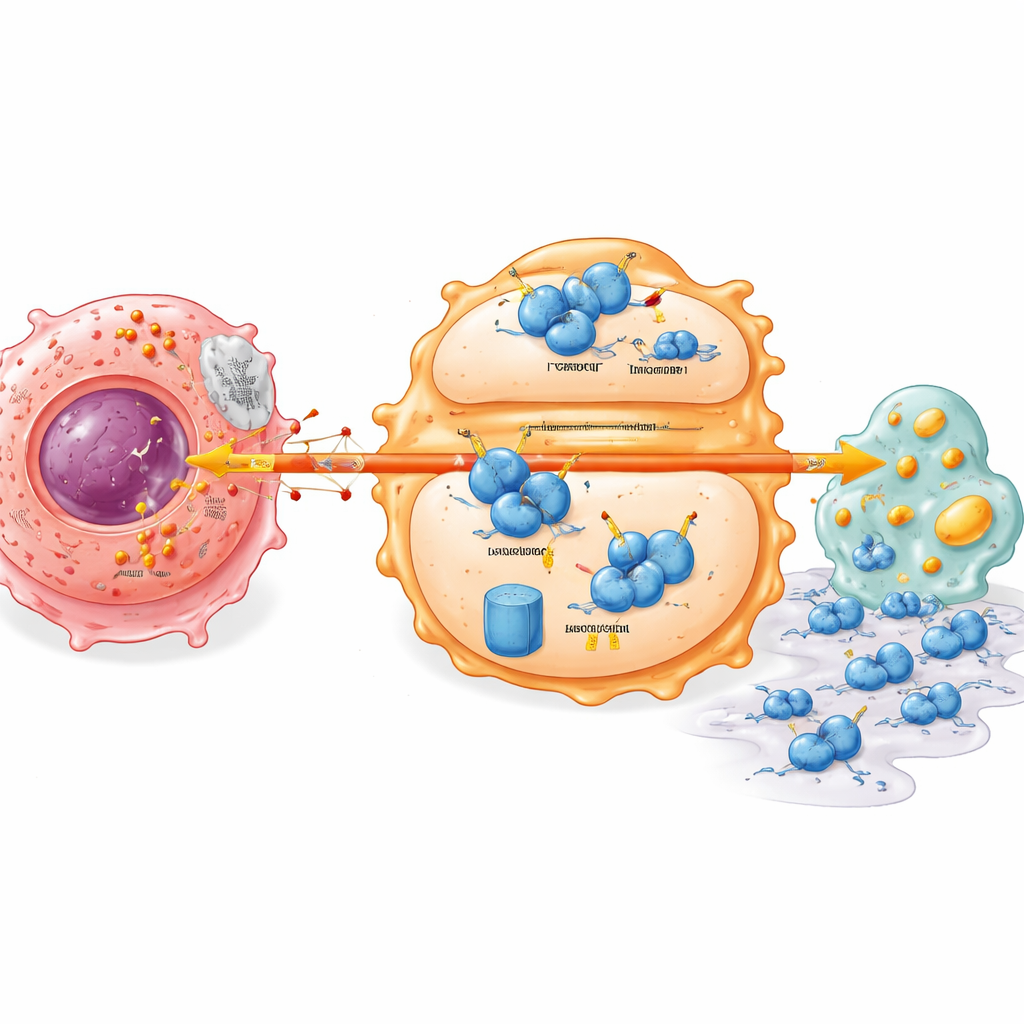
Een verborgen stabiliteitsschakelaar in immuuncellen
Dieper gravend ontdekte de studie een moleculaire schakelaar die het tumormetabolisme koppelt aan immuuncelgedrag. Een sleutelregulator in het immuunsysteem genaamd IRF7, die normaal gesproken een waakzamere, aanvalsklare macrofaagtoestand en een gezonde lipidehuishouding ondersteunt, werd in lage niveaus aangetroffen in alvleeskliertumoren. Lactaat van kankercellen zorgde ervoor dat het IRF7-eiwit in macrofagen instabiel werd en sneller afgebroken raakte. Dit hing af van een ander eiwit, UFL1, dat een klein label (UFM1) toevoegt dat IRF7 beschermt tegen markering voor afbraak. Lactaat onderdrukte UFL1 in macrofagen, waardoor de balans verschoof naar een tag-systeem dat IRF7 naar het cellulaire eiwitversnipperaar stuurde. Zonder stabiel IRF7 lopen macrofagen metabolische defecten op en helpen ze gemakkelijker tumorcellen bij migratie en invasie van omliggende weefsels.
Wat dit betekent voor toekomstige behandelingen
In tumormonsters van mensen met alvleesklierkanker zagen de onderzoekers een duidelijk patroon: hogere niveaus van RASSF1C en HIF-1α in tumorcellen, en lagere niveaus van UFL1 en IRF7 in het omringende weefsel. Deze patronen kwamen overeen met gevorderde ziekte en kenmerken van metastase. Gezamenlijk leggen de bevindingen een keten bloot waarin lage zuurstof RASSF1C en HIF-1α activeert, leidt tot overproductie van lactaat, en op zijn beurt de beschermende UFL1–IRF7-rem in macrofagen uitschakelt. Voor niet-specialisten is de conclusie dat alvleesklierkanker floreert door zijn eigen afvalproducten om te zetten in wapens die nabije immuuncellen ontwapenen. Het onderbreken van deze keten—door lactaat te beperken, RASSF1C–HIF-1α-signaalgeving te blokkeren of IRF7 te stabiliseren—kan nieuwe wegen openen voor therapieën die metabolische middelen combineren met immuun-gebaseerde benaderingen.
Bronvermelding: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Trefwoorden: alvleesklierkanker, tumormicro-omgeving, tumormetabolisme, macrofagen, lactaat