Clear Sky Science · ru
Ось RASSF1C–HIF-1α запускает липидный метаболизм макрофагов и способствует развитию рака поджелудочной железы
Почему эта история о раке важна
Рак поджелудочной железы — один из самых смертоносных видов рака отчасти потому, что он «прячется» глубоко в теле и часто обнаруживается поздно. Но его агрессивность обусловлена не только свойствами самих опухолевых клеток. В этом исследовании показано, как дефицит кислорода в опухолях поджелудочной перепрограммирует и раковые клетки, и соседние иммунные клетки таким образом, что это помогает опухоли расти и метастазировать. Выявив эту цепочку событий, авторы указывают на новые подходы к лечению, направленные одновременно на метаболизм опухоли и иммунную систему.
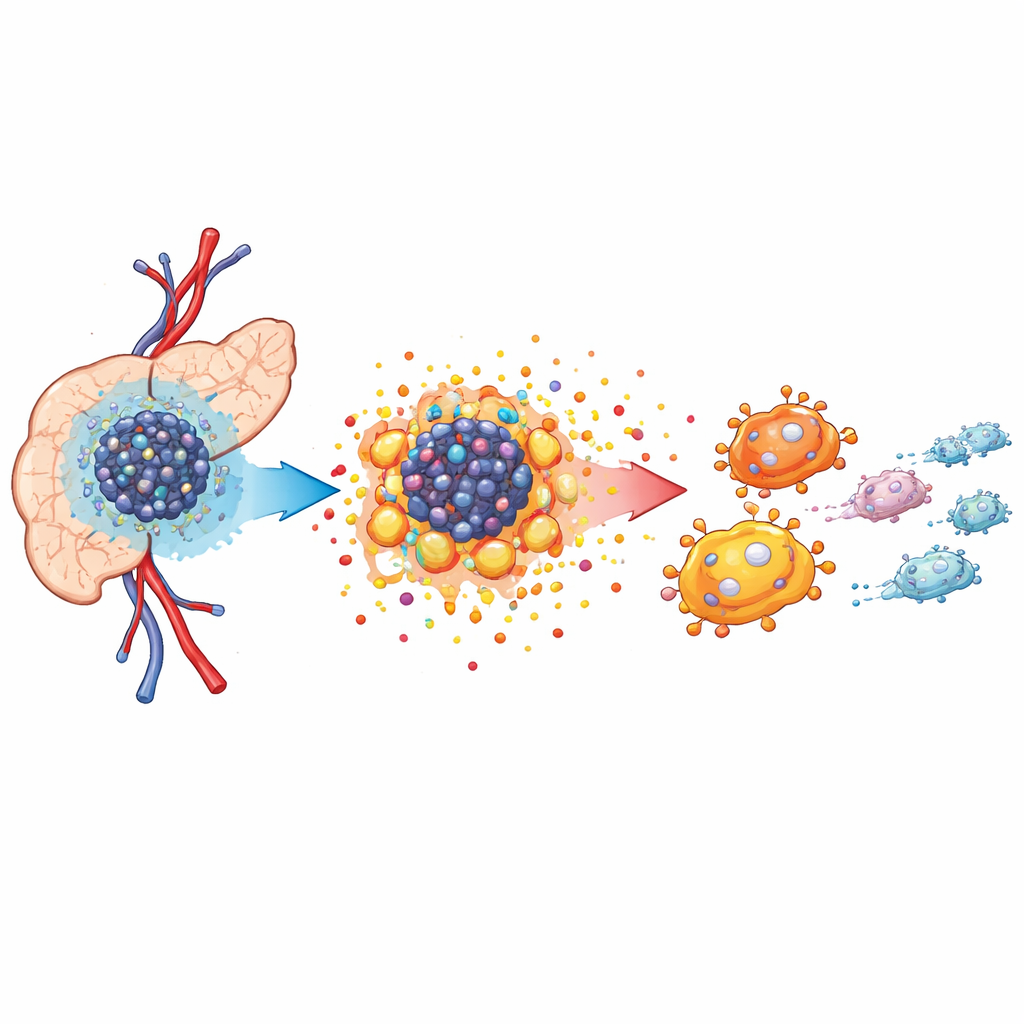
Низкий уровень кислорода и «голодный» микрорайон опухоли
Опухоли поджелудочной растут в плотном, враждебном окружении, известном как опухолевое микроокружение. Кровоснабжение там плохое, поэтому уровень кислорода падает, и опухолевые клетки вынуждены менять способы выработки энергии. С помощью секвенирования РНК по отдельным клеткам и пространственного картирования в модельных мышах авторы показали, что ткань опухоли плотно заполнена раковыми клетками, раково-ассоциированными фибробластами и специализированными иммунными клетками — опухоле-ассоциированными макрофагами. Эти макрофаги группируются рядом с раковыми клетками и склоняются к роли, поддерживающей рост опухоли, а не к её уничтожению. Анализ выявил, что раковые клетки сильно зависят от изменённого метаболизма для обеспечения быстрого роста, что создаёт предпосылки для широкого перестроения тканевого окружения.
Подпитывание рака сахаром и кислотой
При недостатке кислорода раковые клетки опираются на процесс, похожий на быструю, но неэффективную «сжигание» сахара, часто называемый эффектом Варбурга. Авторы обнаружили, что вариант белка RASSF1C, ранее связанный с поведением опухолей, сильно активируется при гипоксии. Под контролем другого кислород-чувствительного белка HIF-1α, RASSF1C усиливает гликолиз, приводя к высокой выработке лактата и закислению окружающей среды. В клеточных и животных экспериментах снижение уровня RASSF1C уменьшало образование кислоты и замедляло рост опухоли, тогда как его усиление давало обратный эффект. Важно, что блокирование образования лактата с помощью препарата ослабляло преимущество в росте, обеспечиваемое RASSF1C, что показывает: этот метаболический сдвиг — не просто побочный эффект, а активный фактор прогрессирования болезни.
Как побочные продукты опухоли перепрограммируют иммунные клетки
Лактат, выделяемый опухолевыми клетками, делает больше, чем просто меняет местную химию; он выступает как сигнальная молекула. Когда исследователи подвергали макрофаги обработанной среде от клеток панкреатической онкологии с высоким содержанием лактата, макрофаги сдвигались в сторону М2-подобного состояния, поддерживающего опухоль. Они вырабатывали больше противовоспалительных факторов и меньше молекул, связанных с атакой и уничтожением раковых клеток. У мышей опухоли с высоким уровнем RASSF1C содержали больше таких протуморных макрофагов — эффект, который можно было ослабить, блокируя образование лактата. Дальнейшие тесты показали, что лактат также перепрограммирует у макрофагов обмен жиров и холестерина, усиливая накопление липидов таким образом, что это коррелирует с более благоприятной для роста и распространения опухоли нишей.
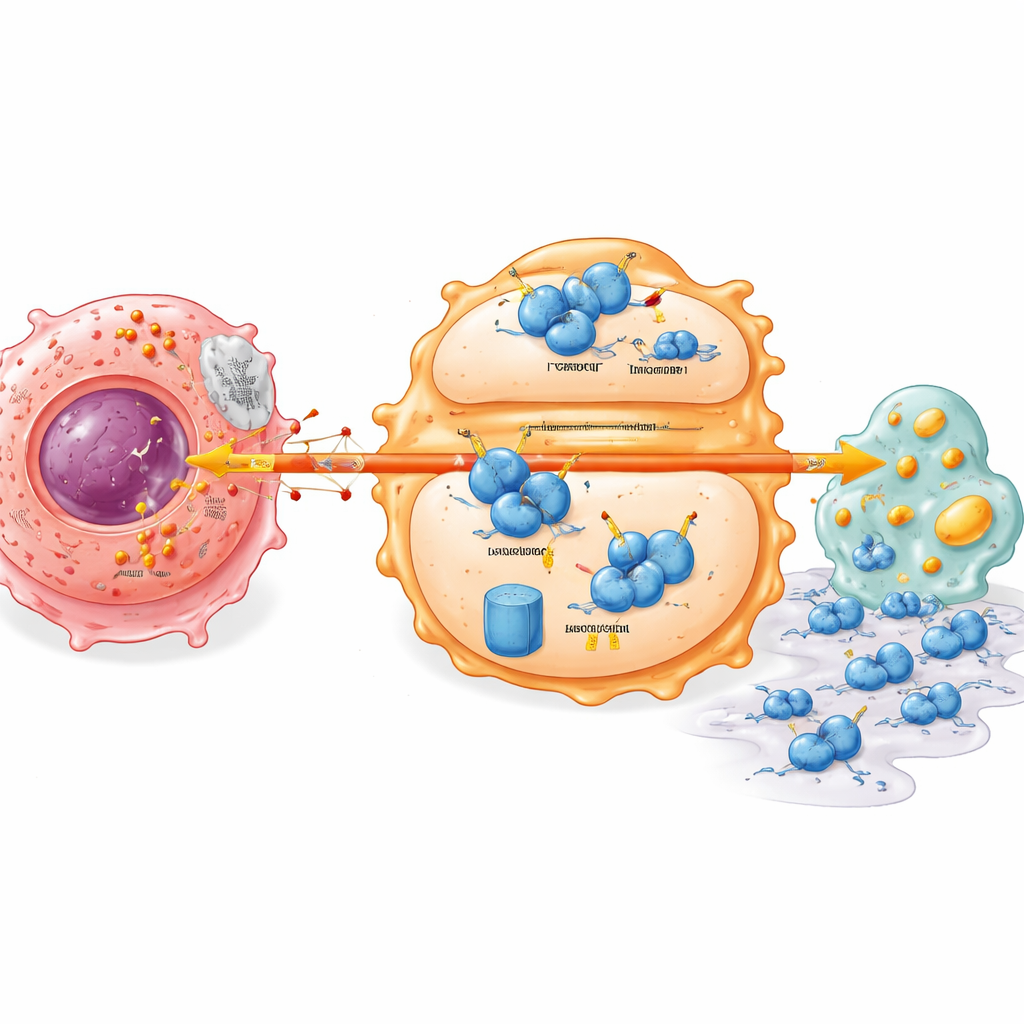
Скрытый переключатель стабильности внутри иммунных клеток
Глубже исследование выявило молекулярный переключатель, который связывает метаболизм опухоли с поведением иммунных клеток. Ключевой иммунный регулятор IRF7, который обычно поддерживает более бдительное, «атакующее» состояние макрофага и здоровое обращение с липидами, обнаруживался в низком количестве в опухолях поджелудочной. Лактат от раковых клеток вызывал нестабильность белка IRF7 в макрофагах и ускорял его распад. Это зависело от другого белка, UFL1, который присоединяет небольшой тег (UFM1), защищающий IRF7 от маркировки на разрушение. Лактат подавлял UFL1 в макрофагах, смещая баланс в сторону системы маркировки, направляющей IRF7 в протеазомный разрушитель клетки. Без стабильного IRF7 макрофаги накапливают метаболические дефекты и легче помогают раковым клеткам мигрировать и инвазировать окружающие ткани.
Что это значит для будущих методов лечения
В образцах опухолей от пациентов с раком поджелудочной исследователи обнаружили четкую закономерность: более высокие уровни RASSF1C и HIF-1α в раковых клетках и более низкие уровни UFL1 и IRF7 в окружающих тканях. Эти профили соответствовали более продвинутой стадии заболевания и признакам метастазирования. В совокупности результаты описывают цепочку, в которой гипоксия активирует RASSF1C и HIF-1α, приводит к перепроизводству лактата и, в свою очередь, дезактивирует защитный тормоз UFL1–IRF7 в макрофагах. Для непрофессионального читателя вывод таков: рак поджелудочной использует собственные «отходы» как оружие, чтобы обезвредить соседние иммунные клетки. Прерывание этой цепочки — уменьшение лактата, блокирование сигнальной оси RASSF1C–HIF-1α или стабилизация IRF7 — может открыть новые пути для терапии, сочетающей метаболические препараты и иммунные подходы.
Цитирование: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Ключевые слова: рак поджелудочной железы, опухолевое микроокружение, опухолевый метаболизм, макрофаги, лактат