Clear Sky Science · fr
L’axe RASSF1C–HIF‑1α pilote le métabolisme lipidique des macrophages pour favoriser le cancer du pancréas
Pourquoi cette histoire de cancer importe
Le cancer du pancréas est l’un des cancers les plus meurtriers, en partie parce qu’il se loge profondément dans le corps et est souvent détecté tardivement. Mais son agressivité ne s’explique pas uniquement par les cellules tumorales elles‑mêmes. Cette étude montre comment le manque d’oxygène au sein des tumeurs pancréatiques reprogramme à la fois les cellules cancéreuses et les cellules immunitaires environnantes de manière à favoriser la croissance et la dissémination du cancer. En dévoilant cette chaîne d’événements, les chercheurs pointent vers de nouvelles stratégies thérapeutiques ciblant à la fois le métabolisme tumoral et le système immunitaire.
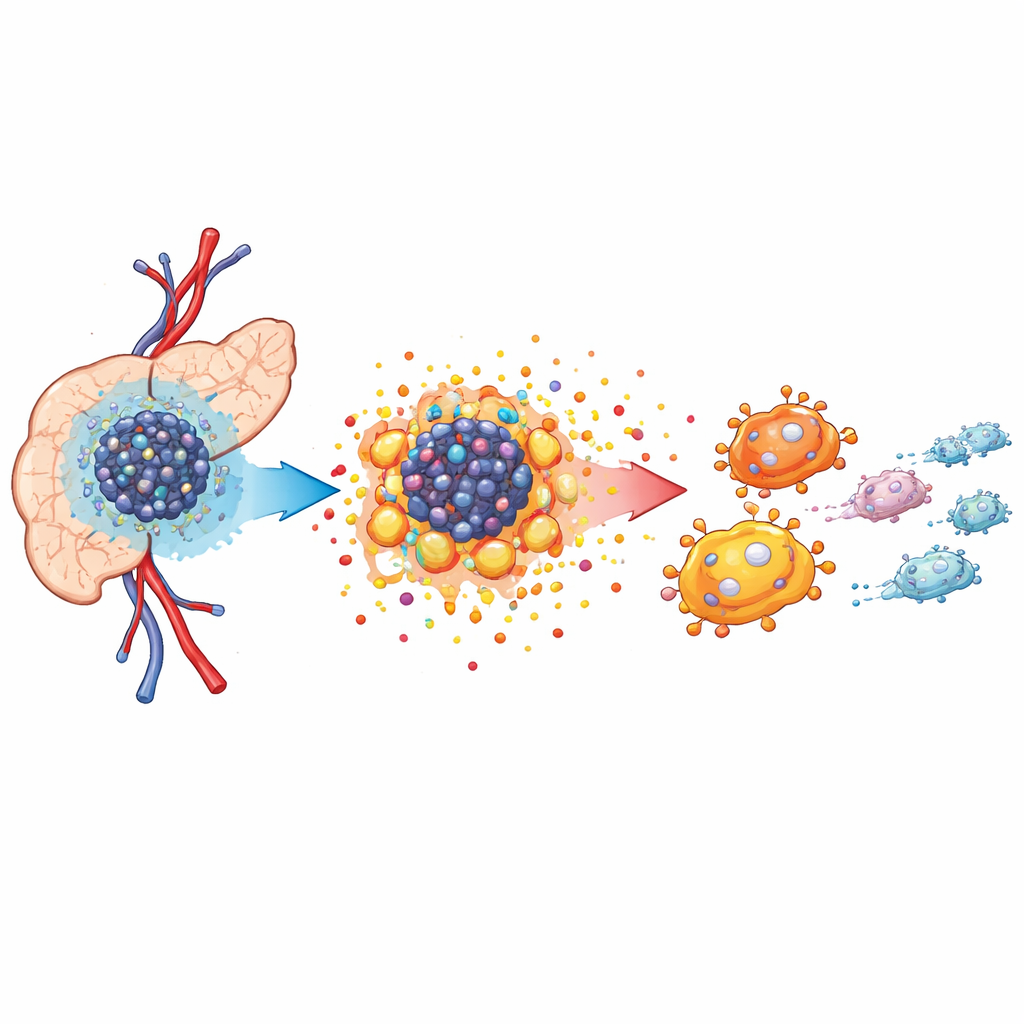
Faible oxygène et un voisinage tumoral affamé
Les tumeurs pancréatiques se développent dans un environnement confiné et hostile appelé microenvironnement tumoral. L’irrigation sanguine y est pauvre, entraînant une chute des niveaux d’oxygène qui force les cellules cancéreuses à modifier leur façon de produire de l’énergie. Grâce au séquençage ARN unicellulaire et à la cartographie spatiale dans des modèles murins, les auteurs montrent que le tissu tumoral est saturé de cellules cancéreuses, de fibroblastes associés à la tumeur et de cellules immunitaires spécialisées appelées macrophages associés à la tumeur. Ces macrophages se groupent près des cellules cancéreuses et adoptent plutôt un rôle favorable à la croissance qu’un rôle anti‑tumoral. L’analyse révèle que les cellules cancéreuses s’appuient fortement sur un métabolisme altéré pour alimenter leur prolifération rapide, préparant ainsi un remodelage plus large de l’environnement tissulaire.
Alimenter le cancer avec du sucre et de l’acide
Lorsque l’oxygène vient à manquer, les cellules cancéreuses favorisent un processus comparable à une combustion rapide et inefficace du glucose, souvent qualifié d’effet Warburg. L’équipe a découvert qu’une variante protéique nommée RASSF1C, précédemment associée au comportement tumoral, est fortement activée en hypoxie. Sous l’égide d’un autre capteur d’oxygène, HIF‑1α, RASSF1C stimule la glycolyse, entraînant une production accrue de lactate et l’acidification du milieu. Dans des expériences sur cellules et animaux, diminuer l’expression de RASSF1C réduisait la production d’acide et ralentissait la croissance tumorale, alors que l’augmenter produisait l’effet inverse. De manière importante, bloquer la formation de lactate avec un médicament atténuait l’avantage de croissance conféré par RASSF1C, montrant que ce basculement métabolique n’est pas un simple effet secondaire mais alimente activement la progression de la maladie.
Comment les sous‑produits tumoraux reprogramment les cellules immunitaires
Le lactate libéré par les cellules tumorales fait plus que modifier la chimie locale : il sert de signal. Lorsque les chercheurs ont exposé des macrophages à un milieu conditionné par des cellules de cancer du pancréas riches en lactate, les macrophages ont basculé vers un état de type M2, favorable à la tumeur. Ils ont produit davantage de facteurs anti‑inflammatoires et moins de molécules associées à l’attaque et à l’élimination des cellules cancéreuses. Chez la souris, les tumeurs présentant des taux élevés de RASSF1C contenaient plus de ces macrophages pro‑tumoraux, un effet qui pouvait être atténué en bloquant la production de lactate. D’autres essais ont montré que le lactate reconfigurait également la façon dont les macrophages gèrent les lipides et le cholestérol, augmentant l’accumulation lipidique d’une manière qui correspond à un micro‑environnement plus propice à la croissance et à la dissémination tumorales.
Un interrupteur de stabilité caché au sein des cellules immunitaires
En creusant davantage, l’étude a mis au jour un commutateur moléculaire reliant le métabolisme tumoral au comportement des cellules immunitaires. Un régulateur immunitaire clé, IRF7, qui favorise normalement un état macrophagique plus vigilant et une gestion lipidique saine, était présent à faible niveau dans les tumeurs pancréatiques. Le lactate provenant des cellules cancéreuses rendait la protéine IRF7 dans les macrophages instable et accélèrait sa dégradation. Cela dépendait d’une autre protéine, UFL1, qui attache une petite étiquette (UFM1) protégeant IRF7 du marquage pour destruction. Le lactate réprimait UFL1 dans les macrophages, inclinant l’équilibre vers un système de marquage qui envoie IRF7 vers la broyeuse protéique de la cellule. Sans IRF7 stable, les macrophages accumulent des défauts métaboliques et aident plus facilement les cellules tumorales à migrer et à envahir les tissus environnants.
Ce que cela signifie pour les traitements futurs
Dans des échantillons tumoraux de patients atteints de cancer du pancréas, les chercheurs ont observé un schéma net : des niveaux plus élevés de RASSF1C et de HIF‑1α dans les cellules tumorales, et des niveaux plus faibles d’UFL1 et d’IRF7 dans les tissus environnants. Ces signatures s’associaient à une maladie plus avancée et à des caractéristiques métastatiques. Ensemble, les résultats décrivent une chaîne dans laquelle l’hypoxie active RASSF1C et HIF‑1α, conduit à une surproduction de lactate et, à son tour, neutralise un frein protecteur UFL1–IRF7 à l’intérieur des macrophages. Pour un public non spécialiste, la conclusion est que le cancer du pancréas prospère en transformant ses propres déchets en armes qui désarment les cellules immunitaires voisines. Interrompre cette chaîne — en limitant le lactate, en bloquant la signalisation RASSF1C–HIF‑1α ou en stabilisant IRF7 — pourrait ouvrir de nouvelles pistes thérapeutiques combinant des médicaments métaboliques et des approches basées sur le système immunitaire.
Citation: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Mots-clés: cancer du pancréas, microenvironnement tumoral, métabolisme tumoral, macrophages, lactate