Clear Sky Science · he
ציר RASSF1C–HIF-1α מכתיב את חילוף החומרים השומני במקרופאג׳ים ומקדם סרטן הלבלב
מדוע הסיפור הזה על סרטן חשוב
סרטן הלבלב הוא מאחד מסוגי הסרטן הקטלניים ביותר, בין השאר כי הוא מתמקם עמוק בגוף ועולה לעתים קרובות רק בשלבים מתקדמים. עם זאת, האגרסיביות שלו אינה נובעת רק מתאים סרטניים עצמם. המחקר הזה מראה כיצד חוסר בחמצן בתוך גידולי הלבלב משנה הן את תאי הסרטן והן את תאי החיסון הסמוכים באופן שמסייע לגידול ולתפשטות. בחשיפת שרשרת האירועים הזו מצביעים החוקרים על דרכי התערבות חדשות שיכולות לתקוף את המחלה על ידי מיקוד גם במטבוליזם של הגידול וגם במערכת החיסון.
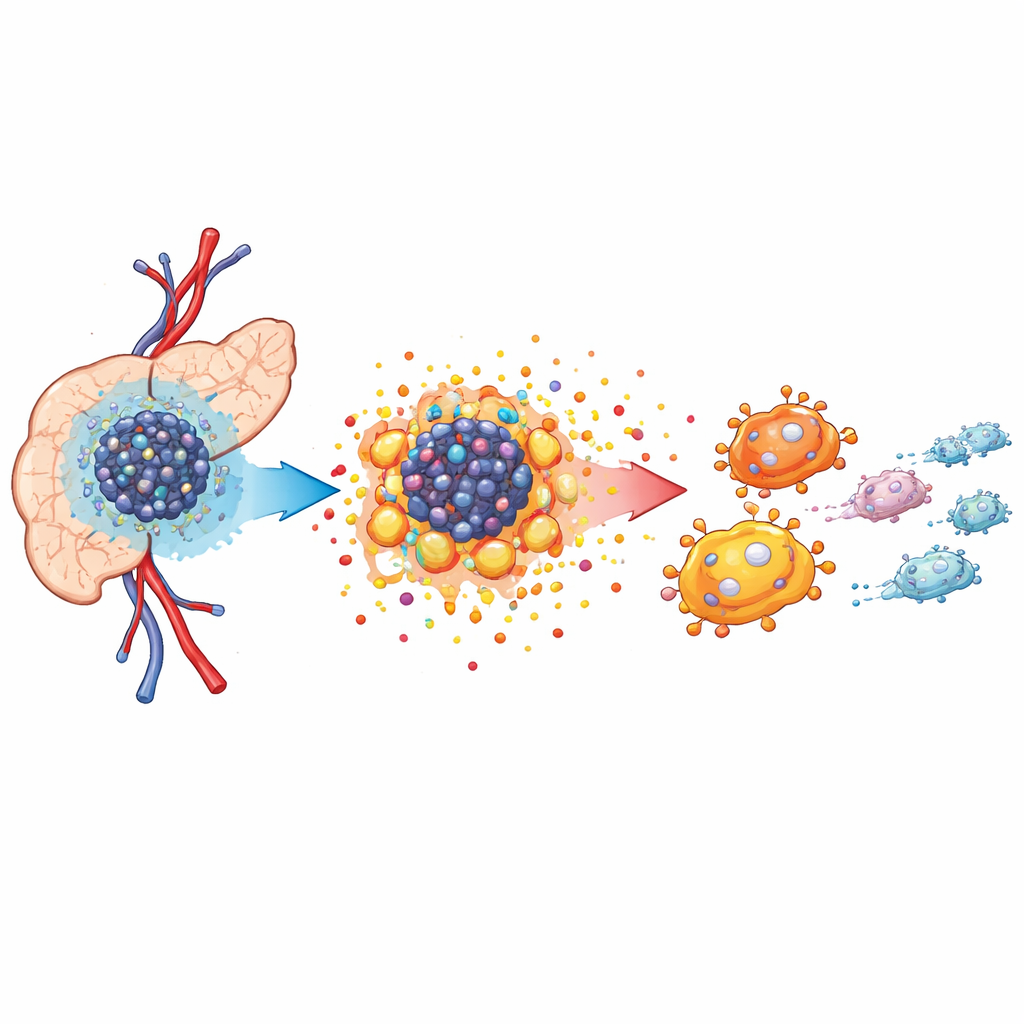
חמצן נמוך ושכונה רעבה סביב הגידול
גידולי הלבלב גדלים בשכונה צפופה ועוינת המוכרת כמיקרו‑סביבה גידולית. אספקת הדם דלה, כך שרמות החמצן יורדות והן מאלצות את תאי הסרטן לשנות את האופן שבו הם מייצרים אנרגיה. באמצעות ריצוף RNA בודדי‑תאים ומיפוי מרחבי במודלים עכבריים הראו המחברים כי רקמת הגידול מלאה בתאים סרטניים, בפיברובלסטים מקושרים לגידול ובתאי חיסון מיוחדים המכונים מקרופאג׳ים קשורים לגידול. מקרופאג׳ים אלה מתקבצים סמוך לתאים הסרטניים ונוטים לאמץ תפקיד התומך בצמיחה במקום תפקיד הלחימה בסרטן. הניתוח חשף שתאי הסרטן מסתמכים במידה רבה על מטבוליזם משונה להאצת הצמיחה, מה שיוצר קרקע לשינוי רחב יותר של סביבת הרקמה.
הזנת הסרטן בסוכר ובחומציות
כשחמצן חסר, תאי הסרטן נשענים על תהליך דומה לשריפת סוכר מהירה ולא‑יעילה, הידוע לעתים כאפקט וורבורג. הצוות מצא שגרסה חלבונית בשם RASSF1C, שהייתה מקושרת בעבר להתנהגות סרטנית, מופעלת בעוצמה בתנאי חוסר חמצן. בהנחיית חלבון חיישן חמצן נוסף, HIF-1α, RASSF1C מגבירה את שיעור הגליקוליזה, מה שמוביל לייצור מוגבר של חומצה לקטית ולהחמצת המיקרו‑סביבה. בניסויים בתאים ובעכברים, דיכוי RASSF1C הפחית את ייצור החומציות והאט את צמיחת הגידול, בעוד שהגברת הביטוי הפכה את המצב. חשוב לציין כי חסימת היווצרות לקטט בעזרת תרופה החלישה את יתרון הצמיחה שנתנה RASSF1C, מה שמראה שהשינוי המטבולי אינו רק תוצאה לוואי — הוא מזין במישרין את התקדמות המחלה.
כיצד תוצרי הגידול מתכנתים מחדש את תאי החיסון
הלקטט שמשתחרר מתאים סרטניים עושה יותר משלשנות את הכימיה המקומית; הוא פועל כאות. כאשר החוקרים חשפו מקרופאג׳ים לנוזל מותנה שהכיל ריכוזי לקטט גבוהים מתאי סרטן הלבלב, המקרופאג׳ים עברו למצב דמוי M2 שתומך בגידול. הם ייצרו יותר גורמים אנטי‑דלקתיים ופחות מולקולות המקושרות להתקפה ולניקוי תאים סרטניים. בעכברים, בגידולים עם רמות גבוהות של RASSF1C נמצאו יותר מקרופאג׳ים פרו‑גידוליים — אפקט שניתן היה להחלישו באמצעות חסימת ייצור לקטט. בדיקות נוספות הראו שלקטט גם שינה את האופן שבו מקרופאג׳ים מעבדים שומנים וכולסטרול, והגביר הצטברות שומנים באופן שמתיישב עם נישה תומכת‑גידול המקדמת נדידה ותפוצה.
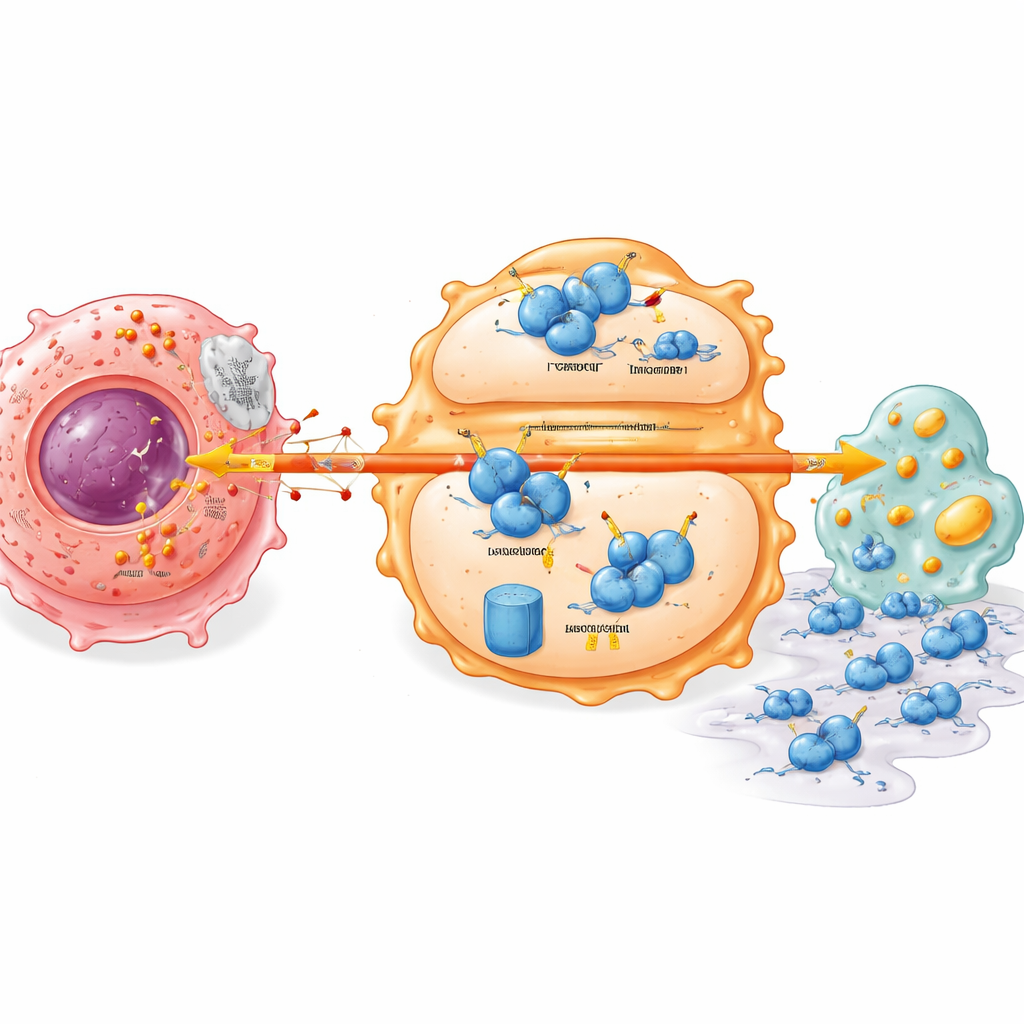
מפתח יציבות נסתר בתוך תאי החיסון
בחקר עמוק יותר חשף המחקר מתג מולקולרי שמקשר בין מטבוליזם הגידול להתנהגות תאי החיסון. בודד מרכזי של מערכת החיסון בשם IRF7, שבמצב רגיל תומך במצב מקרופאג׳י ערני ומוכן לתקיפה ובטיפול נכון בשומנים, נמצא ברמות נמוכות בגידולי הלבלב. הלקטט מהתאים הסרטניים גרם לחלבון IRF7 במקרופאג׳ים להיות פחות יציב ולהתפרק מהר יותר. תהליך זה היה תלוי בחלבון נוסף, UFL1, שמצמיד תג מגן קטן (UFM1) המגן על IRF7 מסימון להרס. הלקטט דיכא את UFL1 במקרופאג׳ים, ובכך הטה את המאזן למערכת תגיות ששולחת את IRF7 למגרסת החלבונים של התא. ללא IRF7 יציב, מקרופאג׳ים מצטברים בחסרונות מטבוליים ותורמים ביתר קלות לתנועה ולהתפשטות של תאים סרטניים ברקמה הסובבת.
מה משמעות הדבר לטיפולים עתידיים
בדגימות גידול מאנשים עם סרטן הלבלב ראו החוקרים דפוס ברור: רמות גבוהות של RASSF1C ו‑HIF-1α בתאים הסרטניים, ורמות נמוכות של UFL1 ו‑IRF7 ברקמה הסמוכה. הדפוסים הללו תואמו למחלה מתקדמת יותר ולמאפייני גרורה. יחד, הממצאים מתארים שרשרת שבה חמצן נמוך מפעיל את RASSF1C ו‑HIF-1α, ממריץ ייצור לקטט מופרז, ובתמורה משתק ברקס מגן של UFL1–IRF7 בתוך מקרופאג׳ים. לקורא ההמוני, המסקנה היא שסרטון הלבלב משגשג על ידי הפיכת תוצרי הפסולת שלו לנשק שמנטרל תאי חיסון סמוכים. הפרעה בשרשרת הזו — על ידי הגבלת לקטט, חסימת איתות RASSF1C–HIF-1α או ייצוב IRF7 — עשויה לפתוח דרכים חדשות לטיפולים שמשלבים תרופות מטבוליות עם גישות מבוססות חיסון.
ציטוט: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
מילות מפתח: סרטן הלבלב, מיקרו‑סביבה גידולית, מטבוליזם של גידול, מקרופאג׳ים, חומצה לקטית