Clear Sky Science · it
L’asse RASSF1C-HIF-1α guida il metabolismo lipidico dei macrofagi per promuovere il cancro del pancreas
Perché questa ricerca sul cancro è importante
Il cancro del pancreas è uno dei tumori più letali, in parte perché si annida in profondità nell’addome e viene spesso diagnosticato in fase avanzata. Ma la sua aggressività non dipende solo dalle cellule tumorali. Questo studio mostra come la carenza di ossigeno all’interno dei tumori pancreatici riorganizzi sia le cellule tumorali sia le cellule immunitarie vicine in modo da favorire la crescita e la diffusione del tumore. Svelando questa catena di eventi, i ricercatori indicano nuove strategie per colpire la malattia agendo sul metabolismo tumorale e sul sistema immunitario.
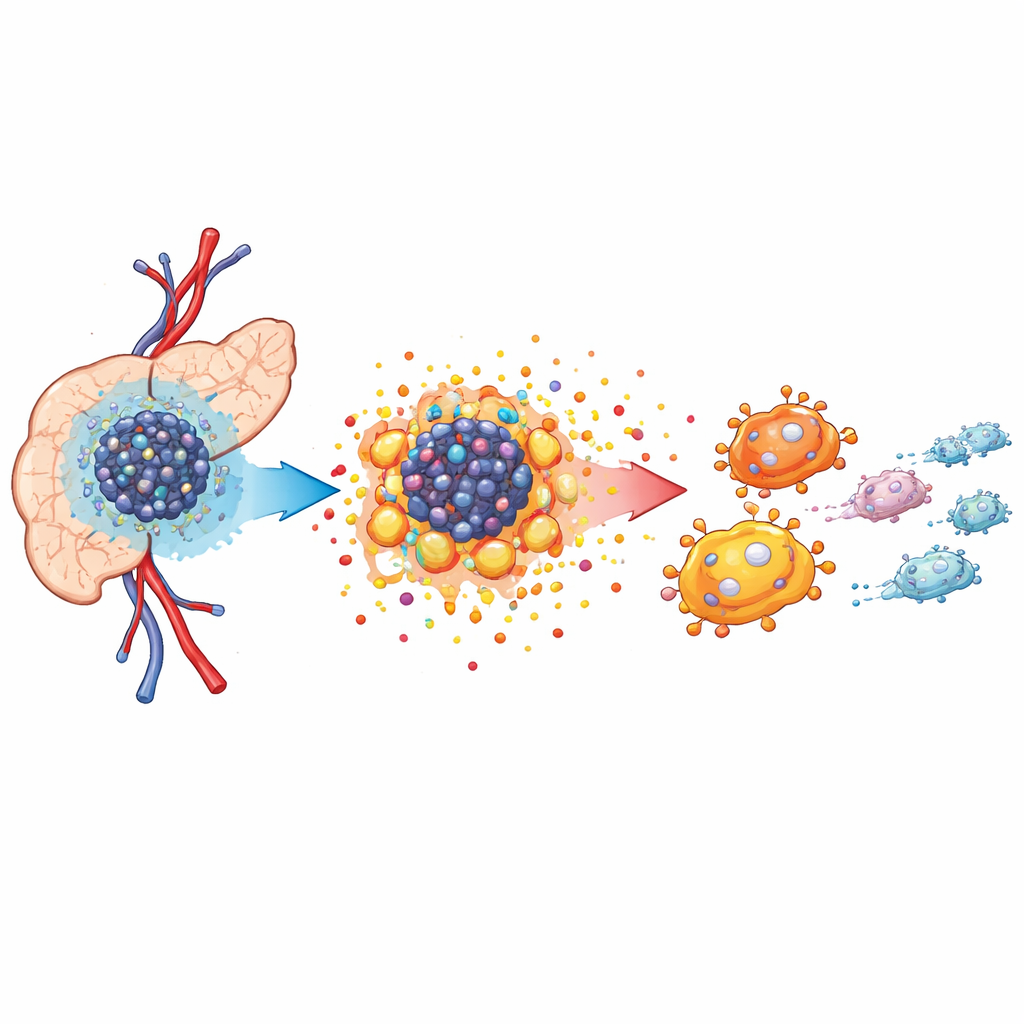
Basso ossigeno e un vicinato tumorale affamato
I tumori pancreatici crescono in un microambiente affollato e ostile. L’apporto di sangue è scadente, quindi i livelli di ossigeno calano, costringendo le cellule tumorali a modificare il modo in cui producono energia. Utilizzando sequenziamento dell’RNA a singola cellula e mappature spaziali in modelli murini, gli autori hanno mostrato che il tessuto tumorale è popolato da cellule tumorali, fibroblasti associati al tumore e cellule immunitarie specializzate chiamate macrofagi associati al tumore. Questi macrofagi si raggruppano vicino alle cellule tumorali e tendono ad assumere un ruolo che sostiene la crescita piuttosto che combattere il cancro. L’analisi ha rivelato che le cellule tumorali dipendono fortemente da un metabolismo alterato per sostenere la rapida crescita, preparandosi così a una rimodellamento più ampio dell’ambiente tissutale.
Alimentare il cancro con zucchero e acidità
Quando l’ossigeno scarseggia, le cellule tumorali si affidano a un processo simile a una combustione rapida e inefficiente degli zuccheri, spesso chiamato effetto Warburg. Il gruppo ha scoperto che una variante proteica denominata RASSF1C, precedentemente associata al comportamento tumorale, si attiva fortemente in condizioni di ipossia. Guidata da un altro sensore dell’ossigeno, HIF-1α, RASSF1C potenzia la glicolisi, portando a un’elevata produzione di lattato e all’acidificazione dell’ambiente circostante. In esperimenti su cellule e animali, la riduzione di RASSF1C diminuiva la produzione di acidità e rallentava la crescita del tumore, mentre la sua sovraespressione aveva l’effetto opposto. Inoltre, bloccare la formazione di lattato con un farmaco attenuava il vantaggio di crescita conferito da RASSF1C, dimostrando che questo cambiamento metabolico non è solo un effetto collaterale, ma alimenta attivamente la progressione della malattia.
Come i prodotti di scarto tumorali riprogrammano le cellule immunitarie
Il lattato rilasciato dalle cellule tumorali fa più che modificare la chimica locale; agisce come segnale. Quando i ricercatori hanno esposto i macrofagi a un fluido condizionato da cellule di cancro pancreatico ricche di lattato, i macrofagi sono passati a uno stato di tipo M2, che sostiene il tumore. Hanno prodotto più fattori anti-infiammatori e meno molecole associate all’attacco e all’eliminazione delle cellule tumorali. Nei topi, i tumori con alti livelli di RASSF1C contenevano un maggior numero di questi macrofagi pro-tumorali, un effetto che poteva essere attenuato bloccando la produzione di lattato. Ulteriori test hanno mostrato che il lattato riorganizza anche il modo in cui i macrofagi gestiscono i grassi e il colesterolo, aumentando l’accumulo lipidico in modi coerenti con la creazione di una nicchia più favorevole alla crescita e alla dispersione del tumore.
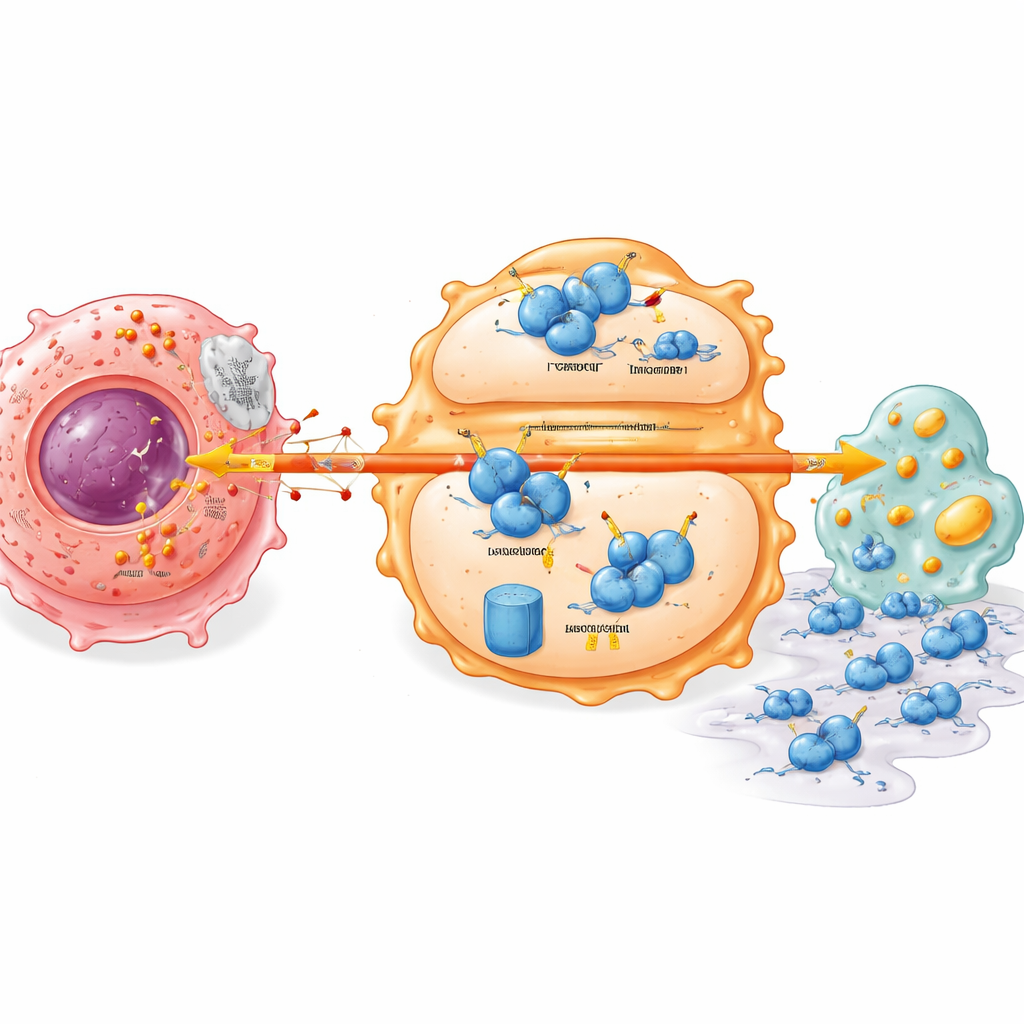
Un interruttore di stabilità nascosto nelle cellule immunitarie
Approfondendo, lo studio ha scoperto un interruttore molecolare che collega il metabolismo tumorale al comportamento delle cellule immunitarie. Un regolatore chiave del sistema immunitario chiamato IRF7, che normalmente sostiene uno stato dei macrofagi più vigile e pronto all’attacco e una gestione lipidica corretta, è risultato presente a livelli ridotti nei tumori pancreatici. Il lattato proveniente dalle cellule tumorali rendeva la proteina IRF7 nei macrofagi instabile e ne accelerava la degradazione. Questo dipendeva da un’altra proteina, UFL1, che aggiunge un piccolo tag (UFM1) che protegge IRF7 dall’essere segnato per la distruzione. Il lattato sopprimeva UFL1 nei macrofagi, spostando l’equilibrio verso un sistema di marcatura che invia IRF7 al trituratore proteico della cellula. Senza IRF7 stabile, i macrofagi accumulano difetti metabolici e facilitano più facilmente la migrazione e l’invasione delle cellule tumorali nei tessuti circostanti.
Cosa significa per i trattamenti futuri
Nei campioni tumorali di pazienti con cancro del pancreas, i ricercatori hanno osservato un quadro chiaro: livelli più alti di RASSF1C e HIF-1α nelle cellule tumorali e livelli più bassi di UFL1 e IRF7 nei tessuti circostanti. Questi schemi corrispondevano a una malattia più avanzata e a caratteristiche metastatiche. Nel complesso, i risultati delineano una catena in cui la bassa ossigenazione attiva RASSF1C e HIF-1α, stimola la sovrapproduzione di lattato e, a sua volta, disabilita il freno protettivo UFL1–IRF7 all’interno dei macrofagi. Per i lettori non specialisti, la conclusione è che il cancro del pancreas prospera trasformando i propri prodotti di scarto in armi che disarmano le cellule immunitarie vicine. Interrompere questa catena — limitando il lattato, bloccando la segnalazione RASSF1C–HIF-1α o stabilizzando IRF7 — potrebbe aprire nuove strade terapeutiche che combinano farmaci metabolici con approcci basati sul sistema immunitario.
Citazione: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Parole chiave: cancro del pancreas, microambiente tumorale, metabolismo tumorale, macrofagi, lattato