Clear Sky Science · tr
RASSF1C-HIF-1α ekseni, pankreas kanserini desteklemek için makrofaj lipid metabolizmasını yönlendiriyor
Bu kanser öyküsü neden önemli
Pankreas kanseri en öldürücü kanserlerden biridir; kısmen derinde saklanması ve genellikle geç bulunması nedeniyle. Ancak saldırganlığı sadece tümör hücrelerinin kendisiyle ilgili değildir. Bu çalışma, pankreas tümörlerinin içindeki oksijen eksikliğinin hem kanser hücrelerini hem de yakınlardaki bağışıklık hücrelerini kanserin büyümesini ve yayılmasını kolaylaştıracak şekilde yeniden programladığını gösteriyor. Araştırmacılar bu olay zincirini açığa çıkararak tümör metabolizmasını ve bağışıklık sistemini hedefleyen yeni saldırı yollarına işaret ediyor.
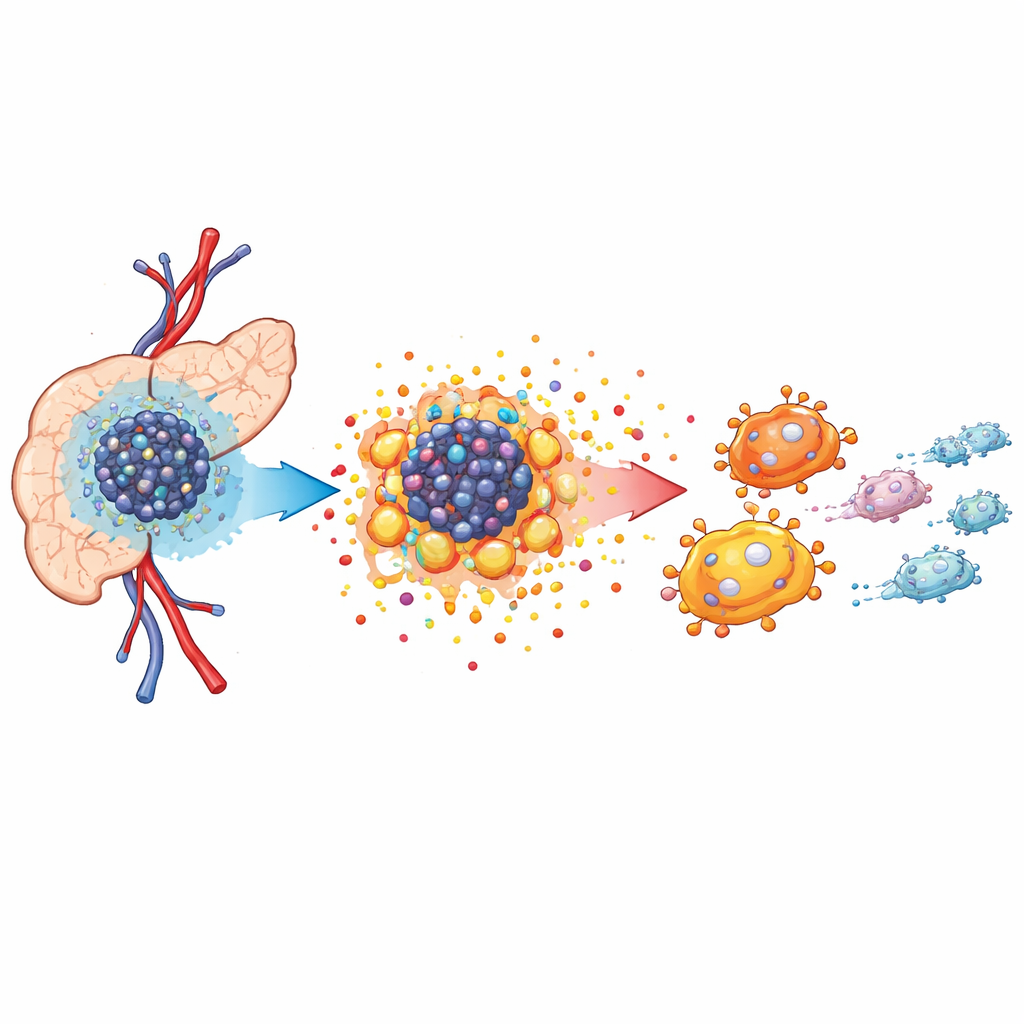
Düşük oksijen ve aç bir tümör çevresi
Pankreas tümörleri, tümör mikroçevresi olarak bilinen kalabalık ve elverişsiz bir ortamda büyür. Kan akışı zayıftır, bu yüzden oksijen seviyeleri düşer ve kanser hücreleri enerji üretme yollarını değiştirmeye zorlanır. Fare modellerinde tek hücre RNA dizileme ve mekânsal eşleştirme kullanan yazarlar, tümör dokusunun kanser hücreleri, tümör ilişkili fibroblastlar ve tümörle ilişkili makrofajlar diye adlandırılan özelleşmiş bağışıklık hücreleriyle dolu olduğunu gösterdi. Bu makrofajlar kanser hücrelerinin yakınında kümelenir ve kanseri yok etmeye çalışmaktan çok büyümeyi destekleyen bir rol üstlenme eğilimindedir. Analiz, kanser hücrelerinin hızlı büyümeyi beslemek için değişmiş metabolizmaya güçlü biçimde dayandığını ortaya koydu ve bu da doku ortamının daha geniş çapta yeniden şekillenmesi için zemin hazırladı.
Kanseri şeker ve asitle beslemek
Oksijen kıt olduğunda, kanser hücreleri genellikle hızlı fakat verimsiz şeker yakımına benzeyen bir süreç olan Warburg etkisine yönelir. Ekip, daha önce kanser davranışıyla ilişkilendirilmiş bir protein varyantı olan RASSF1C'nin düşük oksijende güçlü biçimde aktifleştiğini buldu. Oksijeni algılayan başka bir protein olan HIF-1α tarafından yönlendirilen RASSF1C, glikolizi artırarak yüksek düzeyde laktat üretimine ve çevrenin asitlenmesine yol açıyor. Hücre ve hayvan deneylerinde RASSF1C’yi azaltmak asit üretimini düşürdü ve tümör büyümesini yavaşlattı; artırmak ise ters etki yarattı. Önemli olarak, bir ilaçla laktat oluşumunu engellemek RASSF1C’nin sağladığı büyüme avantajını azalttı; bu da bu metabolik değişimin yalnızca bir yan etki olmadığını, hastalık ilerlemesini aktif olarak beslediğini gösteriyor.
Tümör yan ürünleri bağışıklık hücrelerini nasıl yeniden programlıyor
Tümör hücrelerinin saldığı laktat yerel kimyayı değiştirmekten öte bir sinyal görevi görür. Araştırmacılar, laktatça zengin pankreas kanseri hücrelerinin kondisyone ortamında bekletilen makrofajların M2-benzeri, tümörü destekleyen bir duruma kaydığını gözlemledi. Bu makrofajlar daha fazla anti-inflamatuar faktör üretirken, kanser hücrelerini hedef alma ve temizlemeyle ilişkilendirilen moleküllerden daha az yaptı. Farelerde yüksek RASSF1C düzeyine sahip tümörler bu pro-tümör makrofajları daha fazla barındırıyordu; bu etki laktat üretimi engellenerek azaltılabiliyordu. İleri testler laktatın ayrıca makrofajların yağ ve kolesterol işleyişini de yeniden düzenlediğini, lipid birikimini artırdığını ve bunun da tümör büyümesini ve yayılmasını destekleyen bir nişle örtüştüğünü gösterdi.
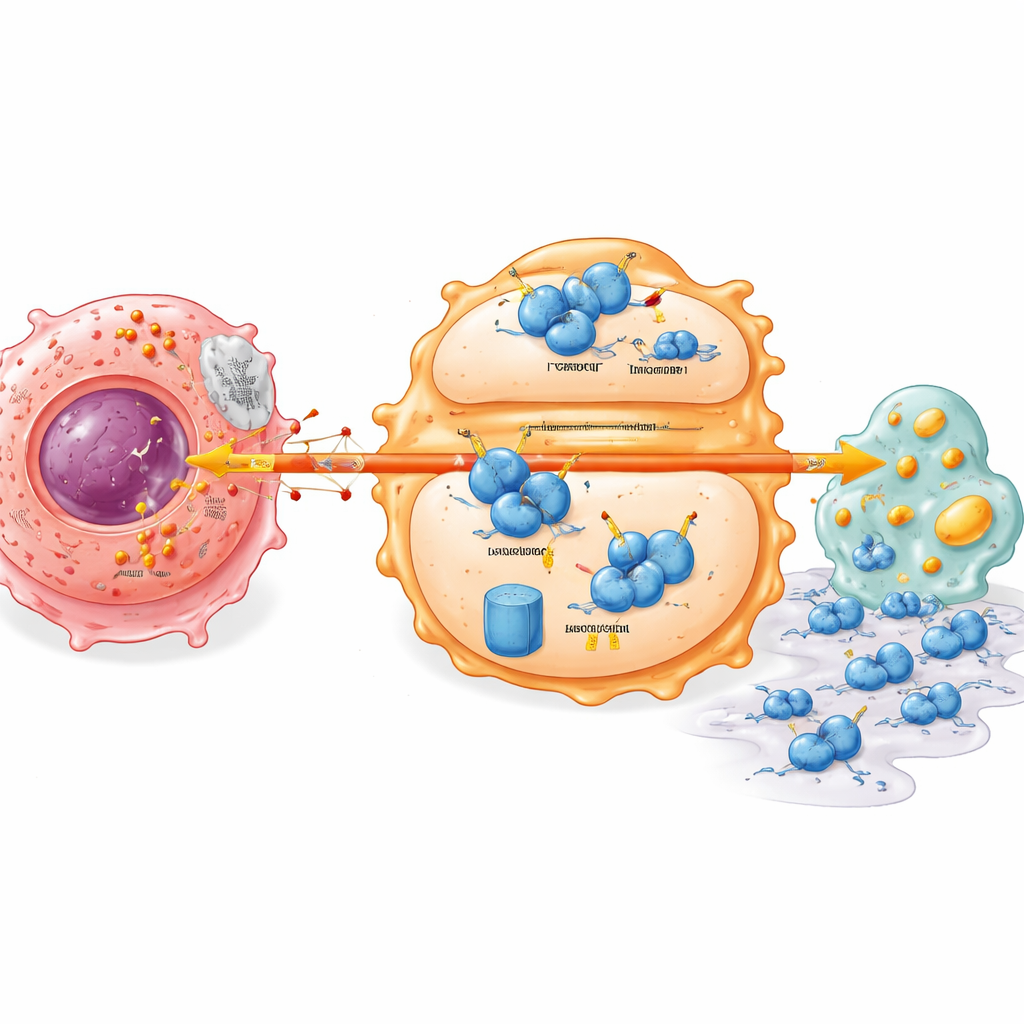
Bağışıklık hücrelerinin içinde gizli bir stabilite anahtarı
Daha derine indikçe çalışma, tümör metabolizması ile bağışıklık hücresi davranışı arasında bağlantı kuran moleküler bir anahtar keşfetti. Normalde daha uyanık, saldırıya hazır makrofaj durumunu ve sağlıklı lipid yönetimini destekleyen bir bağışıklık düzenleyicisi olan IRF7, pankreas tümörlerinde düşük düzeyde bulundu. Kanser hücrelerinden gelen laktat, makrofajlardaki IRF7 proteinini kararsız hale getirip daha hızlı parçalanmasına neden oldu. Bu, IRF7'yi yıkımdan koruyan küçük bir etiket (UFM1) ekleyen UFL1 adlı başka bir proteine bağlıydı. Laktat makrofajlarda UFL1’i baskıladı ve dengeyi IRF7’yi hücrenin protein öğütücüsüne gönderen etiketleme sistemine kaydırdı. Stabil IRF7 olmadığında, makrofajlar metabolik kusurlar biriktirir ve tümör hücrelerinin göç etmesine ve çevre dokulara invaze olmasına daha kolay yardımcı olur.
Gelecekteki tedaviler için ne anlama geliyor
Pankreas kanseri olan insanlardan alınan tümör örneklerinde araştırmacılar belirgin bir desen gördü: tümör hücrelerinde daha yüksek RASSF1C ve HIF-1α seviyeleri ile çevre dokuda daha düşük UFL1 ve IRF7 seviyeleri. Bu desenler daha ileri hastalık ve metastatik özelliklerle örtüştü. Bulgular, düşük oksijenin RASSF1C ve HIF-1α’yı aktifleştirdiği, laktat aşırı üretimini tetiklediği ve bunun da makrofajlar içinde koruyucu bir UFL1–IRF7 frenini devre dışı bıraktığı bir zinciri özetliyor. Halk için çıkarım şudur: pankreas kanseri, kendi atık ürünlerini yakın bağışıklık hücrelerini etkisiz hale getiren silahlara dönüştürerek gelişir. Bu zinciri kesmek—laktatı sınırlamak, RASSF1C–HIF-1α sinyalini engellemek veya IRF7’yi stabilize etmek—metabolik ilaçları bağışıklık temelli yaklaşımlarla birleştiren yeni tedavi yolları açabilir.
Atıf: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Anahtar kelimeler: pankreas kanseri, tümör mikroçevresi, tümör metabolizması, makrofajlar, laktat