Clear Sky Science · ja
RASSF1C–HIF-1α軸がマクロファージの脂質代謝を駆動し膵臓がんを促進する
このがん研究が重要な理由
膵臓がんは発見が遅れやすく体内深部に潜むため、最も致死率の高いがんの一つです。しかしその凶暴さは腫瘍細胞自体だけの問題ではありません。本研究は、膵臓腫瘍内の酸素不足ががん細胞と近傍の免疫細胞の両方の振る舞いを書き換え、がんの増殖と転移を助ける仕組みを示しています。この連鎖を明らかにすることで、腫瘍の代謝と免疫系の双方を標的にする新しい治療戦略の可能性が示されます。
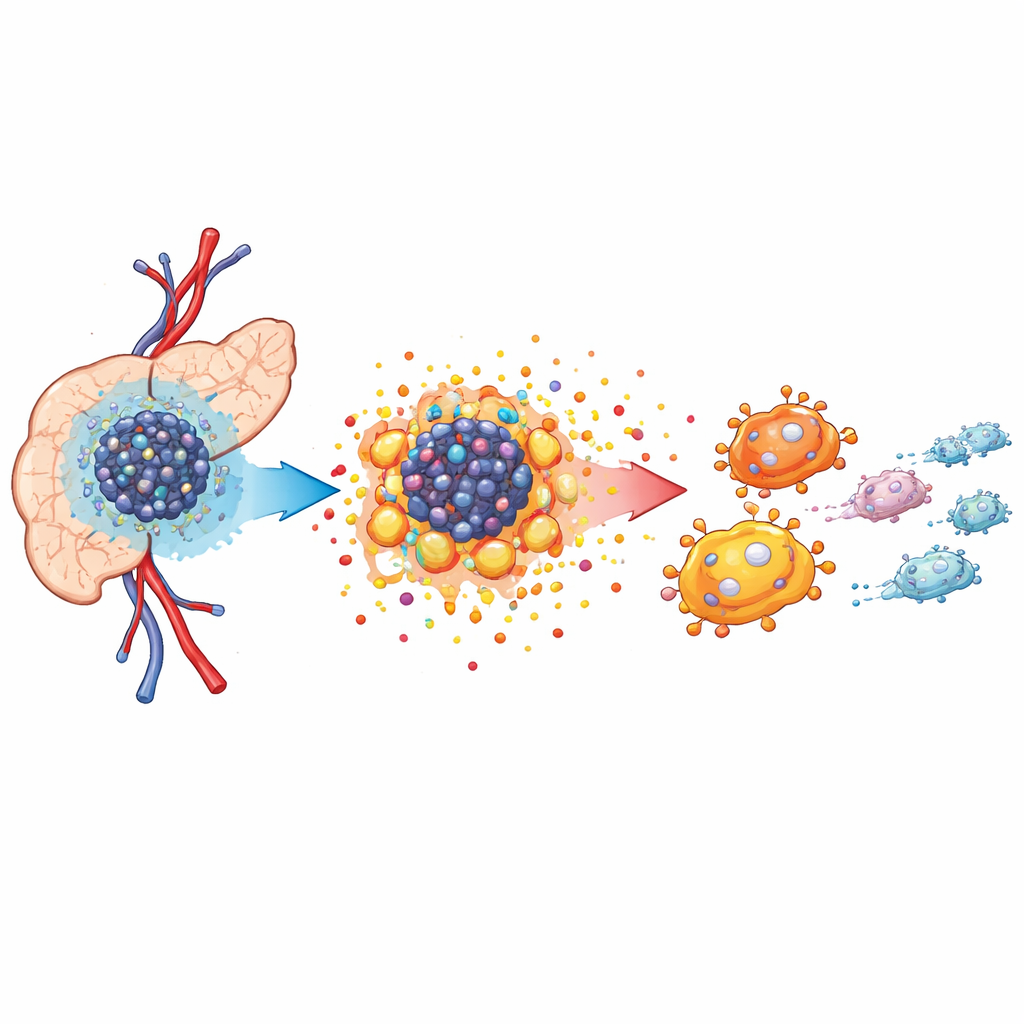
低酸素と飢えた腫瘍の周辺環境
膵臓腫瘍は腫瘍微小環境と呼ばれる混雑し過酷な領域で成長します。血流が乏しく酸素濃度が低下するため、がん細胞はエネルギー産生の方法を変えざるを得ません。マウスモデルでの単一細胞RNAシーケンスと空間マッピングにより、腫瘍組織はがん細胞、がん関連線維芽細胞、そして腫瘍関連マクロファージと呼ばれる特殊な免疫細胞で密に満たされていることが示されました。これらのマクロファージはがん細胞の近くに集まり、がんと戦うよりも増殖を支援する役割を取りがちです。解析は、がん細胞が急速な増殖を支えるために大きく代謝を変化させていることを明らかにし、組織環境全体の再構築の舞台を整えていることを示しました。
糖と酸でがんに燃料を供給する
酸素が不足すると、がん細胞は速いが非効率的な糖代謝に依存するようになり、一般にワールブルグ効果と呼ばれる過程を強めます。研究チームは、以前からがんの振る舞いに関連していたタンパク質変異体RASSF1Cが低酸素下で強く活性化されることを見出しました。酸素を感知する別のタンパク質HIF-1αに駆動されるRASSF1Cは解糖系を促進し、乳酸の大量生産と周囲の酸性化を引き起こします。細胞や動物での実験では、RASSF1Cを抑えると酸の産生が減り腫瘍の成長が遅くなり、逆に増強するとその反対の効果が見られました。重要なのは、乳酸生成を薬剤で阻害するとRASSF1Cによる成長優位が弱まったことで、こうした代謝シフトが単なる副産物ではなく疾患進行を能動的に駆動していることが示された点です。
腫瘍の副産物が免疫細胞を書き換える仕組み
腫瘍細胞が放出する乳酸は局所の化学環境を変えるだけでなく、シグナルとして機能します。研究者らが乳酸を多く含む膵臓がん細胞の条件培養上清でマクロファージを処理すると、これらのマクロファージはM2様の腫瘍支持的な状態へと変化しました。抗炎症性因子の産生が増え、がん細胞の攻撃や除去に結びつく分子は減少しました。マウスではRASSF1Cが高い腫瘍ほどこれらの腫瘍促進マクロファージが多く存在し、この効果は乳酸産生を阻害することで弱められました。さらに実験を進めると、乳酸はマクロファージの脂質やコレステロールの扱い方も書き換え、脂質の蓄積を増やして腫瘍の成長と転移を助ける支援的な環境に一致する変化をもたらすことが分かりました。
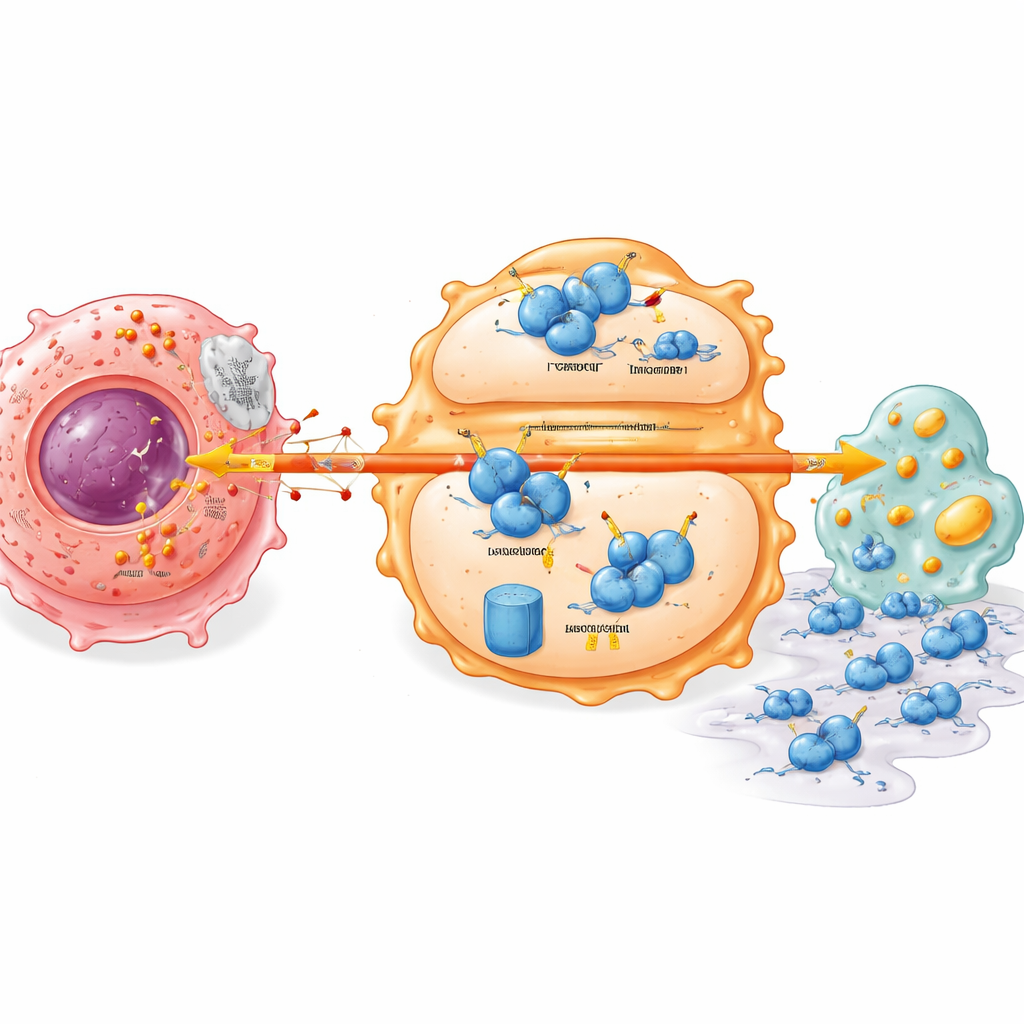
免疫細胞内部の隠れた安定化スイッチ
さらに掘り下げると、腫瘍代謝と免疫細胞の挙動を結ぶ分子スイッチが明らかになりました。通常はより厳戒心のある攻撃的なマクロファージ状態と健全な脂質処理を支える主要な免疫調節因子IRF7が膵臓腫瘍では低量であることが見つかりました。がん細胞由来の乳酸はマクロファージ内のIRF7タンパク質を不安定にし、分解を早めます。この過程にはUFL1という別のタンパク質が関与しており、UFL1はUFM1という小さなタグを付けてIRF7を破壊マークから守ります。乳酸はマクロファージでUFL1を抑制し、IRF7を細胞のタンパク質分解機構へ送り込む標識系へと傾けます。安定したIRF7が失われると、マクロファージは代謝的欠陥を蓄積し、がん細胞の遊走や浸潤を手助けしやすくなります。
将来の治療にとっての意義
膵臓がん患者の腫瘍サンプルでは、腫瘍細胞におけるRASSF1CとHIF-1αの高発現と、周辺組織におけるUFL1とIRF7の低発現という明確なパターンが確認されました。これらのパターンは進行した病期や転移の特徴と一致していました。総じて、低酸素がRASSF1CとHIF-1αを活性化し、乳酸の過剰生産を引き起こし、その結果マクロファージ内部の保護的なUFL1–IRF7ブレーキを無効化する一連の連鎖が描き出されます。一般向けの要点としては、膵臓がんは自らの廃棄物を武器に変え、近傍の免疫細胞の力をそぎ落とすことで繁栄しているということです。この連鎖を断ち切る—乳酸を制限する、RASSF1C–HIF-1αシグナルを阻害する、あるいはIRF7を安定化する—ことで、代謝薬と免疫療法を組み合わせた新たな治療法の道が開ける可能性があります。
引用: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
キーワード: 膵臓がん, 腫瘍微小環境, 腫瘍代謝, マクロファージ, 乳酸