Clear Sky Science · es
El eje RASSF1C-HIF-1α impulsa el metabolismo lipídico de los macrófagos para promover el cáncer de páncreas
Por qué importa esta historia sobre el cáncer
El cáncer de páncreas es uno de los más letales, en parte porque se oculta profundamente en el cuerpo y a menudo se detecta tarde. Pero su agresividad no depende solo de las células tumorales. Este estudio muestra cómo la falta de oxígeno dentro de los tumores pancreáticos reconecta tanto a las células cancerosas como a las células inmunitarias cercanas de una manera que favorece el crecimiento y la diseminación del tumor. Al desvelar esta cadena de eventos, los investigadores señalan nuevas formas de atacar la enfermedad dirigidas tanto al metabolismo tumoral como al sistema inmunitario.
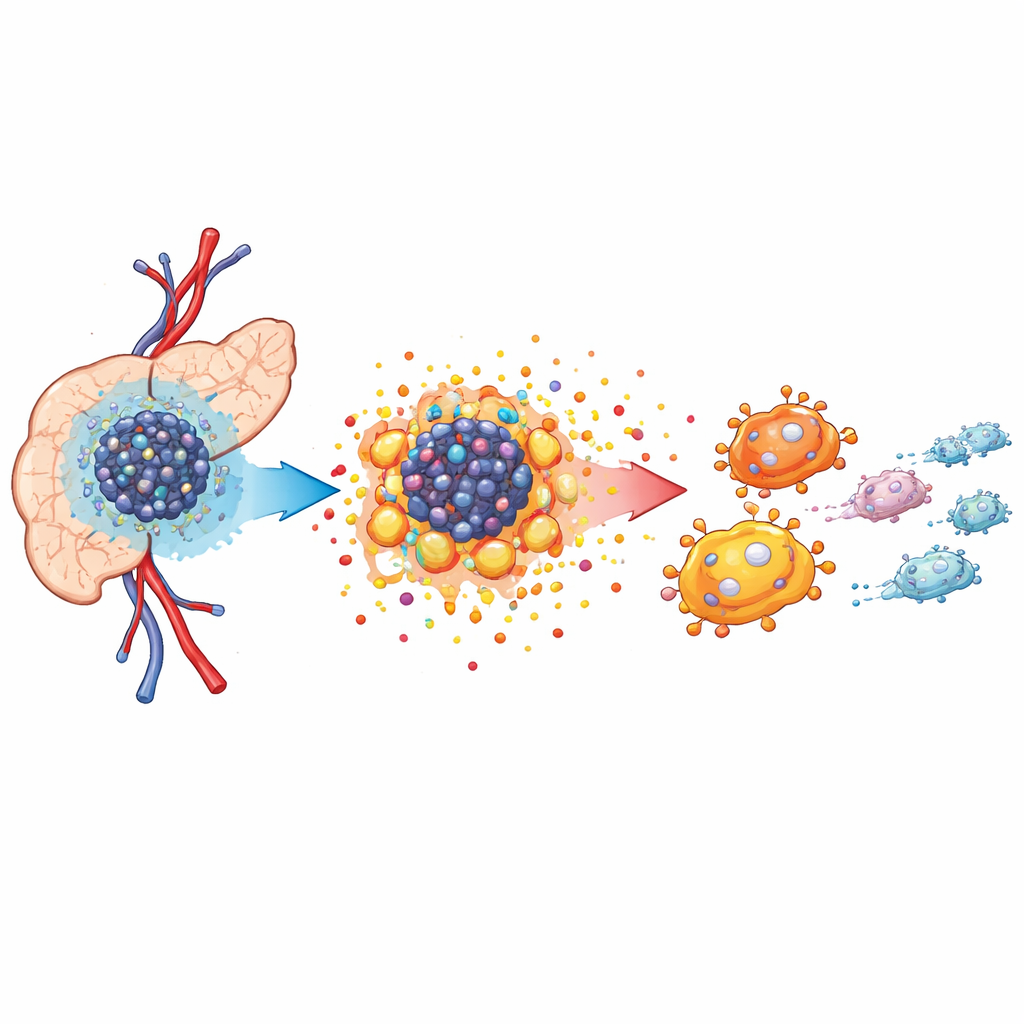
Bajo oxígeno y un vecindario tumoral hambriento
Los tumores pancreáticos crecen en un vecindario concurrido y hostil conocido como microambiente tumoral. El suministro de sangre es pobre, por lo que los niveles de oxígeno bajan y obligan a las células cancerosas a cambiar la forma en que obtienen energía. Usando secuenciación de ARN a nivel de célula única y mapeo espacial en modelos de ratón, los autores mostraron que el tejido tumoral está repleto de células cancerosas, fibroblastos asociados al tumor y células inmunitarias especializadas llamadas macrófagos asociados al tumor. Estos macrófagos se agrupan cerca de las células cancerosas y tienden a adoptar un papel que apoya el crecimiento, en lugar de combatir el cáncer. El análisis reveló que las células tumorales dependen en gran medida de un metabolismo alterado para alimentar el rápido crecimiento, lo que prepara el terreno para una remodelación más amplia del entorno tisular.
Alimentando el cáncer con azúcar y ácido
Cuando el oxígeno escasea, las células cancerosas recurren a un proceso similar a una combustión rápida e ineficiente de azúcares, a menudo llamado efecto Warburg. El equipo encontró que una variante proteica llamada RASSF1C, vinculada previamente al comportamiento canceroso, se activa de forma intensa en condiciones de baja oxigenación. Impulsada por otra proteína sensible al oxígeno, HIF-1α, RASSF1C potencia la glucólisis, lo que conduce a una alta producción de lactato y a la acidificación del entorno. En experimentos celulares y en animales, reducir RASSF1C disminuyó la producción de ácido y frenó el crecimiento tumoral, mientras que aumentarlo tuvo el efecto contrario. De forma importante, bloquear la formación de lactato con un fármaco atenuó la ventaja de crecimiento conferida por RASSF1C, mostrando que este cambio metabólico no es solo un efecto colateral: alimenta activamente la progresión de la enfermedad.
Cómo los subproductos tumorales reprograman las células inmunitarias
El lactato liberado por las células tumorales hace más que cambiar la química local; actúa como una señal. Cuando los investigadores expusieron macrófagos a medio condicionado de células de cáncer de páncreas ricas en lactato, los macrófagos cambiaron hacia un estado tipo M2, más propicio para el tumor. Produjeron más factores antiinflamatorios y menos moléculas relacionadas con el ataque y la eliminación de células cancerosas. En ratones, los tumores con niveles altos de RASSF1C contenían más de estos macrófagos pro‑tumorales, un efecto que pudo mitigarse bloqueando la producción de lactato. Pruebas adicionales mostraron que el lactato también reprogramó el manejo de las grasas y el colesterol por parte de los macrófagos, aumentando la acumulación lipídica de maneras compatibles con un nicho más favorable para el crecimiento y la diseminación tumoral.
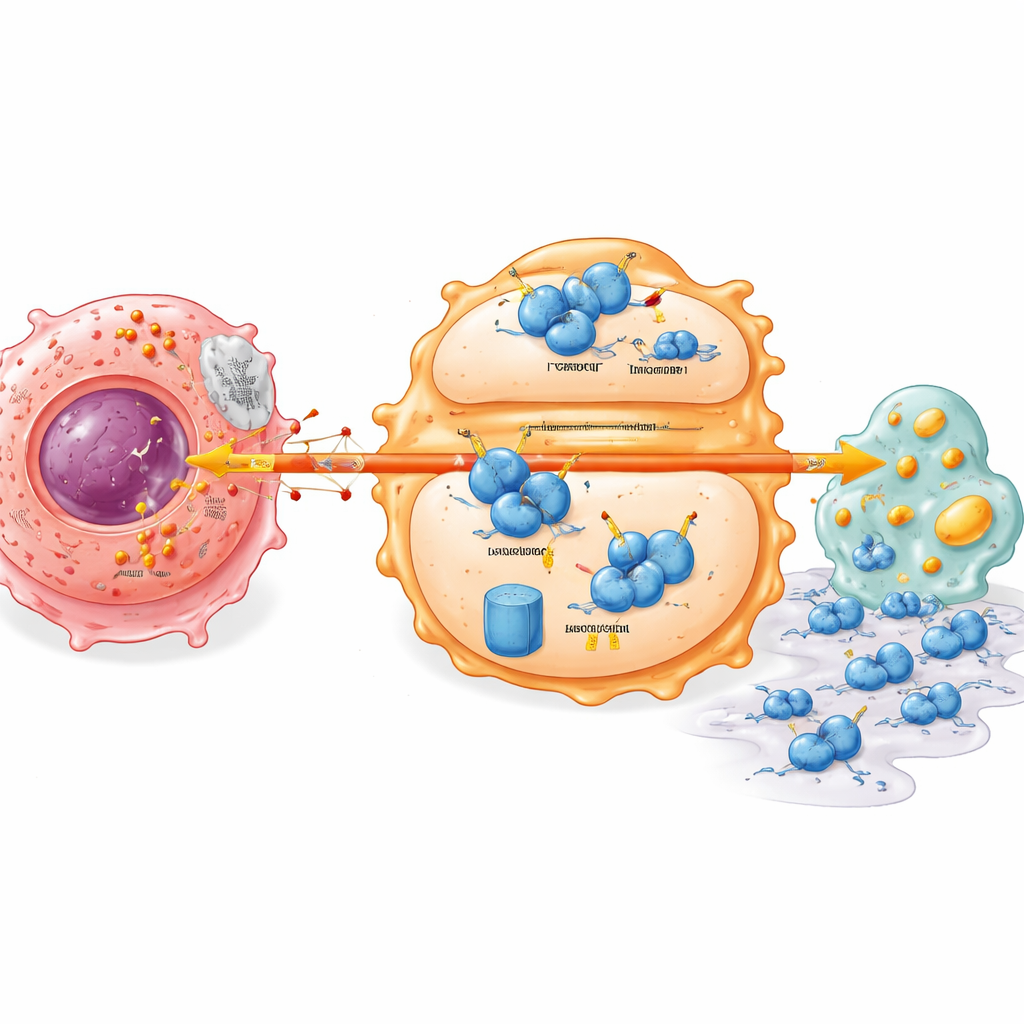
Un interruptor de estabilidad oculto dentro de las células inmunitarias
Ahondando más, el estudio descubrió un interruptor molecular que enlaza el metabolismo tumoral con el comportamiento de las células inmunitarias. Un regulador inmunitario clave llamado IRF7, que normalmente favorece un estado de macrófago más vigilante y preparado para atacar y un manejo lipídico saludable, se encontró en niveles bajos en tumores pancreáticos. El lactato procedente de las células cancerosas provocó que la proteína IRF7 en los macrófagos se volviera inestable y se degradara más rápido. Esto dependió de otra proteína, UFL1, que añade una pequeña etiqueta (UFM1) que protege a IRF7 de ser marcada para la destrucción. El lactato suprimió UFL1 en los macrófagos, inclinando el equilibrio hacia un sistema de etiquetado que envía a IRF7 al triturador proteico de la célula. Sin IRF7 estable, los macrófagos acumulan defectos metabólicos y ayudan con más facilidad a las células tumorales a migrar e invadir los tejidos circundantes.
Qué significa esto para tratamientos futuros
En muestras tumorales de personas con cáncer de páncreas, los investigadores observaron un patrón claro: niveles más altos de RASSF1C y HIF-1α en las células tumorales, y niveles más bajos de UFL1 e IRF7 en el tejido circundante. Estos patrones se asociaron con enfermedad más avanzada y características metastásicas. En conjunto, los hallazgos describen una cadena en la que la baja oxigenación activa RASSF1C y HIF-1α, impulsa la sobreproducción de lactato y, a su vez, desactiva un freno protector UFL1–IRF7 dentro de los macrófagos. Para los lectores no especializados, la conclusión es que el cáncer de páncreas prospera convirtiendo sus propios desechos en armas que desarman a las células inmunitarias cercanas. Interrumpir esta cadena —limitando el lactato, bloqueando la señalización RASSF1C–HIF-1α o estabilizando IRF7— podría abrir nuevas vías para terapias que combinen fármacos metabólicos con enfoques basados en el sistema inmunitario.
Cita: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Palabras clave: cáncer de páncreas, microambiente tumoral, metabolismo tumoral, macrófagos, lactato