Clear Sky Science · de
Die RASSF1C–HIF-1α-Achse treibt den Lipidstoffwechsel von Makrophagen an und fördert Bauchspeicheldrüsenkrebs
Warum diese Krebsstory wichtig ist
Bauchspeicheldrüsenkrebs gehört zu den tödlichsten Krebsarten, unter anderem weil er tief im Körper liegt und oft erst spät entdeckt wird. Seine Aggressivität beruht jedoch nicht nur auf den Tumorzellen selbst. Diese Studie zeigt, wie Sauerstoffmangel in Tumoren sowohl Krebszellen als auch benachbarte Immunzellen so umprogrammiert, dass das Tumorwachstum und die Ausbreitung gefördert werden. Indem die Forschenden diese Abfolge aufdecken, weisen sie auf neue Angriffspunkte hin: Es könnte sinnvoll sein, sowohl den Tumorstoffwechsel als auch das Immunsystem therapiebezogen anzugehen.
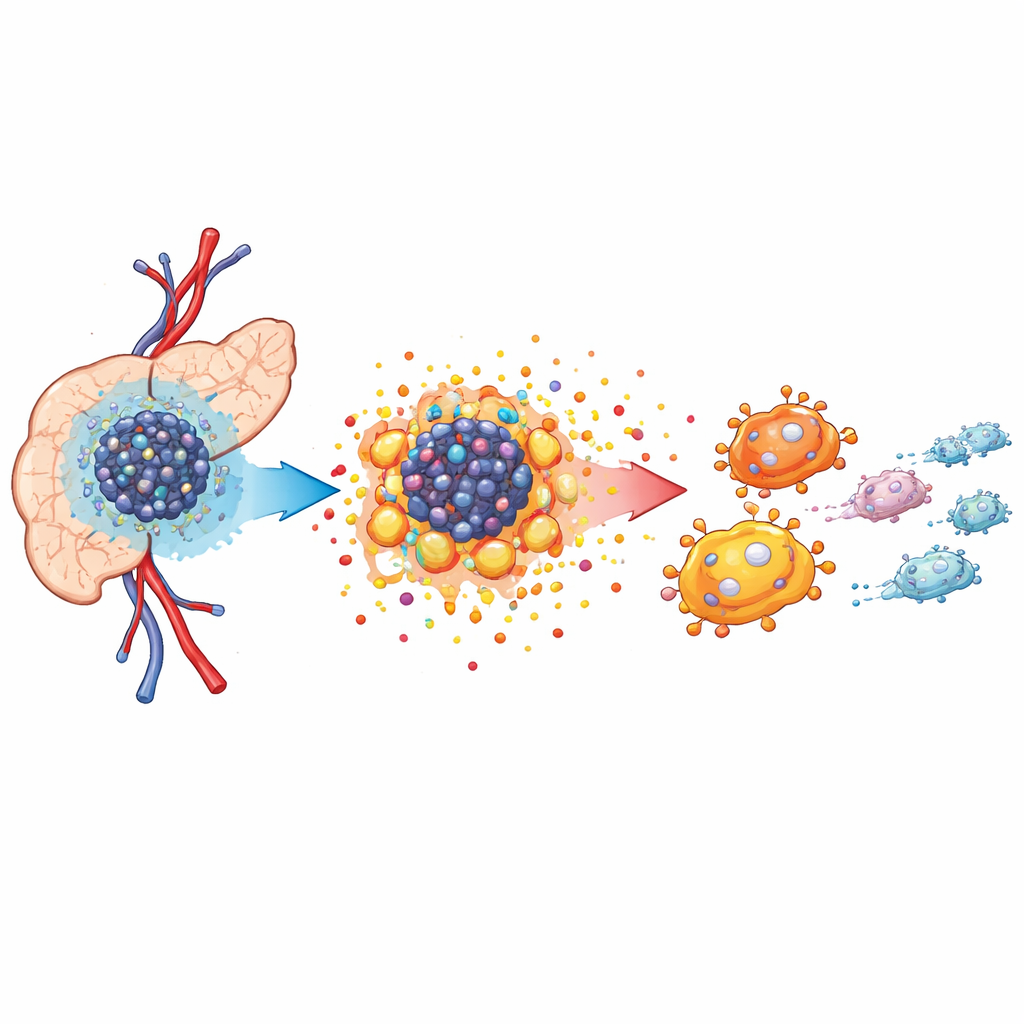
Wenig Sauerstoff und eine hungrige Tumornachbarschaft
Bauchspeicheltumoren wachsen in einer dichten, feindlichen Umgebung, der sogenannten Tumormikroumgebung. Die Blutversorgung ist schlecht, sodass der Sauerstoffgehalt sinkt und die Krebszellen ihre Energiegewinnung umstellen müssen. Mithilfe von Einzelzell-RNA-Sequenzierung und räumlicher Kartierung in Mausmodellen zeigten die Autor:innen, dass das Tumorgewebe voller Krebszellen, tumorfördernder Fibroblasten und spezialisierter Immunzellen namens tumorassoziierte Makrophagen ist. Diese Makrophagen gruppieren sich in der Nähe von Krebszellen und nehmen eher eine wachstumsunterstützende als eine krebsbekämpfende Rolle ein. Die Analyse offenbarte, dass Krebszellen stark auf veränderte Stoffwechselwege angewiesen sind, um schnelles Wachstum zu ermöglichen, und damit die Umgebung des Gewebes grundlegend neu formen.
Krebs mit Zucker und Säure antreiben
Bei Sauerstoffmangel setzen Krebszellen auf einen schnellen, aber ineffizienten Zuckerabbau, oft als Warburg-Effekt bezeichnet. Die Forscher:innen fanden heraus, dass eine Proteinvariante namens RASSF1C, die zuvor mit Krebsverhalten in Verbindung gebracht wurde, bei niedrigen Sauerstoffwerten stark aktiviert wird. Unter der Steuerung eines weiteren Sauerstoff-Sensors, HIF-1α, steigert RASSF1C die Glykolyse, was zu hoher Laktatproduktion und einer Ansäuerung der Umgebung führt. In Zell- und Tierexperimenten reduzierte das Herunterregeln von RASSF1C die Säureproduktion und verlangsamte das Tumorwachstum, während eine Erhöhung den gegenteiligen Effekt hatte. Wichtig ist, dass die Hemmung der Laktatbildung durch ein Medikament den Wachstumsvorteil, den RASSF1C verschafft, abschwächte — ein Hinweis darauf, dass diese Stoffwechselumstellung nicht bloß ein Begleiteffekt ist, sondern aktiv die Krankheitsprogression antreibt.
Wie Tumornebenprodukte Immunzellen umprogrammieren
Das von Tumorzellen freigesetzte Laktat verändert nicht nur die lokale Chemie, sondern wirkt auch als Signal. Wenn die Forschenden Makrophagen mit konditioniertem Medium von laktatreichen Bauchspeicheldrüsenkrebszellen behandelten, verschoben sich die Makrophagen in einen M2-ähnlichen, tumorfördernden Zustand. Sie produzierten mehr entzündungshemmende Faktoren und weniger Moleküle, die mit der Bekämpfung und Beseitigung von Krebszellen verbunden sind. In Mäusen enthielten Tumoren mit hohem RASSF1C-Anteil mehr dieser pro-tumoralen Makrophagen — ein Effekt, der durch die Blockade der Laktatproduktion abgeschwächt werden konnte. Weitere Tests zeigten, dass Laktat auch den Fett- und Cholesterinstoffwechsel der Makrophagen umprogrammiert und so zu einer erhöhten Lipidansammlung führt, was mit einer Umgebung zusammenfällt, die Tumorwachstum und -ausbreitung begünstigt.
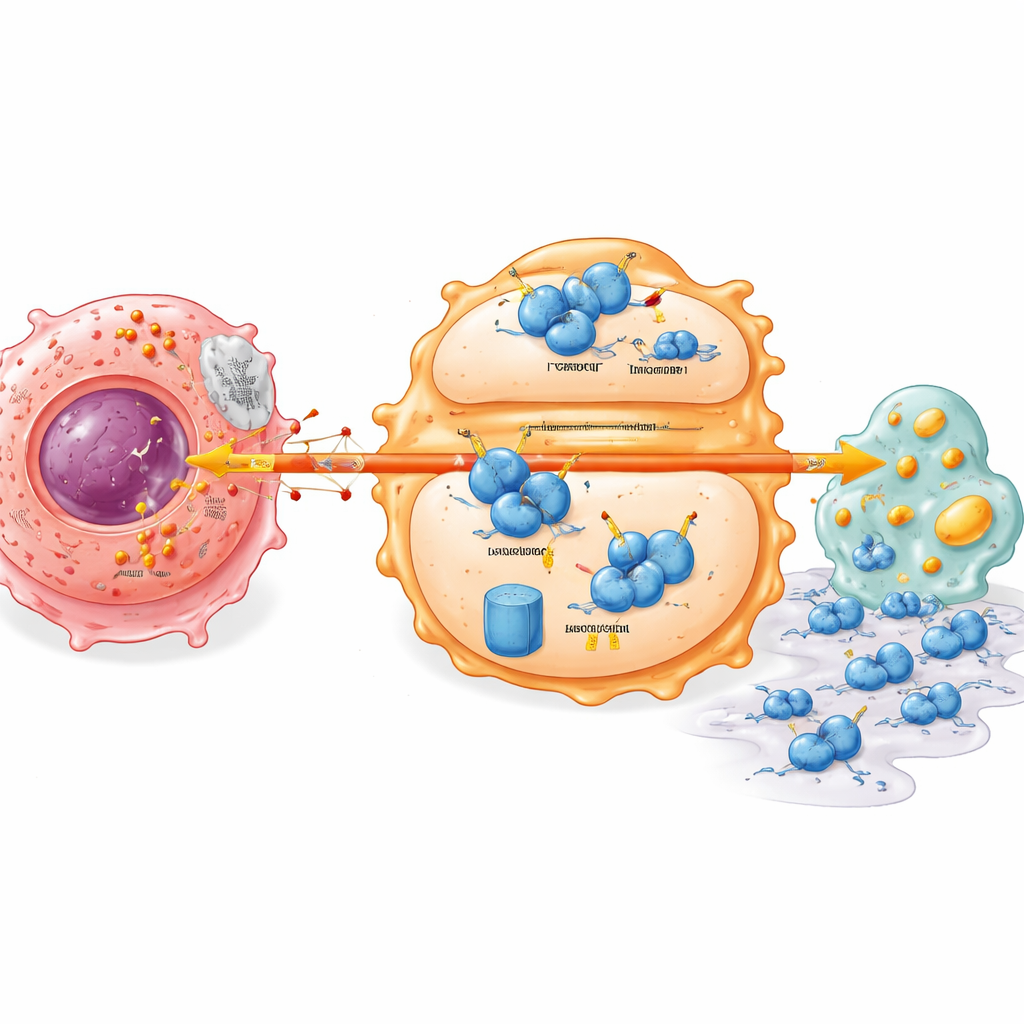
Ein verborgener Stabilitätsschalter in Immunzellen
Tiefergehende Analysen enthüllten einen molekularen Schalter, der den Tumorstoffwechsel mit dem Verhalten der Immunzellen verbindet. Ein wichtiger Immunregulator namens IRF7, der normalerweise einen wachsameren, angreifbereiten Makrophagenstatus und gesunden Lipidstoffwechsel unterstützt, war in Bauchspeicheldrüsentumoren auf niedrigen Niveau zu finden. Laktat aus Krebszellen machte das IRF7-Protein in Makrophagen instabil und beschleunigte seinen Abbau. Dies hing von einem weiteren Protein, UFL1, ab, das eine kleine Schutzmarke (UFM1) anbringt und damit IRF7 davor bewahrt, für den Abbau markiert zu werden. Laktat unterdrückte UFL1 in Makrophagen und verschob so das Gleichgewicht zugunsten eines Systems, das IRF7 an den zellulären Proteinzerleger schickt. Ohne stabiles IRF7 häufen Makrophagen Stoffwechseldefekte an und unterstützen Tumorzellen leichter bei Migration und Gewebeinvasion.
Was das für künftige Therapien bedeutet
In Tumorproben von Menschen mit Bauchspeicheldrüsenkrebs beobachteten die Forschenden ein klares Muster: höhere RASSF1C- und HIF-1α-Werte in Tumorzellen und niedrigere UFL1- und IRF7-Werte im umgebenden Gewebe. Diese Muster korrelierten mit fortgeschrittenerem Krankheitsstadium und metastatischen Merkmalen. Zusammengenommen beschreiben die Befunde eine Kette, in der Sauerstoffmangel RASSF1C und HIF-1α aktiviert, die Laktatüberproduktion antreibt und dadurch die schützende UFL1–IRF7-Bremse in Makrophagen außer Kraft setzt. Für Laien lautet die Kernbotschaft: Bauchspeicheldrüsenkrebs nutzt seine eigenen Abfallprodukte als Waffen, um benachbarte Immunzellen zu entwaffnen. Das Unterbrechen dieser Kette — etwa durch Reduktion von Laktat, Blockade der RASSF1C–HIF-1α-Signalgebung oder Stabilisierung von IRF7 — könnte neue Wege für Therapien eröffnen, die stoffwechselwirksame Mittel mit immunbasierten Ansätzen kombinieren.
Zitation: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Schlüsselwörter: Bauchspeicheldrüsenkrebs, tumormikroumgebung, Tumorstoffwechsel, Makrophagen, Laktat