Clear Sky Science · zh
乳酰化稳定PD-L1以促进肿瘤免疫逃逸与细胞生长
这则癌症研究为何重要
癌症免疫疗法已改变了许多患者的治疗前景,但只有少数患者能获得持久疗效。本研究揭示了肿瘤用来躲避免疫系统的一个隐蔽化学手段——并提示了一种出乎意料的简单途径可以将这一手段反过来用于对抗癌症。通过说明一种常见代谢副产物乳酸如何帮助肿瘤躲避杀伤性T细胞,研究为使现有免疫疗法在更多患者身上更有效指明了新策略。
癌细胞如何与免疫系统“对话”
我们的免疫系统依赖细胞间的分子“握手”来决定何时攻击、何时退让。其中最重要的之一是肿瘤细胞表面的蛋白PD-L1与T细胞上的受体PD-1之间的相互作用。当癌细胞上PD-L1丰富时,它会告诉T细胞后退,从而让肿瘤得以不受控制地生长。阻断PD-1或PD-L1的药物可以解除这一制动,但它们的疗效往往取决于肿瘤展示出多少PD-L1。因此,了解是什么控制了癌细胞上PD-L1的水平,对预测和改善这些治疗的反应至关重要。
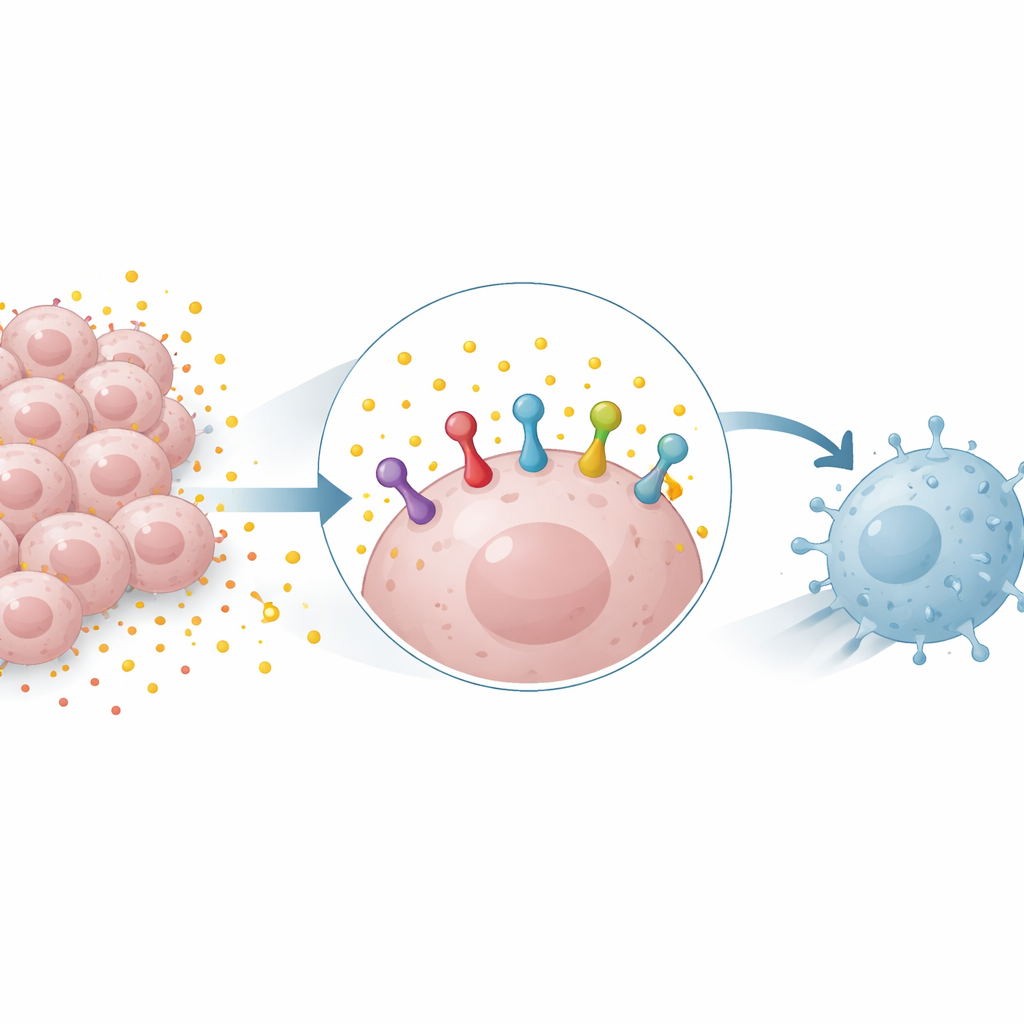
成为武器的“燃料废物”
许多肿瘤严重依赖一种称为糖酵解的糖类代谢途径,这会产生大量乳酸。乳酸长期以来主要被视为代谢废物,但现在被认识为一种活跃的信号分子。研究人员发现,向肺癌和乳腺癌细胞添加乳酸会增加PD-L1蛋白的含量,而阻断糖酵解则会降低其含量。这一效应在人和小鼠细胞中均可观察到,并且即便在乳酸并未提升PD-L1基因活性时也能出现,意味着乳酸是在稳定已有的PD-L1蛋白,而不仅仅是启动其生成。
保护PD-L1的微小化学标记
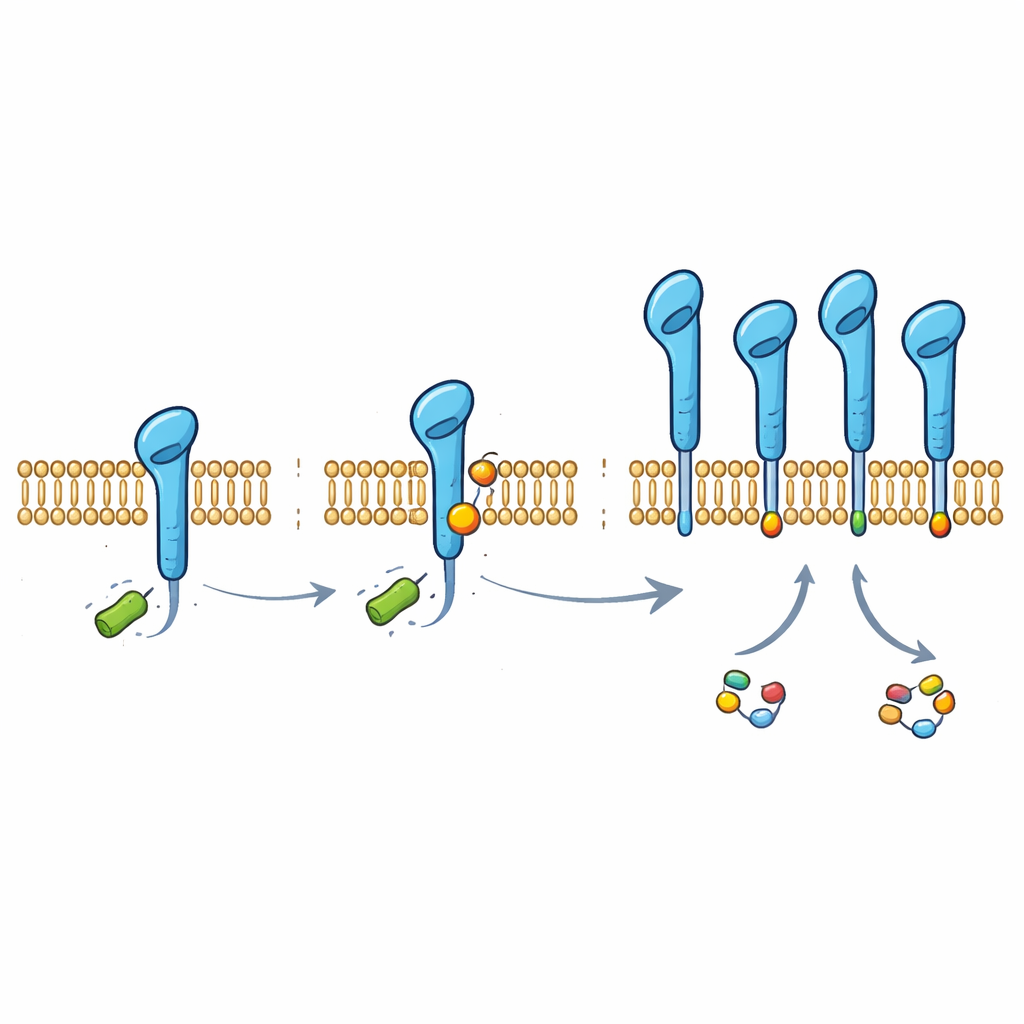
进一步研究表明,PD-L1携带一个源自乳酸的小化学标记,附着在蛋白的一个特定氨基酸上(位于280号位的赖氨酸)。这一称为乳酰化的标记在若干肺癌细胞系和正常气道细胞中的PD-L1上均被检测到。当科学家把该赖氨酸替换为无法被修饰的残基时,PD-L1失去了乳酸依赖的保护,变得更容易被细胞降解。通常,一个名为HUWE1的分子机器通过在附近位点添加多聚泛素链来标记PD-L1以便降解。新的基于乳酸的标记在空间上阻碍了HUWE1的接近,防止了这种“垃圾标签”的附着,从而保护PD-L1免于被拆解。
书写乳酰化标记的酶
为了解这一标记如何被添加,研究人员寻找能够直接使用乳酸作为供体的酶。他们鉴定出丙氨酰-tRNA合成酶1(AARS1),一种通常参与蛋白质合成的常规酶,作为PD-L1乳酰化的关键“书写者”。在试管实验和细胞中,AARS1能将乳酸基团附加到PD-L1的尾部,而相关酶AARS2则不能。过表达AARS1会增加PD-L1上的乳酸标记,减少HUWE1的结合与泛素标注,从而稳定该免疫检查点蛋白。沉默AARS1则产生相反效果,并抹去乳酸的稳定作用,表明该酶是连接肿瘤代谢与PD-L1保护的关键环节。
从细胞伎俩到治疗机会
研究人员在小鼠中检验了这种化学修饰的生物学后果。工程化携带不可乳酰化版本PD-L1的肿瘤细胞在培养中更容易被CD8+ T细胞杀死,并在动物体内形成更小的肿瘤,伴随更多这些杀伤细胞的浸润。作者随后研究了乳酸的医学用盐——乳酸钠(NaLa),该物质已在静脉输液中广泛使用。在小鼠肺癌模型中,单独使用NaLa并未加速肿瘤生长,但与抗PD-L1疗法合用时显著增强了治疗对肿瘤的控制能力,并增加了肿瘤内CD8+ T细胞的数量。在患者肺癌样本中,携带乳酸标记的PD-L1水平更高与疾病更晚期和更差的生存率相关,提示该修饰可能作为侵袭性肿瘤以及免疫治疗反应的生物标志物。
对患者与未来疗法的意义
综上所述,研究揭示了一条直接的事件链:肿瘤代谢产生乳酸;乳酸被用来在PD-L1的单一位点打上标记;该标记阻止蛋白被降解,帮助肿瘤使T细胞沉默。然而,这种稳定化同样可能使肿瘤对靶向PD-L1的药物更为可见。就实际而言,这项工作提出了乳酰化及驱动它的AARS1酶,作为调整PD-L1保护强度的新杠杆。通过在患者肿瘤中检测这一标记并设计能对其进行精细调控的治疗,临床医生有望将来更好地预测谁会从免疫疗法中受益,并将检查点抑制剂与代谢干预相结合,把癌症自身的“燃料废物”变为治疗弱点。
引用: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
关键词: PD-L1, 乳酸, 肿瘤免疫, 翻译后修饰, 非小细胞肺癌