Clear Sky Science · de
Lactylierung stabilisiert PD-L1 und fördert Tumor-Immunflucht und Zellwachstum
Warum diese Krebsstudie wichtig ist
Die Krebsimmuntherapie hat die Behandlung vieler Patientinnen und Patienten verändert, doch nur eine Minderheit profitiert dauerhaft. Diese Studie enthüllt einen verborgenen chemischen Trick, den Tumoren einsetzen, um sich vor dem Immunsystem zu schützen — und zeigt einen überraschend einfachen Ansatz, um diesen Trick gegen den Krebs zu verwenden. Indem sie darlegt, wie ein häufiger Stoffwechselnebenprodukt, Lactat, Tumoren dabei hilft, sich vor Killer-T-Zellen zu verbergen, weist die Arbeit auf neue Strategien, bestehende Immuntherapien wirksamer zu machen und für mehr Menschen zugänglich zu machen.
Wie Krebszellen mit dem Immunsystem kommunizieren
Unser Immunsystem beruht auf molekularen „Handschlägen“ zwischen Zellen, um zu entscheiden, wann angegriffen und wann zurückgehalten werden soll. Einer der wichtigsten ist die Interaktion zwischen einem Protein auf Tumorzellen namens PD-L1 und seinem Partner PD-1 auf T‑Zellen. Wenn PD-L1 auf Krebszellen reichlich vorhanden ist, signalisiert es den T‑Zellen, sich zurückzuziehen, sodass der Tumor ungehindert wachsen kann. Wirkstoffe, die PD-1 oder PD-L1 blockieren, können diese Bremse lösen, ihr Erfolg hängt jedoch oft davon ab, wie viel PD-L1 der Tumor zeigt. Zu verstehen, was die PD-L1-Spiegel auf Krebszellen steuert, ist daher zentral, um das Ansprechen auf diese Therapien vorherzusagen und zu verbessern.
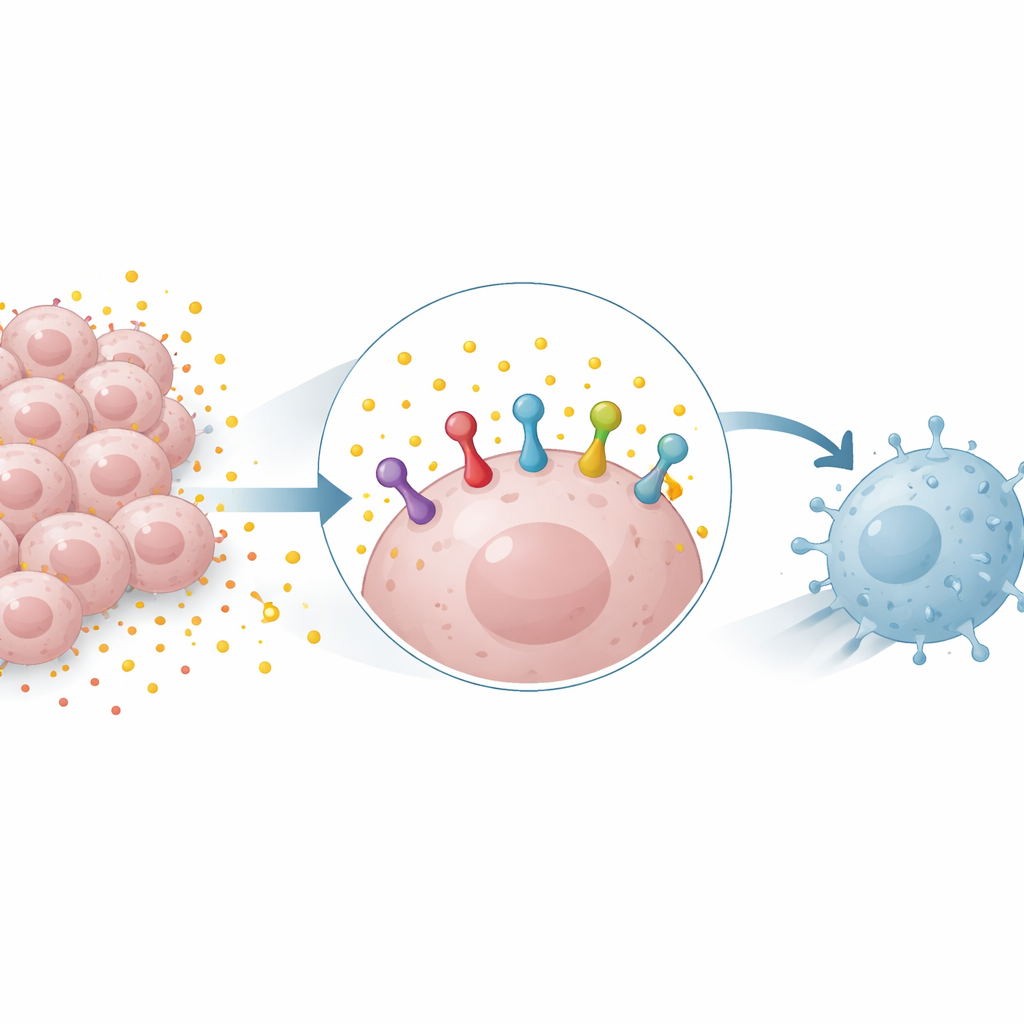
Energiemüll, der zur Waffe wird
Viele Tumoren verlassen sich stark auf den zuckerabbauenden Prozess der Glykolyse, der große Mengen Lactat produziert. Lange Zeit vor allem als Stoffwechselabfall betrachtet, wird Lactat inzwischen als aktives Signalmolekül anerkannt. Die Forschenden fanden heraus, dass das Hinzufügen von Lactat zu Lungen- und Brustkrebszellen die Menge des PD-L1‑Proteins erhöhte, während die Blockade der Glykolyse sie verringerte. Dieser Effekt zeigte sich sowohl in menschlichen als auch in Maus‑Zellen und konnte auftreten, selbst wenn Lactat die Aktivität des PD-L1‑Gens nicht steigerte, was darauf hindeutet, dass Lactat bestehendes PD-L1‑Protein stabilisiert, statt nur seine Produktion anzuschalten.
Ein winziges chemisches Etikett, das PD-L1 schützt
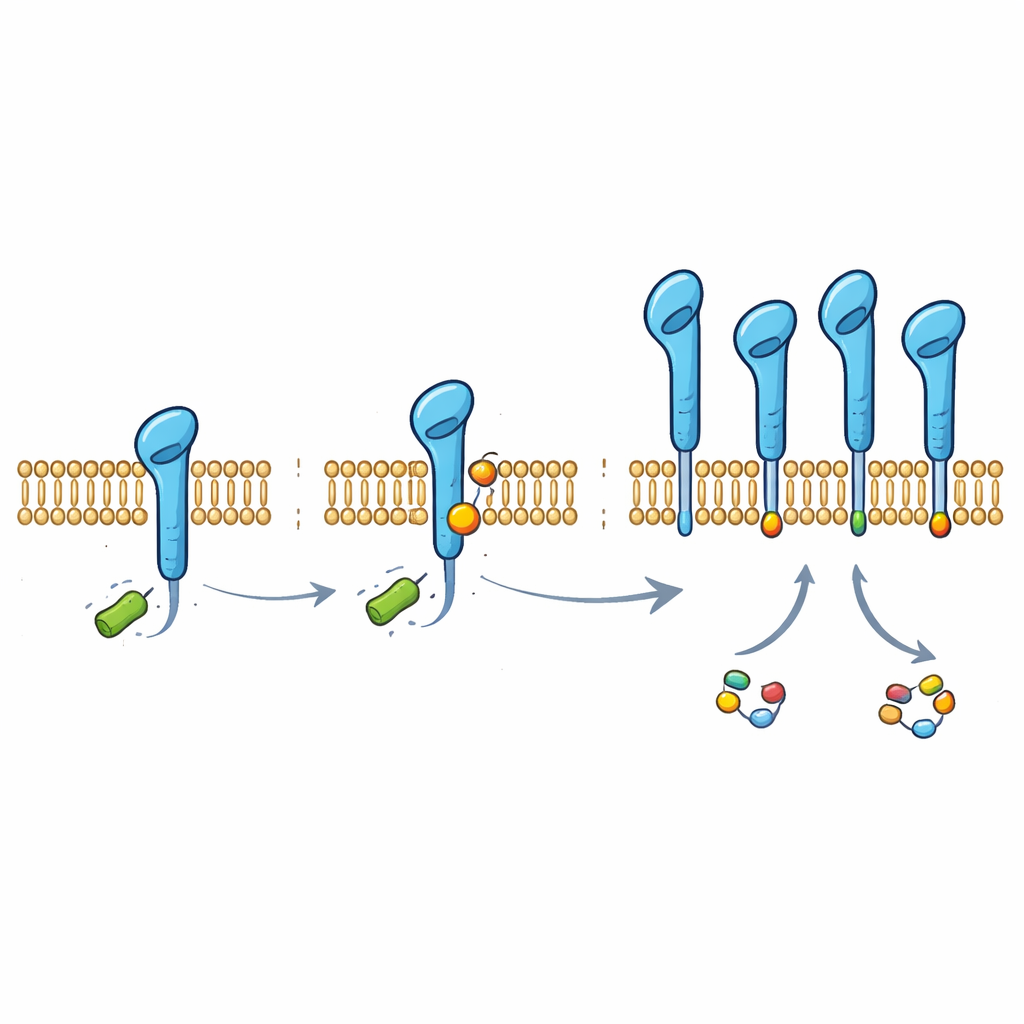
Bei tiefergehender Untersuchung entdeckte das Team, dass PD-L1 eine kleine chemische Gruppe trägt, die von Lactat abgeleitet ist und an eine bestimmte Aminosäure des Proteins gebunden ist (ein Lysin an Position 280). Diese Modifikation, genannt Lactylierung, wurde auf PD-L1 in mehreren Lungenkrebszelllinien und in normalen Atemwegsepithelzellen nachgewiesen. Wenn die Wissenschaftler dieses einzelne Lysin so veränderten, dass es nicht mehr modifiziert werden konnte, verlor PD-L1 den größten Teil seines lactatabhängigen Schutzes und wurde für die Zelle leichter zu zerstören. Normalerweise markiert die molekulare Maschine HUWE1 PD-L1 zur Entsorgung, indem sie in der Nähe Ketten des kleinen Moleküls Ubiquitin anbringt. Das neue lactatbasierte Etikett verhindert physisch den Zugang von HUWE1, sodass dieses „Müllschild“ nicht angeheftet wird und PD-L1 vor dem Abbau geschützt bleibt.
Das Enzym, das das Lactat-Etikett schreibt
Um zu verstehen, wie dieses Etikett angebracht wird, suchten die Forschenden nach Enzymen, die Lactat direkt als Donor verwenden könnten. Sie identifizierten die Alanyl-tRNA-Synthetase 1 (AARS1), ein normalerweise routinemäßiges Protein der Proteinbiosynthese, als den entscheidenden „Schreiber“ der PD-L1‑Lactylierung. In Reagenzglas-Experimenten und in Zellen konnte AARS1 eine Lactatgruppe an das C-Terminus von PD-L1 anfügen, während ein verwandtes Enzym, AARS2, dies nicht konnte. Eine Überexpression von AARS1 erhöhte das Lactat-Etikett auf PD-L1, reduzierte die Bindung von HUWE1 und die Ubiquitinierung und stabilisierte das Checkpoint‑Protein. Das Stilllegen von AARS1 hatte den gegenteiligen Effekt und machte die stabilisierende Wirkung von Lactat rückgängig, was darauf hinweist, dass dieses Enzym die entscheidende Verbindung zwischen Tumorstoffwechsel und PD-L1‑Schutz darstellt.
Von zellulären Tricks zu therapeutischen Chancen
Die biologischen Folgen dieser Chemie wurden in Mäusen untersucht. Tumorzellen, die so konstruiert wurden, dass sie eine nicht‑lactylierbare Version von PD-L1 trugen, wurden in Kultur leichter von CD8+‑T‑Zellen getötet und bildeten in Tieren deutlich kleinere Tumoren mit stärkerer Infiltration dieser Killerzellen. Die Autorinnen und Autoren untersuchten außerdem Natriumlactat (NaLa), ein medizinisch verwendetes Lactatsalz, das bereits in intravenösen Lösungen verbreitet ist. In Maus-Lungenkrebsmodellen beschleunigte NaLa allein nicht das Tumorwachstum, steigerte aber in Kombination mit einer anti‑PD-L1‑Therapie deutlich die Wirksamkeit der Behandlung und erhöhte die Präsenz von CD8+‑T‑Zellen in den Tumoren. In Patientinnen‑ und Patientenproben von Lungenkrebs war ein höherer Anteil von PD-L1 mit dem Lactat‑Etikett mit fortgeschrittenerer Erkrankung und schlechterem Überleben assoziiert, was darauf hindeutet, dass diese Modifikation als Biomarker für aggressive Tumoren und möglicherweise für das Ansprechen auf Immuntherapie dienen könnte.
Was das für Patienten und zukünftige Therapien bedeutet
In der Summe zeigen die Ergebnisse eine direkte Kette von Ereignissen: Der Tumorstoffwechsel produziert Lactat; Lactat wird verwendet, um PD-L1 an einer einzigen Stelle zu markieren; dieses Etikett blockiert den Abbau des Proteins und hilft Tumoren, T‑Zellen stummzuschalten. Doch genau diese Stabilisierung könnte Tumoren zugleich sichtbarer für PD-L1‑zielgerichtete Medikamente machen. Praktisch schlägt diese Arbeit Lactylierung — und das AARS1‑Enzym, das sie vermittelt — als neue Hebel vor, um die Schutzwirkung von PD-L1 zu regulieren. Indem man dieses Etikett in Tumorproben misst und Therapien entwickelt, die es feinjustieren, könnten Ärztinnen und Ärzte künftig besser vorhersagen, wer von einer Immuntherapie profitiert, und Checkpoint‑Blocker mit Stoffwechselinterventionen kombinieren, um den eigenen Energiemüll des Krebses in eine therapeutische Schwäche zu verwandeln.
Zitation: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Schlüsselwörter: PD-L1, Lactat, Tumorimmunität, posttranslationale Modifikation, nicht-kleinzelliges Lungenkarzinom