Clear Sky Science · tr
Laktillanma, tümörün bağışıklık kaçışını ve hücre büyümesini desteklemek için PD-L1’i stabilize eder
Bu kanser öyküsü neden önemli
Kanser immünoterapisi birçok hasta için tedaviyi dönüştürdü, ancak yalnızca azınlık uzun süreli fayda görüyor. Bu çalışma, tümörlerin bağışıklık sisteminden kendilerini korumak için kullandığı gizli bir kimyasal numarayı ortaya çıkarıyor — ve bu numarayı kanserin aleyhine çevirebilecek şaşırtıcı derecede basit bir yol öneriyor. Yaygın bir metabolik yan ürün olan laktatın, tümörlerin öldürücü T hücrelerinden nasıl saklanmasına yardımcı olduğunu göstererek, çalışma mevcut immün terapilerin daha fazla kişide ve daha etkili olmasını sağlayacak yeni stratejilere işaret ediyor.
Kanser hücreleri bağışıklık sistemiyle nasıl konuşur
Bağışıklık sistemimiz, saldırıp saldırmama kararını vermek için hücreler arasında moleküler “tokalaşmalara” dayanır. Bunların en önemlilerinden biri, tümör hücrelerindeki PD-L1 adlı bir protein ile T hücrelerindeki ortağı PD-1 arasındaki etkileşimdir. Kanser hücrelerinde PD-L1 bol olduğunda, T hücrelerine geri çekilmelerini söyler ve tümörün kontrolsüz büyümesine izin verir. PD-1 veya PD-L1’i hedef alan ilaçlar bu freni serbest bırakabilir, ancak başarısı genellikle tümörün ne kadar PD-L1 gösterdiğine bağlıdır. Bu nedenle kanser hücrelerindeki PD-L1 düzeylerini neyin kontrol ettiğini anlamak, bu tedavilere yanıtı tahmin etmek ve iyileştirmek açısından merkezi önemdedir.
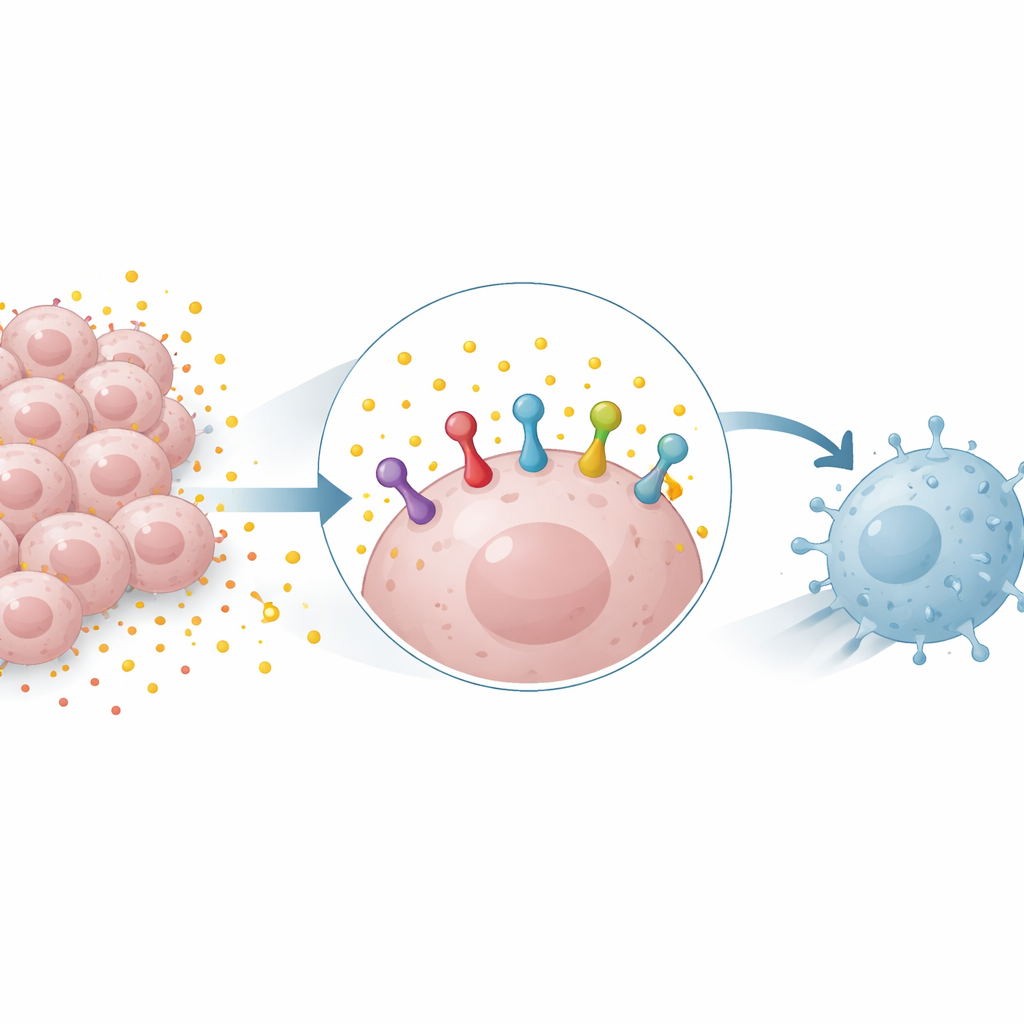
Silaha dönüşen yakıt atığı
Birçok tümör, bol miktarda laktat üreten glikoliz adı verilen bir şeker yakma sürecine yoğun şekilde güvenir. Uzun süre çoğunlukla metabolik atık olarak görülen laktat şimdi aktif bir sinyal molekülü olarak tanınıyor. Araştırmacılar, laktat eklemenin akciğer ve meme kanseri hücrelerinde PD-L1 protein miktarını artırdığını, glikolizi engellemenin ise azalttığını buldu. Bu etki hem insan hem fare hücrelerinde görüldü ve laktat PD-L1 gen aktivitesini yükseltmediğinde bile ortaya çıkabiliyordu; bu da laktatın yalnızca üretimi artırmak yerine mevcut PD-L1 proteinini stabilize ettiğini düşündürüyor.
PD-L1’i koruyan küçük bir kimyasal etiket
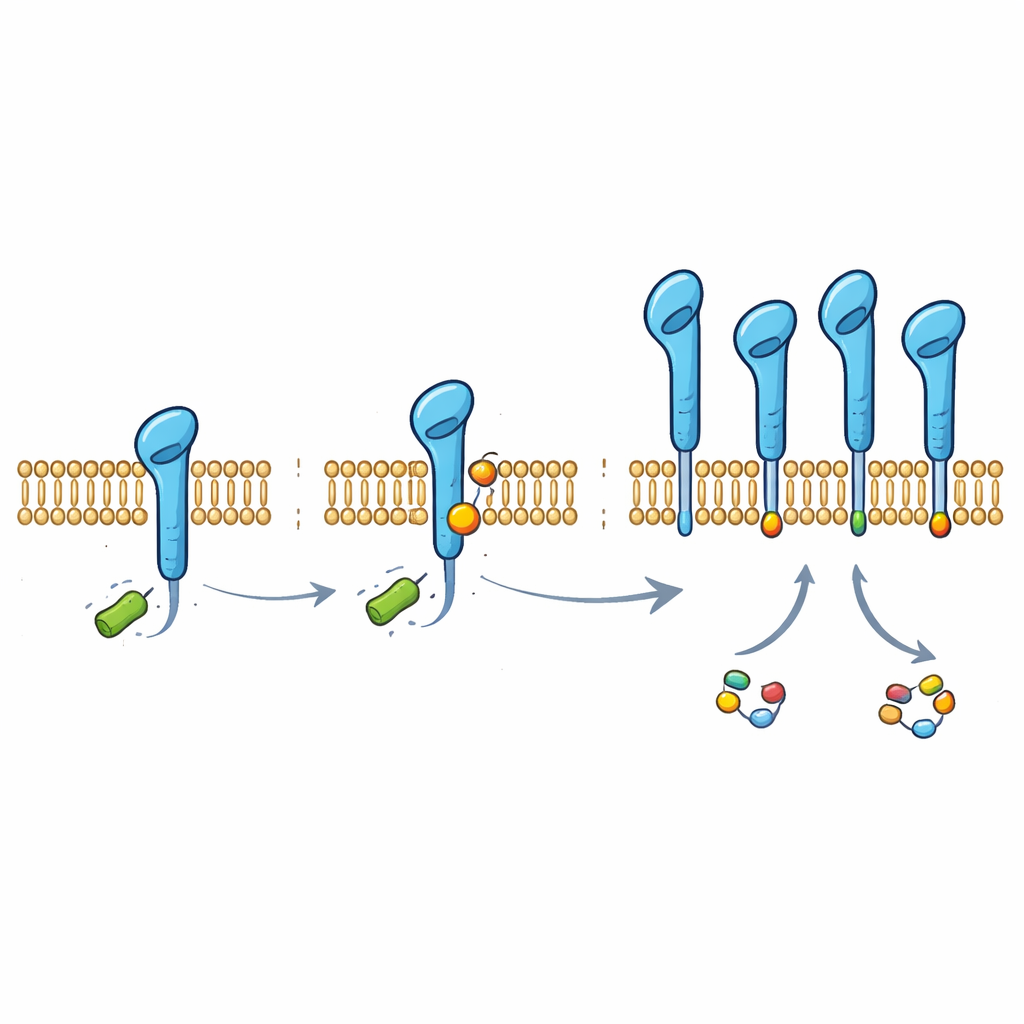
Daha derine indiklerinde, ekip PD-L1’in protein yapısının belirli bir amino asidine (280. pozisyondaki bir lizin) bağlı, laktattan türetilmiş küçük bir kimyasal etikete sahip olduğunu keşfetti. Laktillanma adı verilen bu etiket, birkaç akciğer kanseri hücre hattında ve normal hava yolu hücrelerinde PD-L1 üzerinde bulundu. Bilim insanları o tek lizini değiştirip artık modifiye edilemez hale getirdiklerinde, PD-L1 laktata bağlı korumasının çoğunu kaybetti ve hücrenin onu yok etmesi kolaylaştı. Normalde HUWE1 adlı moleküler bir makine, PD-L1’i çevredeki bir pozisyona ubiquitin zincirleri ekleyerek imha için işaretler. Yeni laktat tabanlı etiket, HUWE1’in erişimini fiziksel olarak engelleyerek bu “çöp etiketi”nin takılmasını önlüyor ve böylece PD-L1’in parçalanmasına karşı koruma sağlıyor.
Laktat etiketini yazan enzim
Bu etiketin nasıl eklendiğini anlamak için araştırmacılar laktatı doğrudan bir verici olarak kullanabilecek enzimleri aradılar. Alanyil-tRNA sentetaz 1 (AARS1) adlı, normalde rutin protein sentezi yapan bir enzimi PD-L1 laktillanmasının ana “yazıcısı” olarak tanımladılar. Deney tüplerinde ve hücrelerde AARS1, PD-L1 kuyruk kısmına bir laktat grubu ekleyebilirken, ilişkili bir enzim olan AARS2 bunu yapamıyordu. AARS1’in aşırı üretimi PD-L1 üzerindeki laktat etiketini artırdı, HUWE1 bağlanmasını ve ubiquitin etiketlenmesini azalttı ve kontrol noktası proteinini stabilize etti. AARS1 susturulduğunda ters etki görüldü ve laktatın stabilize edici etkisi kayboldu; bu da bu enzimin tümör metabolizması ile PD-L1 koruması arasındaki kritik bağlantı olduğunu gösteriyor.
Hücre numaralarından tedavi fırsatlarına
Bu kimyanın biyolojik sonuçları farelerde test edildi. Laktillanamaz bir PD-L1 versiyonunu taşıyacak şekilde tasarlanmış tümör hücreleri kültürde CD8+ T hücreleri tarafından daha kolay öldürüldü ve hayvanlarda çok daha küçük tümörler oluşturarak bu öldürücü hücrelerin doku içine daha fazla girmesine yol açtı. Yazarlar ardından, damariçi solüsyonlarda zaten yaygın olarak kullanılan laktatın tıbbi bir tuzu olan sodyum laktat (NaLa)’ı incelediler. Fare akciğer kanseri modellerinde NaLa tek başına tümör büyümesini hızlandırmadı, ancak anti-PD-L1 terapisiyle birlikte uygulandığında tedavinin tümörleri kontrol etme yeteneğini anlamlı şekilde artırdı ve içlerindeki CD8+ T hücrelerinin varlığını yükseltti. Hasta akciğer kanseri örneklerinde, laktat etiketi taşıyan PD-L1 seviyelerinin yüksek olması daha ileri hastalık ve daha kötü sağkalımla ilişkiliydi; bu, bu modifikasyonun agresif tümörler ve olası olarak immünoterapiye yanıt için bir biyobelirteç olarak hizmet edebileceğini düşündürüyor.
Bu hastalar ve gelecekteki tedaviler için ne anlama geliyor
Bir araya getirildiğinde bulgular doğrudan bir olay zincirini ortaya koyuyor: tümör metabolizması laktat üretir; laktat PD-L1’i tek bir noktada etiketlemek için kullanılır; bu etiket proteinin yok edilmesini engeller ve tümörlerin T hücrelerini susturmasına yardımcı olur. Ancak aynı stabilizasyon, tümörleri PD-L1’i hedefleyen ilaçlara karşı daha görünür hâle getirebilir. Pratik açıdan bu çalışma, laktillanmayı ve bunu tetikleyen AARS1 enzimini, PD-L1’in kanser hücrelerini ne kadar güçlü koruduğunu ayarlamak için yeni bir kaldıraç olarak öne sürüyor. Hastaların tümörlerinde bu etiketi ölçerek ve onu ince ayarlayacak tedaviler tasarlayarak, klinisyenler bir gün immünoterapiden kimlerin fayda göreceğini daha iyi tahmin edebilir ve kontrol noktası blokerlerini metabolik müdahalelerle eşleştirerek kanserin kendi yakıt atığını bir terapötik zayıflığa çevirebilirler.
Atıf: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Anahtar kelimeler: PD-L1, laktat, tümör bağışıklığı, post-translasyonel modifikasyon, küçük hücre dışı akciğer kanseri