Clear Sky Science · pl
Laktylacja stabilizuje PD-L1, wspierając ucieczkę nowotworu przed układem odpornościowym i wzrost komórek
Dlaczego ta historia o nowotworach ma znaczenie
Immunoterapia nowotworów zrewolucjonizowała leczenie wielu pacjentów, lecz tylko nieliczni odnoszą trwałe korzyści. W tym badaniu odkryto ukryty chemiczny trik, którego nowotwory używają, by chronić się przed układem odpornościowym — i zasugerowano zaskakująco prosty sposób, by obrócić ten trik przeciwko rakowi. Pokazując, w jaki sposób powszechny metabolit — mleczan — pomaga guzom ukryć się przed komórkami zabójczymi T, praca wskazuje nowe strategie, które mogą uczynić istniejące terapie immunologiczne skuteczniejszymi i dostępnymi dla większej liczby pacjentów.
Jak komórki nowotworowe „rozmawiają” z układem odpornościowym
Nasz układ odpornościowy polega na molekularnych „uściskach dłoni” między komórkami, by decydować, kiedy atakować, a kiedy się wstrzymać. Jednym z najważniejszych jest interakcja między białkiem na komórkach nowotworowych zwanym PD-L1 a jego partnerem PD-1 na komórkach T. Gdy PD-L1 jest obfite na komórkach nowotworowych, sygnalizuje komórkom T, by się wycofały, co pozwala guzowi rosnąć bez kontroli. Leki blokujące PD-1 lub PD-L1 mogą zdjąć ten hamulec, lecz ich powodzenie często zależy od tego, ile PD-L1 wyświetla guz. Zrozumienie, co reguluje poziomy PD-L1 na komórkach nowotworowych, jest więc kluczowe dla przewidywania i poprawy odpowiedzi na te terapie.
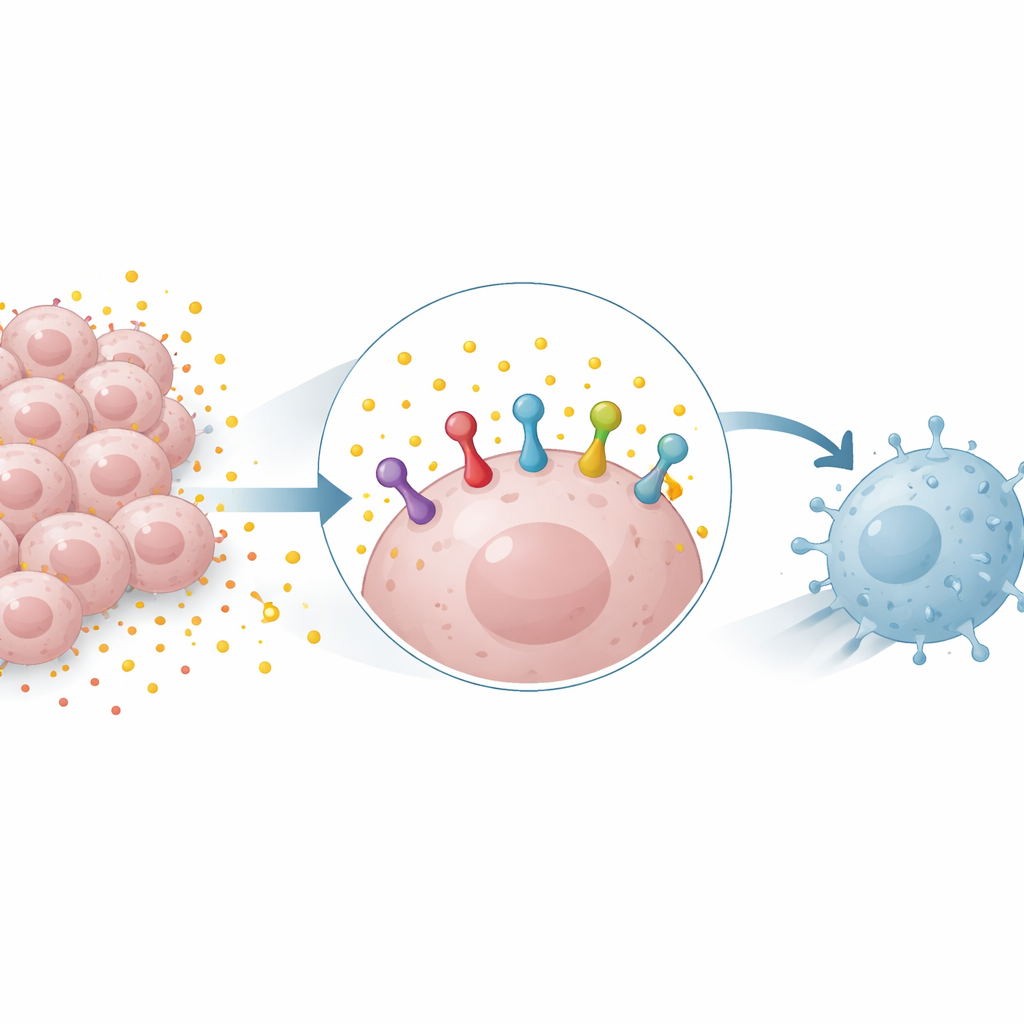
Paliwo jako broń — odpady metaboliczne, które stają się sygnałem
Wiele guzów silnie polega na procesie spalania cukru zwanym glikolizą, który produkuje duże ilości mleczanu. Długo uważany głównie za odpad metaboliczny, mleczan jest obecnie rozpoznawany jako aktywny molekularny sygnał. Badacze stwierdzili, że dodanie mleczanu do komórek raka płuca i raka piersi zwiększało ilość białka PD-L1, podczas gdy blokada glikolizy ją obniżała. Efekt zaobserwowano zarówno w komórkach ludzkich, jak i mysich i mógł wystąpić nawet wtedy, gdy mleczan nie zwiększał aktywności genu PD-L1, co sugeruje, że mleczan stabilizuje istniejące białko PD-L1, a nie tylko pobudza jego syntezę.
Maleńka chemiczna etykietka, która chroni PD-L1
Pogłębiając badania, zespół odkrył, że PD-L1 nosi małą chemiczną etykietę pochodzącą od mleczanu, przyłączoną do jednego konkretnego resztkowego aminokwasu białka (lizyna na pozycji 280). Ta etykietka, nazwana laktylacją, została wykryta na PD-L1 w kilku liniach komórek raka płuca oraz w komórkach prawidłowego nabłonka dróg oddechowych. Gdy naukowcy zmienili tę pojedynczą lizynę tak, aby nie mogła być zmodyfikowana, PD-L1 straciło większość ochrony zależnej od mleczanu i stało się łatwiejsze do zniszczenia przez komórkę. Zwykle molekularna maszyna o nazwie HUWE1 oznacza PD-L1 do usunięcia, przyłączając łańcuchy innej małej cząsteczki — ubikwityny — w pobliżu tej pozycji. Nowa mleczanowa etykietka fizycznie utrudnia dostęp HUWE1, zapobiegając przyłączeniu tej "etykiety na śmieci" i tym samym chroniąc PD-L1 przed rozkładem.
Enzym, który „pisze” laktylową etykietę
Aby zrozumieć, jak ta etykietka jest dodawana, badacze poszukiwali enzymów, które mogłyby użyć mleczanu bezpośrednio jako dawcy. Zidentyfikowali alanyl-tRNA syntetazę 1 (AARS1), rutynowy enzym syntezy białek, jako kluczowego „pisarza” laktylacji PD-L1. W eksperymentach in vitro i w komórkach AARS1 potrafiła przyłączyć grupę mleczanową do ogona PD-L1, podczas gdy pokrewny enzym AARS2 tego nie robił. Nadprodukcja AARS1 zwiększała ilość laktylowej etykiety na PD-L1, zmniejszała wiązanie HUWE1 i ubikwitynację oraz stabilizowała białko punktu kontrolnego. Wyciszenie AARS1 dawało efekt odwrotny i usuwało stabilizujący wpływ mleczanu, co wskazuje, że ten enzym jest kluczowym ogniwem łączącym metabolizm guza z ochroną PD-L1.
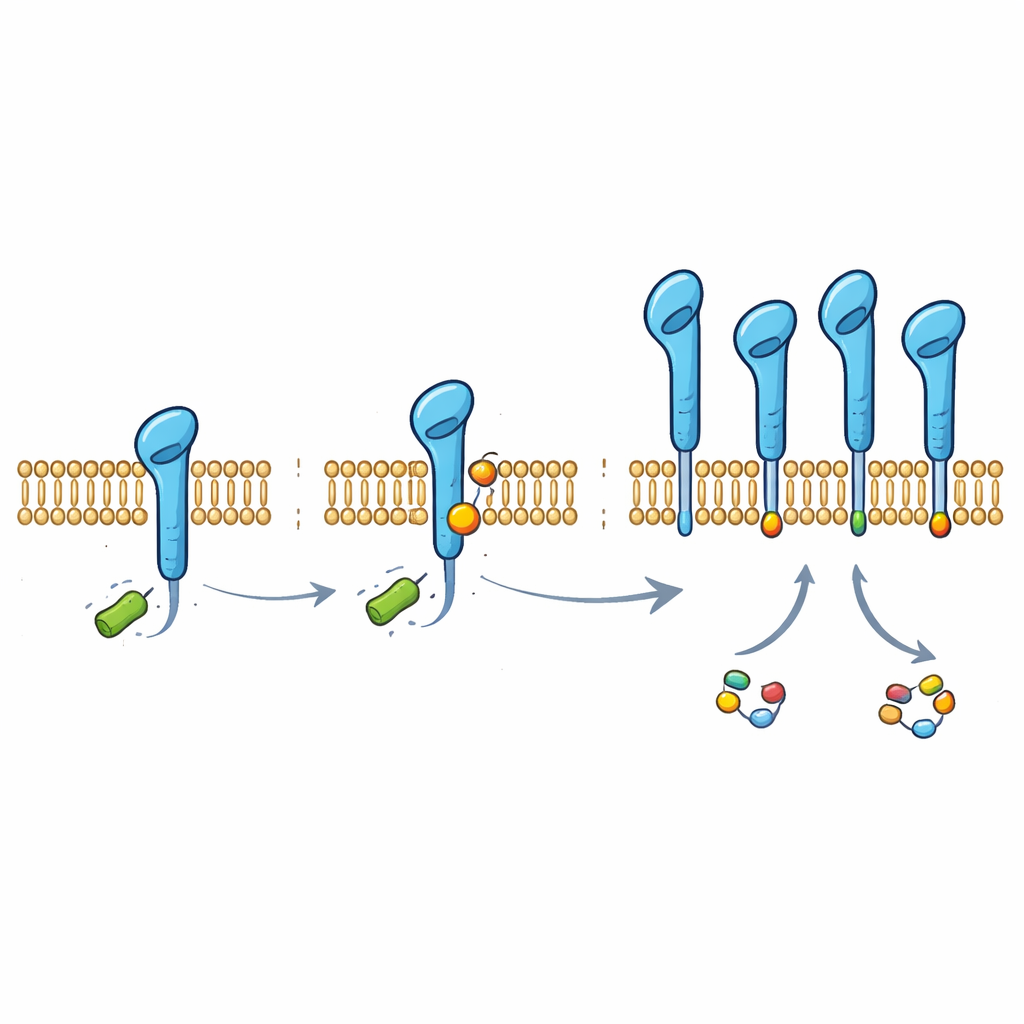
Od sztuczek komórek do możliwości terapeutycznych
Konsekwencje biologiczne tej chemii badano u myszy. Komórki nowotworowe zaprojektowane tak, by mieć wersję PD-L1, której nie można było laktylować, były łatwiej zabijane przez komórki CD8+ T w hodowli i tworzyły znacznie mniejsze guzy u zwierząt, z większym napływem tych komórek zabójców. Autorzy zbadali też mleczan sodu (NaLa), medycznie stosowaną sol mleczanu już powszechną w płynach dożylnych. W modelach raka płuca u myszy sam NaLa nie przyspieszał wzrostu guza, ale w połączeniu z terapią przeciw PD-L1 znacząco zwiększał zdolność leczenia do kontroli guzów i podnosił liczbę CD8+ T w ich wnętrzu. W próbkach tkanek pacjentów z rakiem płuca wyższe poziomy PD-L1 niosącego laktylową etykietę wiązały się z bardziej zaawansowaną chorobą i gorszym przeżyciem, co sugeruje, że ta modyfikacja może służyć jako biomarker agresywnych guzów i ewentualnie odpowiedzi na immunoterapię.
Co to oznacza dla pacjentów i przyszłych terapii
W sumie wyniki ujawniają bezpośredni łańcuch zdarzeń: metabolizm guza wytwarza mleczan; mleczan jest używany do oznaczenia PD-L1 w jednym miejscu; ta etykietka blokuje niszczenie białka i pomaga guzom uciszać komórki T. Jednocześnie taka stabilizacja może sprawiać, że guzy stają się bardziej widoczne dla leków celujących w PD-L1. W praktycznym wymiarze praca proponuje laktylację — i enzym AARS1, który ją przeprowadza — jako nowe dźwignie do regulacji siły osłony PD-L1. Pomiar tej etykietki w guzach pacjentów oraz projektowanie terapii modulujących ją może w przyszłości pozwolić klinicystom lepiej przewidywać, kto skorzysta z immunoterapii, oraz łączyć blokerów punktów kontrolnych z interwencjami metabolicznymi, by przemienić paliwowy odpad nowotworu w terapeutyczną słabość.
Cytowanie: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Słowa kluczowe: PD-L1, mleczan, odporność przeciw nowotworom, modyfikacja potranslacyjna, pierwotny rak płuc nieoszczędzający drobnych komórek