Clear Sky Science · ja
ラクトイル化はPD-L1を安定化させ腫瘍の免疫回避と細胞増殖を促進する
このがん研究が重要な理由
がん免疫療法は多くの患者の治療を一変させましたが、長期的な恩恵を受けるのは一部にすぎません。本研究は、腫瘍が免疫系から身を守るために用いる隠れた化学的トリックを明らかにし、そのトリックを逆手に取る意外にシンプルな方法を示唆します。一般的な代謝副産物である乳酸がどのようにキラーT細胞から腫瘍を隠すのに寄与しているかを解明することで、現在の免疫療法の効果をより多くの患者に広げる新たな戦略が見えてきます。
がん細胞と免疫系の“会話”
免疫系は細胞間の分子レベルの「握手」に頼って、攻撃すべきか撤退すべきかを判断します。その中でも最も重要なものの一つが、腫瘍細胞上のタンパク質PD-L1とT細胞上のパートナーPD-1との相互作用です。がん細胞がPD-L1を多く発現すると、T細胞に攻撃を止めるよう信号を送って腫瘍の増殖を許してしまいます。PD-1やPD-L1を阻害する薬はこのブレーキを解除できますが、その成功は腫瘍がどれだけPD-L1を提示しているかに大きく依存します。したがって、がん細胞上のPD-L1量を制御する要因を理解することは、これら療法の反応を予測し改善するうえで重要です。
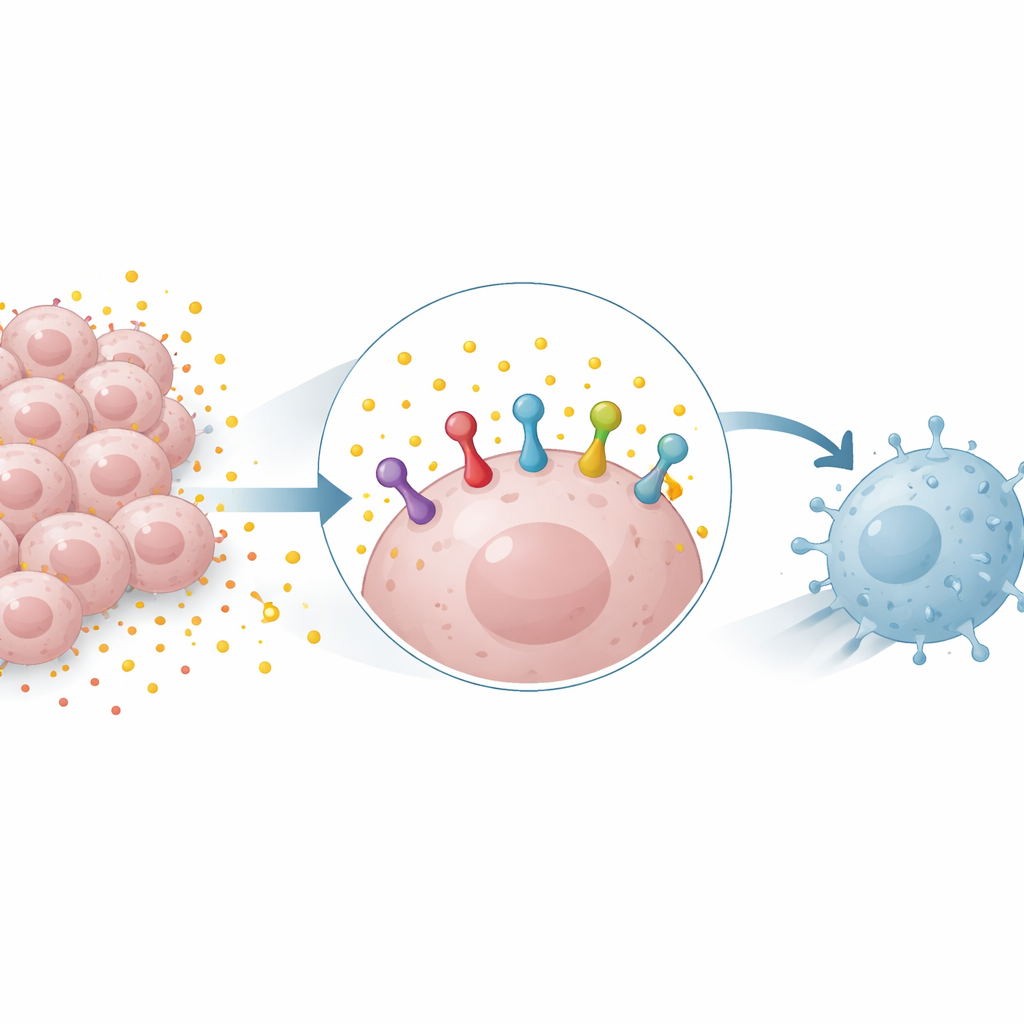
武器となる燃料の“廃棄物”
多くの腫瘍は解糖という糖分分解経路に強く依存しており、大量の乳酸を生み出します。長らく代謝の廃棄物とみなされてきた乳酸は、現在では能動的なシグナル分子として認識されています。研究者らは、乳酸を肺がんおよび乳がん細胞に添加するとPD-L1タンパク質の量が増え、解糖を阻害すると減少することを見いだしました。この効果はヒトとマウスの細胞の両方で観察され、乳酸がPD-L1遺伝子の転写を増やさなくても起こり得たため、乳酸は既存のPD-L1タンパク質を安定化している、つまり産生を増やすだけでなく分解を防いでいることが示唆されます。
PD-L1を守る小さな化学タグ
さらに掘り下げると、PD-L1には乳酸由来の小さな化学タグが結合しており、タンパク質の特定の構成要素(280位のリシン)に付加されていることが分かりました。このタグはラクトイル化と呼ばれ、複数の肺がん細胞株や正常気道細胞内のPD-L1で検出されました。研究者がその単一のリシンを修飾できないように変えると、PD-L1は乳酸依存の保護を失い、細胞によって破壊されやすくなりました。通常はHUWE1という分子機構がPD-L1の近傍にユビキチンという鎖を付けて廃棄ラベルを貼り付けますが、新しく見つかった乳酸由来のタグはHUWE1のアクセスを物理的に妨げ、この“ゴミラベル”の付加を阻止してPD-L1の分解から保護していました。
ラクトイルタグを付ける酵素
このタグがどのように付加されるかを調べるため、研究者らは乳酸を直接ドナーとして使える酵素を探索しました。その結果、通常は蛋白合成に関与するアラニルtRNA合成酵素1(AARS1)がPD-L1のラクトイル化を担う主要な“ライター”であることを特定しました。in vitro実験および細胞内で、AARS1はPD-L1の末端に乳酸基を付加できましたが、類縁酵素のAARS2はできませんでした。AARS1を過剰発現させるとPD-L1のラクトイル化が増え、HUWE1の結合とユビキチン付加が減少してチェックポイントタンパク質が安定化しました。逆にAARS1をサイレンシングするとその効果は消え、乳酸による安定化が失われたため、この酵素が腫瘍代謝とPD-L1保護を結ぶ重要な環となっていることが示されました。
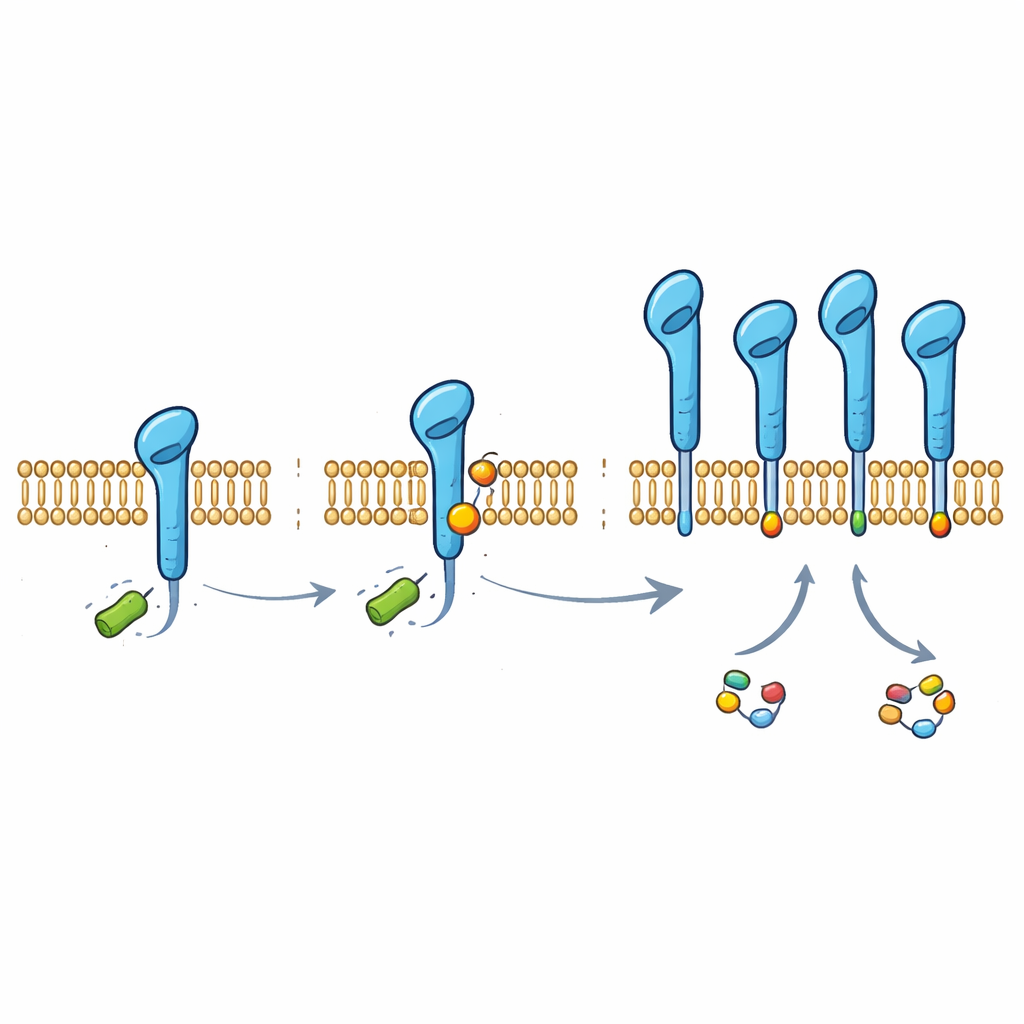
細胞レベルのトリックから治療機会へ
この化学修飾の生物学的影響はマウスで検証されました。ラクトイル化できない変異を持つPD-L1を発現する腫瘍細胞は、培養でCD8+ T細胞により容易に殺され、動物でははるかに小さい腫瘍を形成し、これらのキラー細胞の浸潤が増加しました。著者らは次に、すでに静脈内輸液などで医療的に用いられている乳酸の塩である乳酸ナトリウム(NaLa)を調べました。マウス肺がんモデルではNaLa単独で腫瘍増殖を促進することはなかったものの、抗PD-L1療法と組み合わせると治療の腫瘍制御力を有意に高め、腫瘍内のCD8+ T細胞の存在を増加させました。患者の肺がんサンプルでは、ラクトイル化されたPD-L1のレベルが高いほど病期が進行し生存率が低い傾向があり、この修飾が攻撃的な腫瘍や免疫療法への反応性のバイオマーカーになり得ることが示唆されました。
患者と将来の治療への意義
総じて、本研究は直接的な一連の流れを明らかにします:腫瘍代謝が乳酸を生み、乳酸がPD-L1の単一部位にタグを付け、そのタグがPD-L1の分解を阻み腫瘍がT細胞を沈黙させる。とはいえ、その同じ安定化はPD-L1標的薬にとって腫瘍をより目立たせる可能性もあります。実務的には、本研究はラクトイル化とそれを担うAARS1を、PD-L1による腫瘍保護の強さを調節する新たな操作点として提示します。このタグを患者腫瘍で測定し、それを微調整する治療を設計することで、将来的には誰が免疫療法の恩恵を受けるかをより正確に予測し、チェックポイント阻害薬と代謝介入を組み合わせてがんの燃料の“廃棄物”を治療上の弱点に変えることができるかもしれません。
引用: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
キーワード: PD-L1, 乳酸, 腫瘍免疫, 翻訳後修飾, 非小細胞肺がん