Clear Sky Science · sv
Laktylering stabiliserar PD-L1 för att främja tumöriös immunundvikelse och celltillväxt
Varför den här cancerhistorien är viktig
Cancerimmunterapi har förändrat behandlingen för många patienter, men endast en minoritet får långvarig nytta. Denna studie avslöjar ett dolt kemiskt knep som tumörer använder för att skydda sig mot immunsystemet — och föreslår ett överraskande enkelt sätt att vända knepet mot cancern. Genom att visa hur en vanlig metabol biprodukt, laktat, hjälper tumörer att gömma sig från mördande T‑celler, pekar arbetet på nya strategier för att få dagens immunterapier att fungera bättre och för fler patienter.
Hur cancerceller kommunicerar med immunsystemet
Vårt immunsystem förlitar sig på molekylära ”handlag” mellan celler för att avgöra när det ska attackera och när det ska stå tillbaka. En av de viktigaste interaktionerna sker mellan ett protein på tumörceller kallat PD‑L1 och dess partner PD‑1 på T‑celler. När PD‑L1 är rikligt uttryckt på cancerceller signalerar det till T‑celler att backa, vilket tillåter tumören att växa ostört. Läkemedel som blockerar PD‑1 eller PD‑L1 kan lossa den här spärren, men deras framgång beror ofta på hur mycket PD‑L1 tumören visar upp. Att förstå vad som reglerar PD‑L1‑nivåer på cancerceller är därför centralt för att förutsäga och förbättra svar på dessa behandlingar.
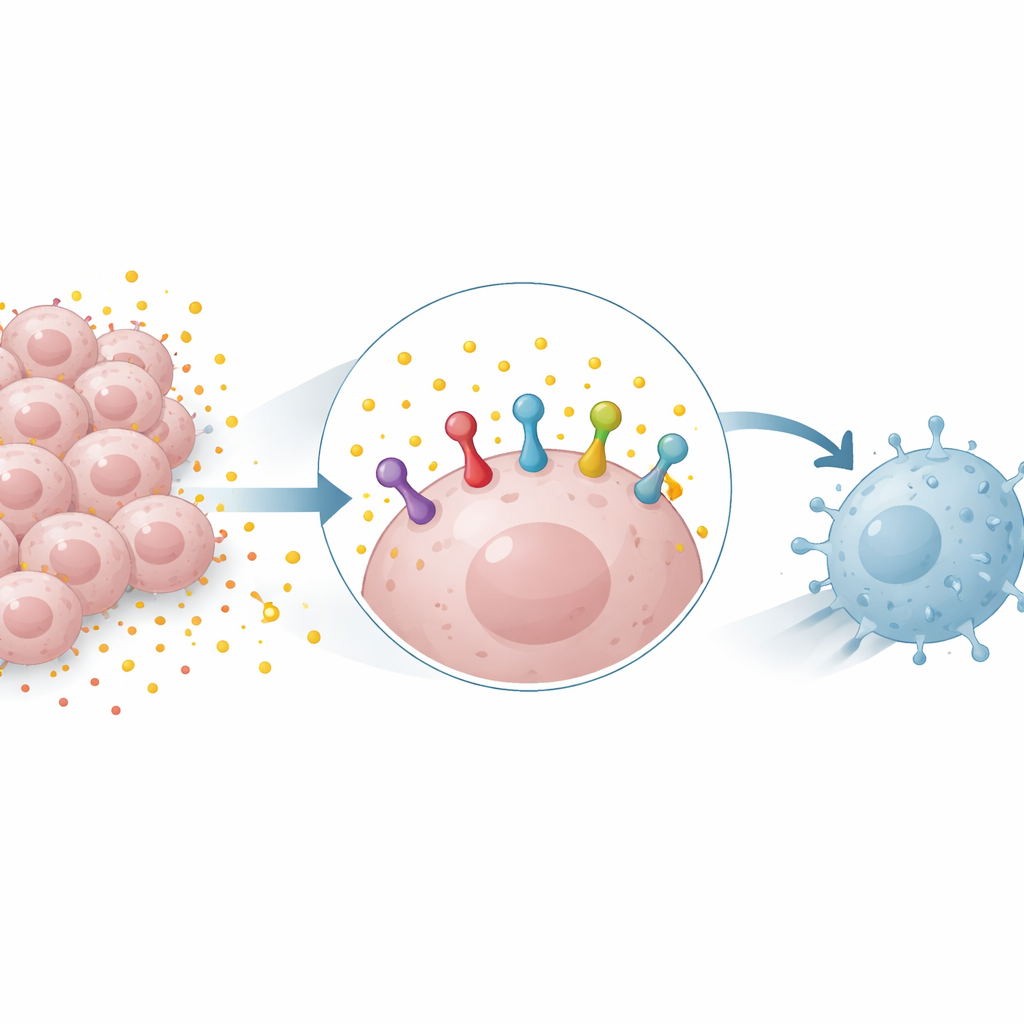
Avfallsbränsle som blir ett vapen
Många tumörer är starkt beroende av en sockerförbrännande process kallad glykolys, som producerar stora mängder laktat. Långt sett som främst metabolt avfall, ses laktat nu också som en aktiv signalsubstans. Forskarna fann att tillsats av laktat till lung‑ och bröstcancerceller ökade mängden PD‑L1‑protein, medan blockering av glykolys minskade den. Effekten sågs i både mänskliga och musceller och kunde uppstå även när laktat inte ökade PD‑L1‑gentranskription, vilket tyder på att laktat stabiliserade befintligt PD‑L1‑protein snarare än bara att öka dess produktion.
En liten kemisk etikett som skyddar PD‑L1
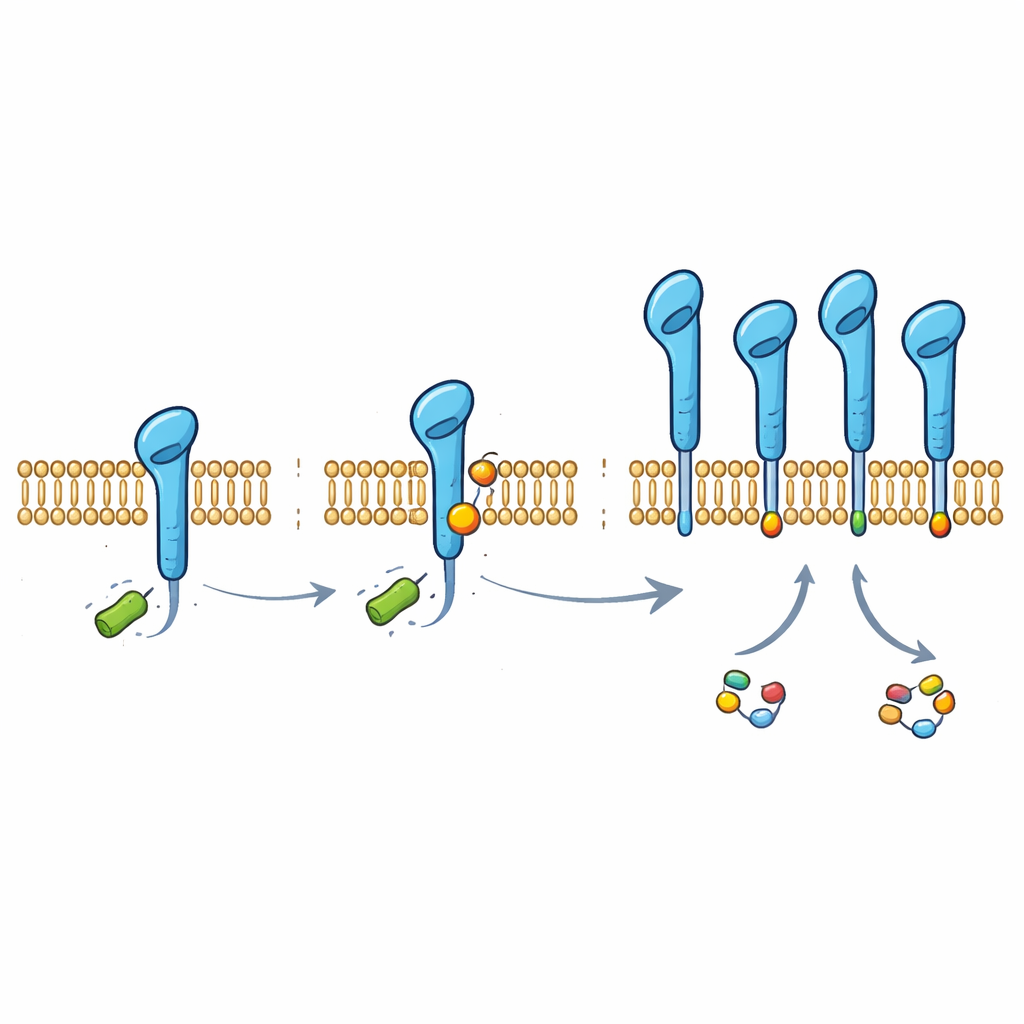
När de grävde djupare upptäckte teamet att PD‑L1 bär på en liten kemisk etikett härledd från laktat, fäst vid en särskild byggsten i proteinet (en lysin vid position 280). Denna etikett, kallad laktylering, hittades på PD‑L1 i flera lungcancercellinjer och i normala luftvägsceller. När forskarna ändrade den enskilda lysinen så att den inte längre kunde modifieras, förlorade PD‑L1 det mesta av sitt laktatberoende skydd och blev lättare för cellen att bryta ner. Normalt märker ett molekylärt maskineri vid namn HUWE1 PD‑L1 för borttagning genom att lägga till kedjor av ett annat litet protein, ubiquitin, vid en närliggande plats. Den nya laktatbaserade etiketten hindrar fysiskt HUWE1:s åtkomst, förhindrar att detta ”skräpetikett” fästs och skyddar därigenom PD‑L1 från nedbrytning.
Enzymet som skriver laktatet
För att förstå hur etiketten sätts på sökte forskarna efter enzymer som kan använda laktat direkt som donator. De identifierade alanyl‑tRNA‑syntetas 1 (AARS1), ett annars rutinärt proteintillverkningsenzym, som den viktigaste ”skrivaren” av PD‑L1‑laktylering. I provrörsexperiment och i celler kunde AARS1 fästa en laktatgrupp på PD‑L1‑svansen, medan ett besläktat enzym, AARS2, inte kunde det. Överuttryck av AARS1 ökade laktatetiketten på PD‑L1, minskade HUWE1‑bindning och ubiquitinmärkning och stabiliserade kontrollproteinet. Att tysta AARS1 gav motsatt effekt och utplånade laktatets stabiliserande inverkan, vilket visar att detta enzym är den avgörande länken mellan tumörmetabolism och PD‑L1‑skydd.
Från cellknep till behandlingsmöjligheter
De biologiska konsekvenserna av denna kemi testades i möss. Tumörceller konstruerade för att bära en icke‑laktylerbar version av PD‑L1 dödades lättare av CD8+ T‑celler i odling och bildade mycket mindre tumörer i djur, med större infiltration av dessa mördarceller. Författarna undersökte sedan natriumlaktat (NaLa), ett medicinskt använt laktatsalt som redan förekommer i intravenösa vätskor. I musmodeller av lungcancer påskyndade inte NaLa ensamt tumörtillväxt, men i kombination med anti‑PD‑L1‑terapi förbättrade det avsevärt behandlingens förmåga att kontrollera tumörer och ökade mängden CD8+ T‑celler i tumörerna. I patientprov från lungcancer var högre nivåer av PD‑L1 som bar laktatetiketten förenade med mer avancerad sjukdom och sämre överlevnad, vilket tyder på att denna modifiering skulle kunna fungera som en biomarkör för aggressiva tumörer och eventuellt för svar på immunterapi.
Vad detta betyder för patienter och framtida terapier
Tillsammans avslöjar fynden en direkt händelsekedja: tumörmetabolism producerar laktat; laktat används för att märka PD‑L1 på ett enda ställe; denna etikett blockerar proteinets nedbrytning och hjälper tumörer att tysta T‑celler. Samtidigt kan samma stabilisering göra tumörer mer synliga för läkemedel som riktar sig mot PD‑L1. I praktiska termer föreslår arbetet laktylering — och enzymet AARS1 som driver den — som nya spakar för att justera hur starkt PD‑L1 skyddar cancerceller. Genom att mäta denna etikett i patienters tumörer och utforma behandlingar som finjusterar den kan kliniker en dag bättre förutsäga vem som kommer att gynnas av immunterapi och kombinera checkpoint‑hämmare med metabola interventioner för att vända cancerns eget avfallsbränsle till en terapeutisk svaghet.
Citering: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Nyckelord: PD-L1, laktat, tumörimmunitet, posttranslationell modifiering, icke-småcellig lungcancer