Clear Sky Science · nl
Lactylatie stabiliseert PD-L1 om tumorimmuunontwijking en celgroei te bevorderen
Waarom dit kankeronderzoek ertoe doet
Immunotherapie tegen kanker heeft de behandeling van veel patiënten veranderd, maar slechts een minderheid ervaart langdurig voordeel. Deze studie onthult een verborgen chemisch trucje dat tumoren gebruiken om zich te verbergen voor het immuunsysteem — en suggereert een verrassend eenvoudige manier om dat trucje tegen de kanker te keren. Door te laten zien hoe een veelvoorkomend metabolisch bijproduct, lactaat, tumoren helpt weg te blijven van dodelijke T-cellen, wijst het werk op nieuwe strategieën om bestaande immuuntherapieën beter en voor meer mensen werkbaar te maken.
Hoe kankercellen communiceren met het immuunsysteem
Ons immuunsysteem vertrouwt op moleculaire “handdrukken” tussen cellen om te beslissen wanneer het moet aanvallen en wanneer het moet staken. Eén van de belangrijkste daarvan is de interactie tussen een eiwit op tumorcellen, PD-L1, en zijn partner PD-1 op T-cellen. Wanneer PD-L1 in grote hoeveelheden op kankercellen aanwezig is, zegt dat tegen T-cellen dat ze terug moeten trekken, waardoor de tumor ongehinderd kan groeien. Geneesmiddelen die PD-1 of PD-L1 blokkeren kunnen dit remmechanisme opheffen, maar hun succes hangt vaak af van hoeveel PD-L1 de tumor toont. Begrijpen wat PD-L1-niveaus op kankercellen reguleert is daarom cruciaal om reacties op deze behandelingen te voorspellen en te verbeteren.
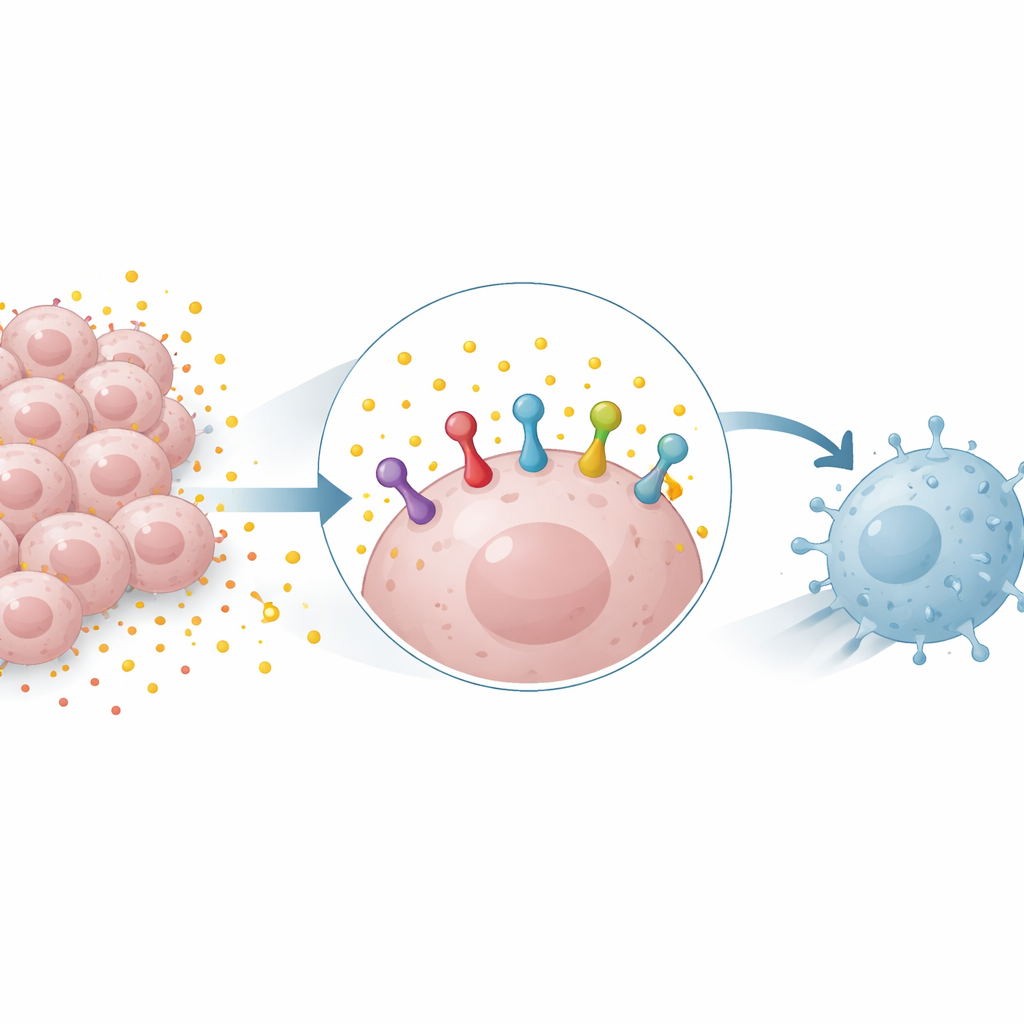
Brandstofafval dat een wapen wordt
Veel tumoren zijn sterk afhankelijk van glycolyse, een suikerverbrandingsproces dat grote hoeveelheden lactaat produceert. Lang beschouwd als vooral metabolisch afval, wordt lactaat nu erkend als een actief signaalmolecuul. De onderzoekers vonden dat het toevoegen van lactaat aan long- en borstkankercellen de hoeveelheid PD-L1-eiwit verhoogde, terwijl het blokkeren van glycolyse deze verminderde. Dit effect trad zowel in menselijke als muiscellen op en kon voorkomen zelfs wanneer lactaat de genactiviteit van PD-L1 niet verhoogde, wat impliceert dat lactaat bestaand PD-L1-eiwit stabiliseerde in plaats van alleen de productie ervan aan te zetten.
Een klein chemisch merkteken dat PD-L1 beschermt
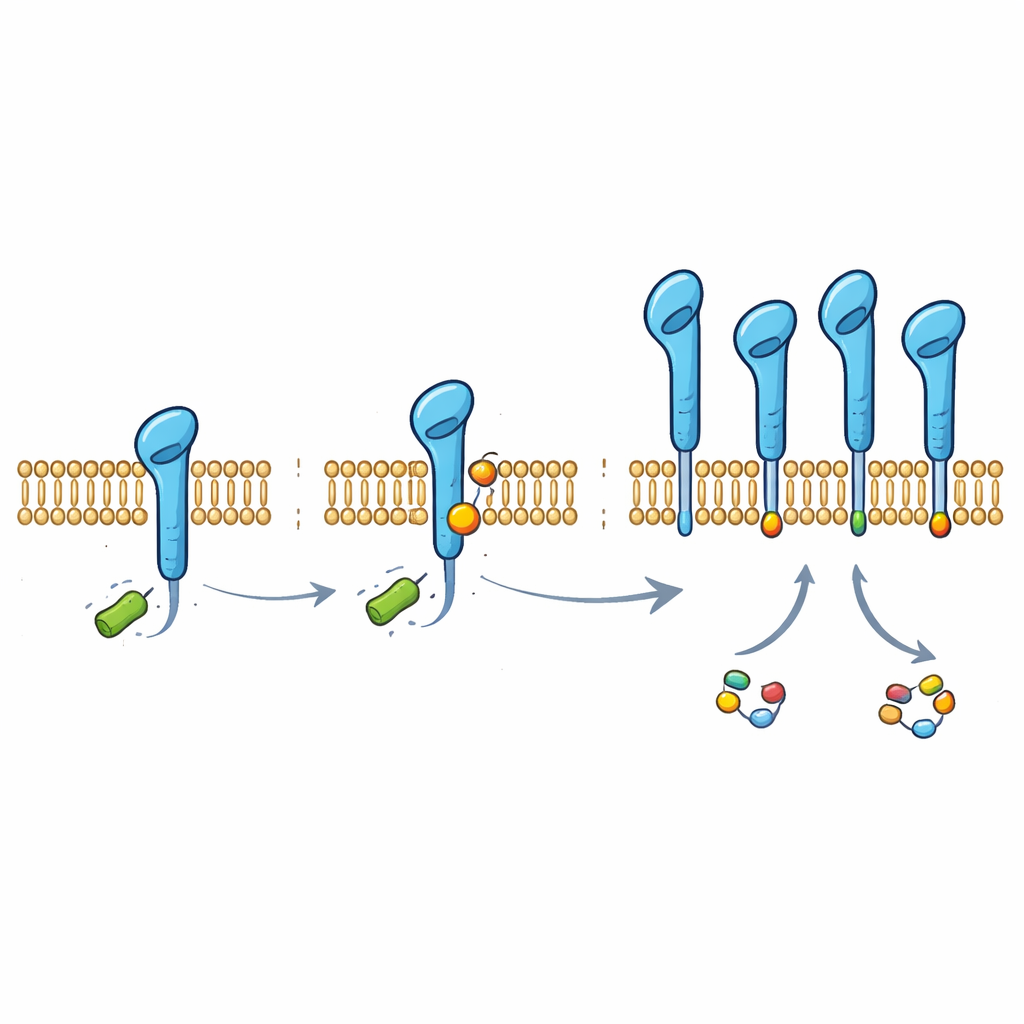
Dieper gravend ontdekten de onderzoekers dat PD-L1 een klein chemisch merkteken draagt afgeleid van lactaat, gehecht aan één specifiek bouwblok van het eiwit (een lysine op positie 280). Dit merkteken, lactylatie genoemd, werd aangetroffen op PD-L1 in meerdere longkankercellijnen en normale luchtwegcellen. Toen de wetenschappers die ene lysine zo veranderden dat hij niet meer gemodificeerd kon worden, verloor PD-L1 het grootste deel van zijn lactaatafhankelijke bescherming en werd het gemakkelijker voor de cel om het af te breken. Normaal markeert een moleculair complex genaamd HUWE1 PD-L1 voor afvoer door ketens van een ander klein molecuul, ubiquitine, toe te voegen op een nabije positie. Het nieuwe lactaatgebaseerde merkteken belemmert fysiek de toegang van HUWE1, voorkomt dat dit “afvallabel” wordt aangebracht en beschermt zo PD-L1 tegen afbraak.
Het enzym dat het lactaatstempel schrijft
Om te begrijpen hoe dit merkteken wordt toegevoegd, zochten de onderzoekers naar enzymen die lactaat direct als donor konden gebruiken. Ze identificeerden alanyl-tRNA-synthetase 1 (AARS1), een doorgaans routinematig eiwitsynthese-enzym, als de sleutel-“schrijver” van PD-L1-lactylatie. In proefbuisexperimenten en cellen kon AARS1 een lactaategroep aan de staart van PD-L1 bevestigen, terwijl een verwant enzym, AARS2, dat niet kon. Overexpressie van AARS1 verhoogde het lactaatstempel op PD-L1, verminderde HUWE1-binding en ubiquitine-tagging, en stabiliseerde het checkpoints-eiwit. Stilleggen van AARS1 had het tegenovergestelde effect en wist de stabiliserende impact van lactaat uit, wat aangeeft dat dit enzym de cruciale schakel is tussen tumormetabolisme en PD-L1-bescherming.
Van celtrucs naar behandelingskansen
De biologische consequenties van deze chemie werden getest in muizen. Tumorcellen die zo waren gemanipuleerd dat ze een niet-lactylatable versie van PD-L1 droegen, werden in kweek gemakkelijker gedood door CD8+ T-cellen en vormden veel kleinere tumoren in dieren, met een grotere infiltratie van deze dodelijke cellen. De auteurs onderzochten vervolgens natriumlactaat (NaLa), een medisch gebruikt zout van lactaat dat al veel voorkomt in intraveneuze vloeistoffen. In muismodellen van longkanker versnelde NaLa op zichzelf de tumorgroei niet, maar in combinatie met anti-PD-L1-therapie versterkte het de mogelijkheid van de behandeling om tumoren onder controle te houden en verhoogde het het aantal CD8+ T-cellen in de tumoren. In patiëntmonsters van longkanker werden hogere niveaus van PD-L1 met het lactaatstempel geassocieerd met meer gevorderde ziekte en slechtere overleving, wat suggereert dat deze modificatie als biomarker voor agressieve tumoren en mogelijk voor respons op immunotherapie zou kunnen dienen.
Wat dit betekent voor patiënten en toekomstige therapieën
Samengevat onthullen de bevindingen een directe keten van gebeurtenissen: tumormetabolisme produceert lactaat; lactaat wordt gebruikt om PD-L1 op één plek te etiketteren; dit etiket blokkeert de afbraak van het eiwit en helpt tumoren T-cellen te laten zwijgen. Toch kan diezelfde stabilisatie tumoren ook gevoeliger maken voor geneesmiddelen die op PD-L1 gericht zijn. In praktische zin stelt dit werk lactylatie — en het AARS1-enzym dat het aandrijft — voor als nieuwe knoppen om te draaien aan de mate waarin PD-L1 kankercellen beschermt. Door dit merkteken in patiëntentumoren te meten en behandelingen te ontwerpen die het fijnregelen, kunnen clinici mogelijk beter voorspellen wie baat heeft bij immunotherapie en checkpointremmers combineren met metabole interventies om het brandstofafval van kanker tot een therapeutische zwakte te maken.
Bronvermelding: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Trefwoorden: PD-L1, lactaat, tumorimmuniteit, post-translationele modificatie, niet-kleincellig longkanker