Clear Sky Science · pt
A lactilação estabiliza PD-L1 para promover evasão imune tumoral e crescimento celular
Por que essa descoberta sobre câncer importa
A imunoterapia contra o câncer transformou o tratamento de muitos pacientes, mas apenas uma minoria obtém benefícios duradouros. Este estudo revela um truque químico oculto que os tumores usam para se proteger do sistema imunológico — e sugere uma maneira surpreendentemente simples de usar esse truque contra o próprio câncer. Ao mostrar como um subproduto metabólico comum, o lactato, ajuda os tumores a se esconderem de células T citotóxicas, o trabalho aponta para novas estratégias para tornar as terapias imunológicas atuais mais eficazes e acessíveis a mais pessoas.
Como as células cancerosas se comunicam com o sistema imune
Nosso sistema imunológico conta com ‘‘apertos de mão’’ moleculares entre células para decidir quando atacar e quando recuar. Um dos mais importantes é entre uma proteína nas células tumorais chamada PD-L1 e sua parceira PD-1 nas células T. Quando o PD-L1 está em abundância nas células cancerosas, ele sinaliza às células T que recuem, permitindo que o tumor cresça sem controle. Medicamentos que bloqueiam PD-1 ou PD-L1 podem soltar esse freio, mas seu sucesso muitas vezes depende de quanto PD-L1 o tumor exibe. Entender o que controla os níveis de PD-L1 nas células cancerosas é, portanto, fundamental para prever e melhorar as respostas a esses tratamentos.
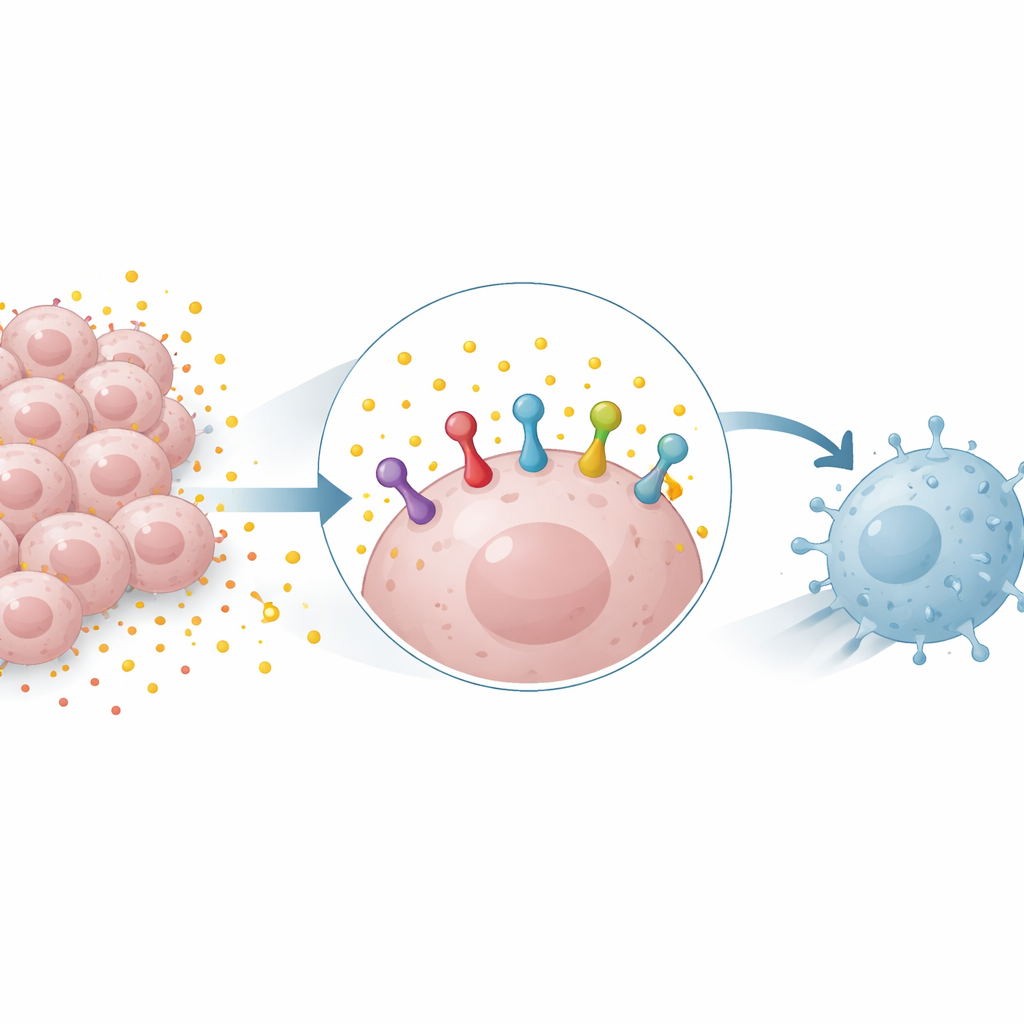
Resíduo de combustível que vira arma
Muitos tumores dependem fortemente de um processo de queima de açúcar chamado glicólise, que produz grandes quantidades de lactato. Visto por muito tempo principalmente como resíduo metabólico, o lactato é agora reconhecido como uma molécula de sinalização ativa. Os pesquisadores descobriram que adicionar lactato a células de câncer de pulmão e de mama aumentou a quantidade da proteína PD-L1, enquanto bloquear a glicólise a reduziu. Esse efeito apareceu em células humanas e de camundongo e podia ocorrer mesmo quando o lactato não aumentava a atividade gênica do PD-L1, o que sugere que o lactato estava estabilizando a proteína PD-L1 já existente em vez de apenas ativar sua produção.
Uma pequena marca química que protege o PD-L1
Aprofundando, a equipe descobriu que PD-L1 carrega uma pequena marca química derivada do lactato, ligada a um determinado bloco de construção da proteína (uma lisina na posição 280). Essa marca, chamada lactilação, foi encontrada em PD-L1 dentro de várias linhagens de câncer de pulmão e em células das vias aéreas normais. Quando os cientistas alteraram essa única lisina para que não pudesse mais ser modificada, o PD-L1 perdeu a maior parte da proteção dependente de lactato e tornou-se mais fácil de ser degradado pela célula. Normalmente, uma máquina molecular chamada HUWE1 marca o PD-L1 para descarte ao adicionar cadeias de outra pequena molécula, a ubiquitina, numa posição próxima. A nova etiqueta baseada em lactato interfere fisicamente no acesso da HUWE1, impedindo que esse ‘‘rótulo de lixo’’ seja anexado e, assim, protegendo o PD-L1 da degradação.
A enzima que escreve a marca de lactato
Para entender como essa marca é adicionada, os pesquisadores procuraram enzimas que pudessem usar o lactato diretamente como doador. Identificaram a alanil-tRNA sintetase 1 (AARS1), uma enzima rotineira da síntese proteica, como a principal ‘‘escritora’’ da lactilação do PD-L1. Em experimentos in vitro e em células, a AARS1 conseguiu anexar um grupo lactato à cauda do PD-L1, enquanto uma enzima relacionada, AARS2, não o fez. A superexpressão de AARS1 aumentou a marca de lactato no PD-L1, reduziu a ligação da HUWE1 e a ubiquitinação, e estabilizou a proteína de checkpoint. Silenciar a AARS1 teve o efeito oposto e aboliu o impacto estabilizador do lactato, indicando que essa enzima é a ligação crucial entre o metabolismo tumoral e a proteção do PD-L1.
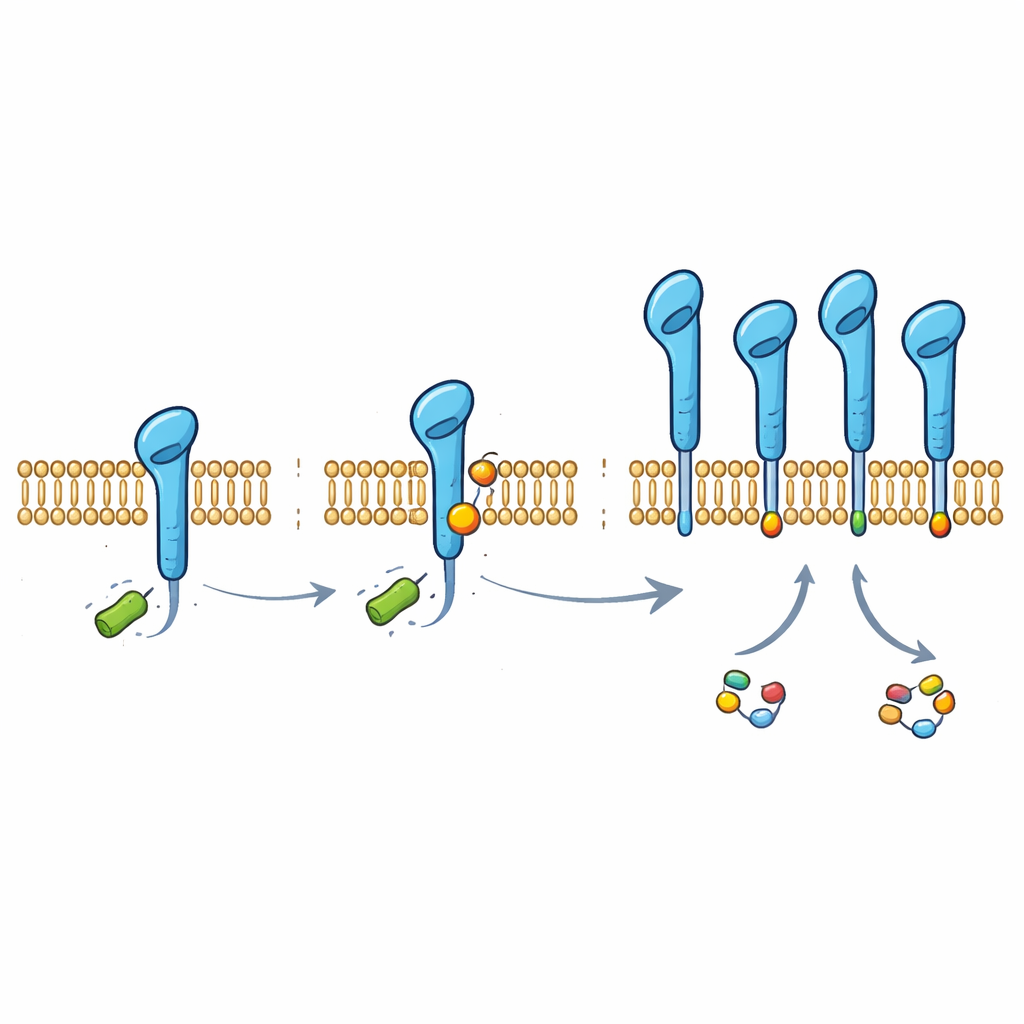
De artifícios celulares a oportunidades terapêuticas
As consequências biológicas dessa química foram testadas em camundongos. Células tumorais modificadas para carregar uma versão do PD-L1 que não podia ser lactilada foram mais facilmente eliminadas por células T CD8+ em cultura e formaram tumores muito menores nos animais, com maior infiltração dessas células citotóxicas. Os autores então exploraram o lactato de sódio (NaLa), um sal medicamente usado do lactato já comum em fluidos intravenosos. Em modelos murinos de câncer de pulmão, NaLa isoladamente não acelerou o crescimento tumoral, mas quando combinado com terapia anti-PD-L1 aumentou significativamente a capacidade do tratamento de controlar os tumores e elevou a presença de células CD8+ em seu interior. Em amostras de pacientes com câncer de pulmão, níveis mais altos de PD-L1 portando a marca de lactato foram associados a doença mais avançada e pior sobrevida, sugerindo que essa modificação poderia servir como biomarcador de tumores agressivos e possivelmente de resposta à imunoterapia.
O que isso significa para pacientes e terapias futuras
Em conjunto, os achados revelam uma cadeia direta de eventos: o metabolismo tumoral produz lactato; o lactato é usado para marcar o PD-L1 em um único ponto; essa marca bloqueia a destruição da proteína e ajuda os tumores a silenciar células T. Ainda assim, essa mesma estabilização pode tornar os tumores mais visíveis a medicamentos que miram o PD-L1. Em termos práticos, este trabalho propõe a lactilação — e a enzima AARS1 que a promove — como novas alavancas para ajustar o quanto o PD-L1 protege as células cancerosas. Ao medir essa marca em tumores de pacientes e desenhar tratamentos que a modulam, clínicos podem, no futuro, prever melhor quem se beneficiará da imunoterapia e combinar bloqueadores de checkpoints com intervenções metabólicas para transformar o próprio resíduo combustível do câncer em uma fraqueza terapêutica.
Citação: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Palavras-chave: PD-L1, lactato, imunidade tumoral, modificação pós-traducional, câncer de pulmão não pequenas células