Clear Sky Science · ar
اللاكتيلَة تُثبّت PD-L1 لتعزز تهرّب الورم المناعي ونمو الخلايا
لماذا تهم هذه القصة السرطانية
حوّلت العلاجات المناعية للسرطان مآلات العديد من المرضى، لكن قلة فقط تحقق فائدة طويلة الأمد. تكشف هذه الدراسة حيلة كيميائية مخفية تستخدمها الأورام لتحمي نفسها من الجهاز المناعي — وتقترح طريقة مفاجِئة البساطة لاستغلال هذه الحيلة ضد السرطان. من خلال توضيح كيف يساعد ناتج أيضي شائع، اللاكتات، الأورام على التخفّي من خلايا T القاتلة، تشير النتائج إلى استراتيجيات جديدة لجعل العلاجات المناعية الحالية تعمل بشكل أفضل ولعدد أكبر من المرضى.
كيف تتواصل خلايا السرطان مع الجهاز المناعي
يعتمد جهازنا المناعي على «مصافحات» جزيئية بين الخلايا ليقرر متى يهاجم ومتى يتراجع. من أهم هذه التفاعلات بروتين على خلايا الورم يُسمى PD-L1 وشريكه PD-1 على خلايا T. عندما يكون PD-L1 وافرًا على خلايا السرطان، يعلِّم خلايا T بالانسحاب، مما يسمح للورم بالنمو دون رقابة. الأدوية التي تحجب PD-1 أو PD-L1 يمكنها إزالة هذا المكبح، لكن نجاحها غالبًا ما يتوقف على كمية PD-L1 التي يعرضها الورم. لذا فإن فهم ما يتحكم بمستويات PD-L1 على خلايا السرطان أمر محوري لتوقع وتحسين الاستجابة لهذه العلاجات.
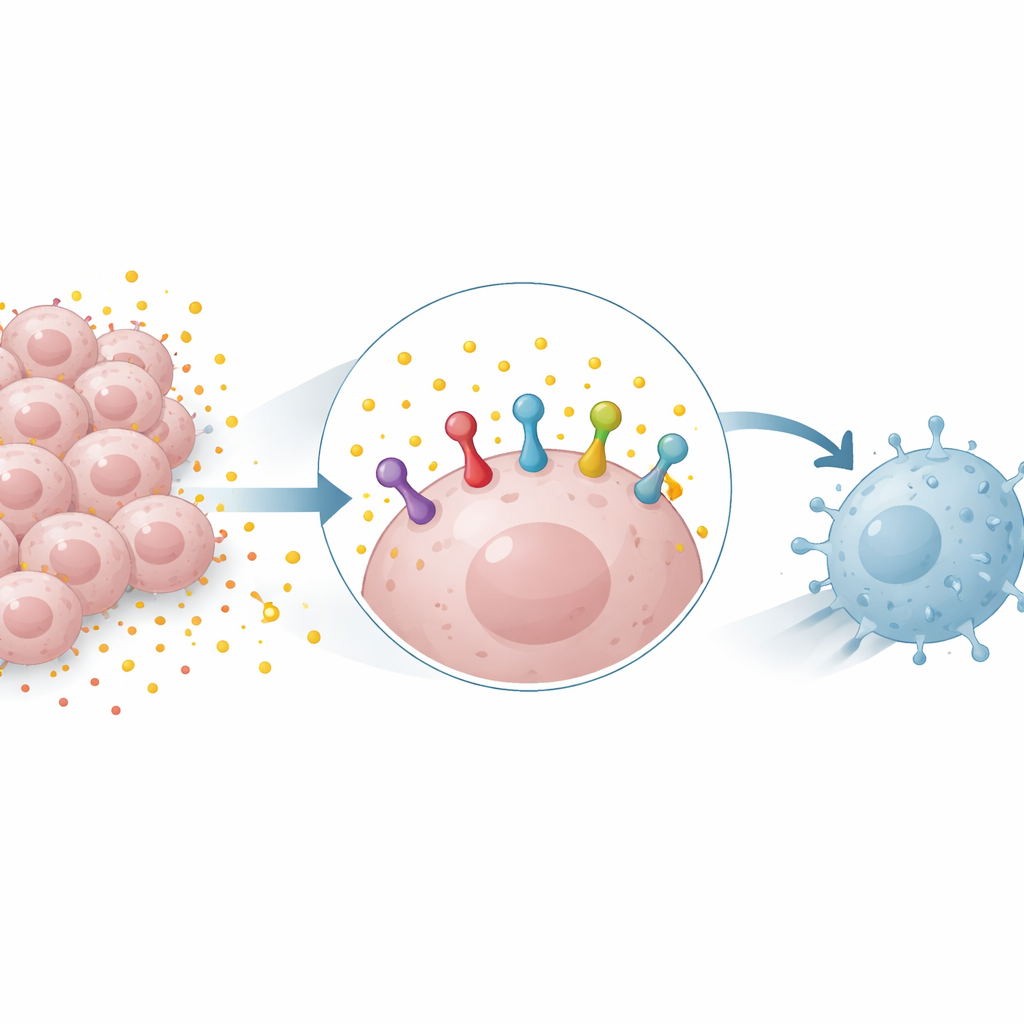
نفاية الوقود التي تتحول إلى سلاح
تعتمد العديد من الأورام بصورة كبيرة على عملية احتراق السكر المسماة تحلل السكر (glycolysis)، التي تُنتج كميات كبيرة من اللاكتات. كان يُنظر إلى اللاكتات طويلاً على أنه نفاية أيضية بحتة، لكن الآن يُعترف به كجزيء إشارِي نشط. وجد الباحثون أن إضافة اللاكتات إلى خلايا سرطان الرئة والثدي زادت من كمية بروتين PD-L1، بينما أدَّى حجب تحلل السكر إلى تقليلها. ظهر هذا التأثير في خلايا بشرية وفأرية ويمكن أن يحدث حتى عندما لا تزيد اللاكتات نشاط جين PD-L1، ما يوحِي بأن اللاكتات كانت تُثبّت بروتين PD-L1 الموجود بالفعل بدلاً من مجرد تشغيل إنتاجه.
وسم كيميائي بسيط يحمي PD-L1
بالتعمق، اكتشف الفريق أن PD-L1 يحمل وسمًا كيميائيًا صغيرًا مشتقًا من اللاكتات، مُلحَقًا بوحيد بناء معين في البروتين (اللايزين عند الموضع 280). وُجدت هذه اللاكتيلَة على PD-L1 داخل عدة خطوط خلايا سرطانية رئوية وخلايا الممرات الهوائية الطبيعية. عندما غيّر العلماء ذلك اللايزين المفرد بحيث لا يمكن تعديله، فقد PD-L1 معظم حمايته المعتمدة على اللاكتات وأصبح أسهل للخلية في تدميره. عادةً، تُشير آلة جزيئية تُدعى HUWE1 إلى PD-L1 للتخلص منه عبر إضافة سلاسل من جزيء صغير آخر، اليوبيكوين، في موضع مجاور. يتداخل الوسم القائم على اللاكتات ماديًا مع وصول HUWE1، مانعًا إرفاق هذا «وسم النفاية» وبالتالي محميًا PD-L1 من التحطيم.
الإنزيم الذي يكتب وسم اللاكتات
لفهم كيفية إضافة هذا الوسم، بحث الباحثون عن إنزيمات يمكنها استخدام اللاكتات مباشرة كمانح. حددوا إنزيم ألانيل-نقل RNA سينثِتاز 1 (AARS1)، وهو إنزيم تركيب بروتين روتيني عادةً، كـ"كاتب" رئيسي للاكتيلَة على PD-L1. في تجارب أنبوبية وخلوية، استطاع AARS1 إلحاق مجموعة لاكتات بذيل PD-L1، بينما لم يتمكن إنزيم قريب، AARS2، من ذلك. أدى إفراط التعبير عن AARS1 إلى زيادة الوسم اللاكتاتي على PD-L1، وتقليل ارتباط HUWE1 ووَسم اليوبيكوين، وتثبيت بروتين نقطة التفتيش. وأدّى إسكات AARS1 إلى العكس وتمحي أثر التثبيت الناتج عن اللاكتات، مما يشير إلى أن هذا الإنزيم هو الحلقة الحاسمة بين أيض الورم وحماية PD-L1.
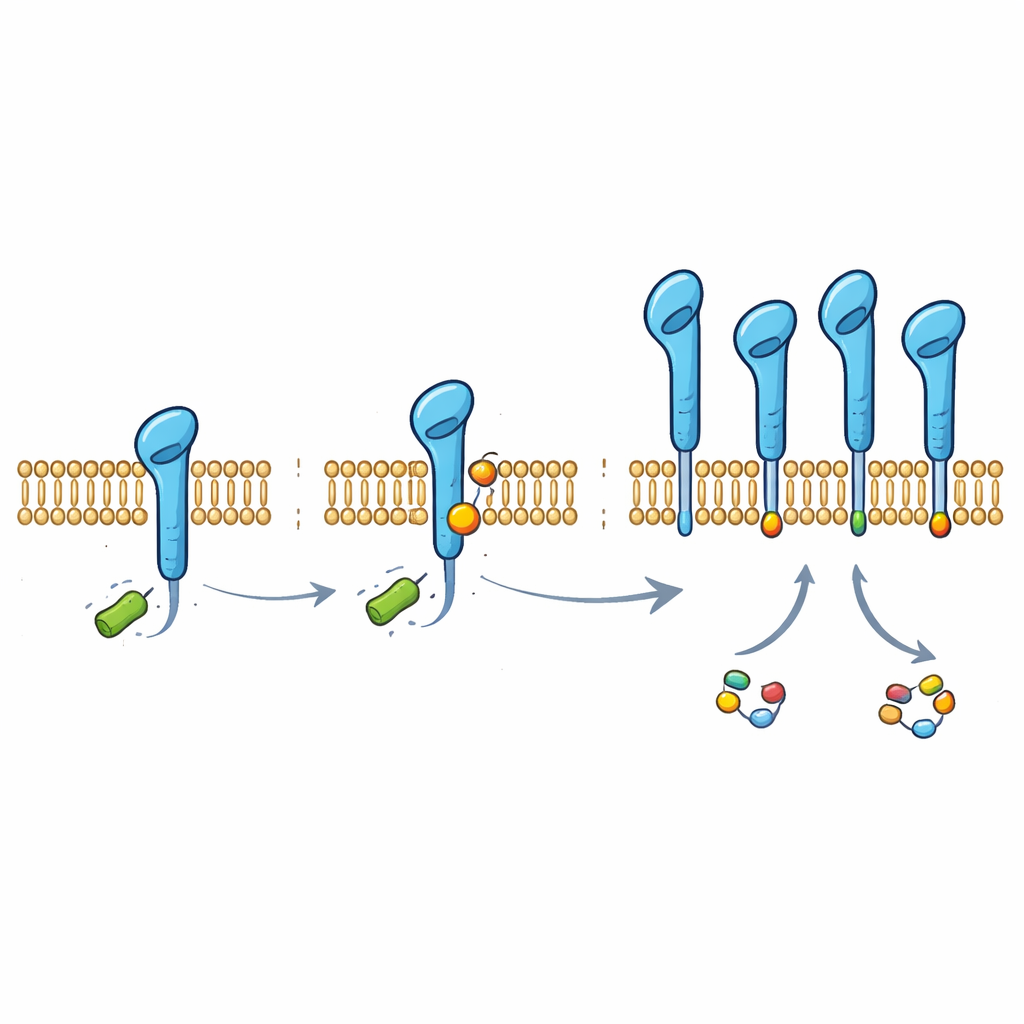
من حِيَل الخلايا إلى فرص العلاج
اختُبرت العواقب البيولوجية لهذه الكيمياء في الفئران. كانت الخلايا الورمية المُهندَسة لتحمل نسخة من PD-L1 لا تقبل اللاكتيلَة أكثر عرضة للقتل بواسطة خلايا CD8+ T في الزرائع وشكلت أورامًا أصغر بكثير في الحيوان، مع توغل أكبر لهذه الخلايا القاتلة. استكشف المؤلفون بعد ذلك لاكتات الصوديوم (NaLa)، ملح طبي للاكتات يُستخدم في السوائل الوريدية. في نماذج سرطان الرئة عند الفئران، لم يسرّع NaLa وحده نمو الورم، لكنه عند دمجه مع علاج مضاد لـ PD-L1 عزّز بشكل ملحوظ قدرة العلاج على السيطرة على الأورام وزاد وجود خلايا CD8+ داخلها. في عينات مرضى سرطان الرئة، ارتبطت مستويات أعلى من PD-L1 الحامل لوسم اللاكتات بمرض أكثر تقدمًا وببقاء أسوأ، مما يوحي أن هذا التعديل قد يكون علامة بيولوجية للأورام العدوانية وربما للاستجابة للعلاج المناعي.
ما يعنيه هذا للمرضى والعلاجات المستقبلية
تجمع النتائج، مجتمعة، سلسلة مباشرة من الأحداث: يُنتج أيض الورم اللاكتات؛ تُستخدم اللاكتات لوسم PD-L1 في موضع واحد؛ يمنع هذا الوسم تدمير البروتين ويساعد الأورام على إسكات خلايا T. ومع ذلك، قد تجعل هذه التثبيتة نفسها الأورام أكثر تعرضًا للأدوية المستهدفة لـ PD-L1. عمليًا، تقترح هذه العمل أن اللاكتيلَة — وإنزيم AARS1 الذي يقودها — تمثلان رافعات جديدة لضبط مدى حماية PD-L1 للخلايا السرطانية. بقياس هذا الوسم في أورام المرضى وتصميم علاجات تضبطه بدقة، قد يتمكن الأطباء يومًا ما من توقع من سيستفيد من العلاج المناعي بشكل أفضل وإقران مثبطات نقاط التفتيش بتدخلات أيضية لتحويل نفاية وقود السرطان إلى نقطة ضعف علاجية.
الاستشهاد: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
الكلمات المفتاحية: PD-L1, اللاكتات, مناعة الورم, تعديل بعد الترجمة, سرطان الرئة غير صغير الخلايا