Clear Sky Science · fr
La lactylation stabilise PD-L1 pour favoriser l’évasion immunitaire tumorale et la croissance cellulaire
Pourquoi cette découverte sur le cancer est importante
L’immunothérapie anticancéreuse a transformé le traitement de nombreux patients, mais seule une minorité bénéficie d’effets durables. Cette étude révèle une astuce chimique cachée que les tumeurs utilisent pour se protéger du système immunitaire — et suggère une manière étonnamment simple de retourner cette astuce contre le cancer. En montrant comment un sous‑produit métabolique courant, le lactate, aide les tumeurs à se dissimuler face aux lymphocytes T tueurs, le travail ouvre des pistes pour améliorer l’efficacité des thérapies immunitaires existantes et étendre leurs bénéfices à davantage de patients.
Comment les cellules cancéreuses communiquent avec le système immunitaire
Notre système immunitaire s’appuie sur des « poignées de main » moléculaires entre cellules pour décider quand attaquer et quand se retirer. L’une des plus importantes oppose une protéine des cellules tumorales, PD‑L1, à son partenaire PD‑1 présent sur les lymphocytes T. Lorsqu’il y a beaucoup de PD‑L1 à la surface des cellules cancéreuses, cela ordonne aux lymphocytes T de se retenir, permettant à la tumeur de croître sans contrôle. Les médicaments qui bloquent PD‑1 ou PD‑L1 peuvent desserrer ce frein, mais leur succès dépend souvent de la quantité de PD‑L1 exposée par la tumeur. Comprendre ce qui règle le niveau de PD‑L1 sur les cellules cancéreuses est donc central pour prédire et améliorer les réponses à ces traitements.
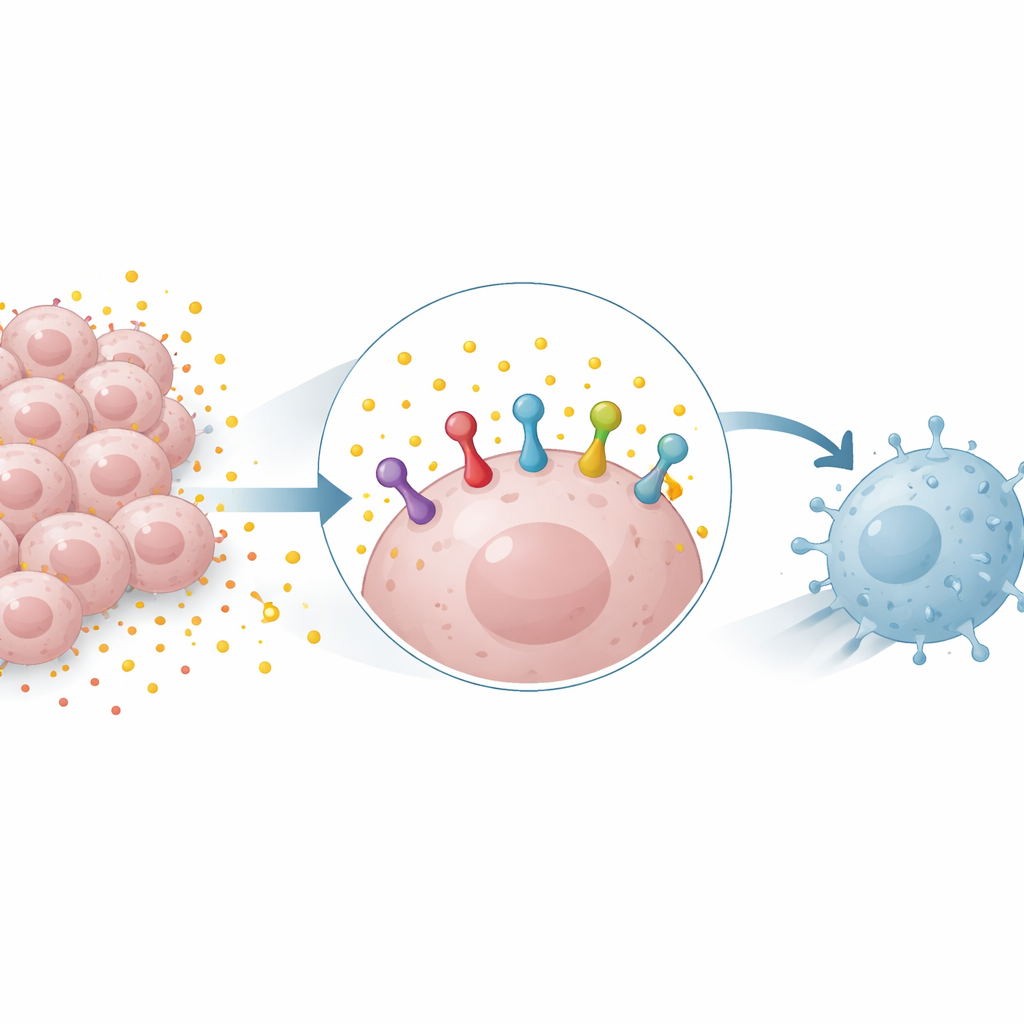
Des déchets énergétiques devenus arme
Be nombreuses tumeurs s’appuient fortement sur un processus de dégradation du sucre appelé glycolyse, qui produit de grandes quantités de lactate. Longtemps considéré principalement comme un déchet métabolique, le lactate est désormais reconnu comme une molécule de signalisation active. Les chercheurs ont constaté que l’ajout de lactate à des cellules de cancer du poumon et du sein augmentait la quantité de protéine PD‑L1, tandis que le blocage de la glycolyse la réduisait. Cet effet apparaissait aussi bien dans des cellules humaines que murines et pouvait survenir même lorsque le lactate n’augmentait pas l’activité du gène PD‑L1, ce qui suggère que le lactate stabilisait la protéine PD‑L1 existante plutôt que d’accroître simplement sa production.
Une petite étiquette chimique qui protège PD‑L1
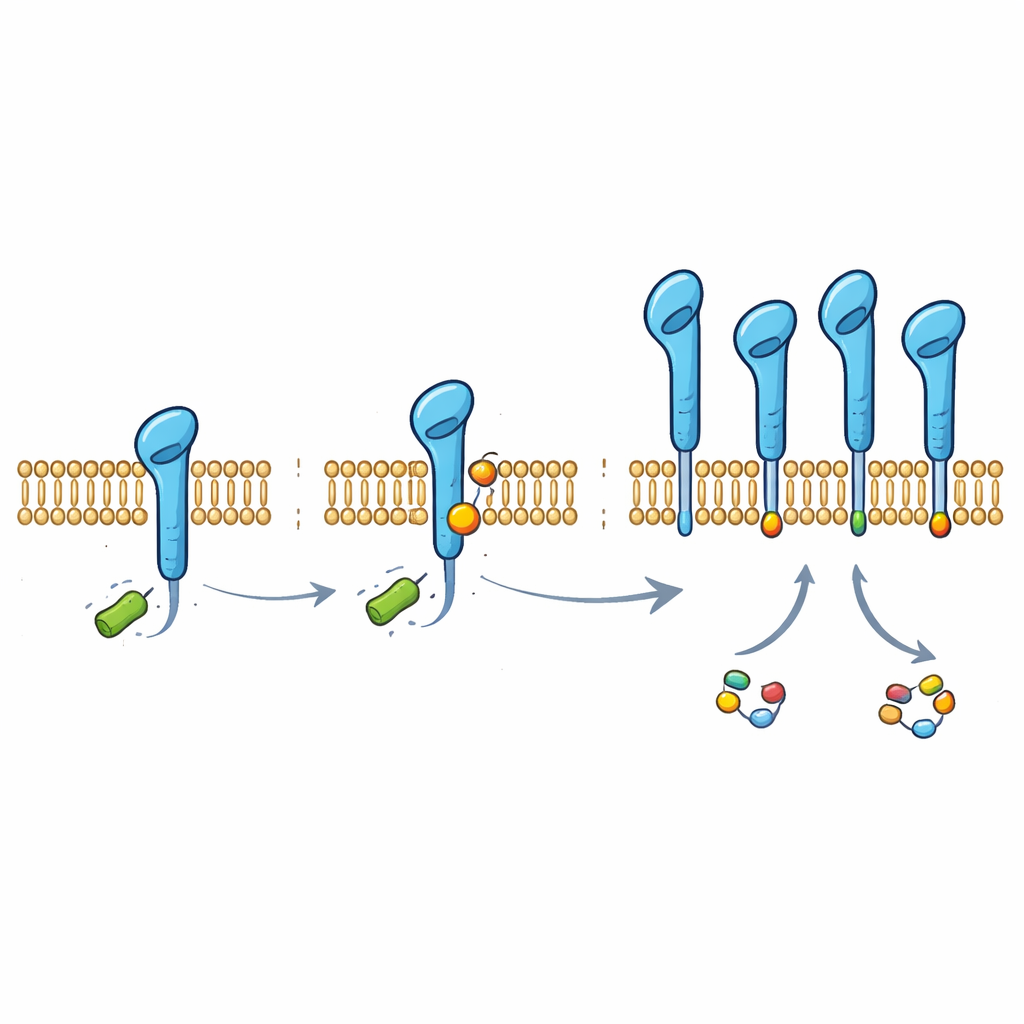
En creusant plus loin, l’équipe a découvert que PD‑L1 porte une petite étiquette chimique dérivée du lactate, attachée à un acide aminé particulier de la protéine (une lysine en position 280). Cette marque, appelée lactylation, a été détectée sur PD‑L1 dans plusieurs lignées de cellules de cancer du poumon et dans des cellules normales des voies aériennes. Lorsque les scientifiques ont modifié cette lysine unique pour qu’elle ne puisse plus être modifiée, PD‑L1 perdait la majeure partie de sa protection dépendante du lactate et devenait plus facilement dégradée par la cellule. Normalement, une machinerie moléculaire nommée HUWE1 marque PD‑L1 pour élimination en ajoutant des chaînes d’une autre petite molécule, l’ubiquitine, à une position voisine. La nouvelle étiquette à base de lactate gêne physiquement l’accès de HUWE1, empêchant l’ajout de ce « tampon poubelle » et protégeant ainsi PD‑L1 de la dégradation.
L’enzyme qui écrit l’étiquette lactate
Pour comprendre comment cette marque est ajoutée, les chercheurs ont cherché des enzymes capables d’utiliser directement le lactate comme donneur. Ils ont identifié l’alanyl‑ARNt synthétase 1 (AARS1), une enzyme normalement impliquée dans la synthèse protéique, comme le « rédacteur » clé de la lactylation de PD‑L1. Dans des expériences in vitro et en cellules, AARS1 pouvait fixer un groupe lactate sur la queue de PD‑L1, alors qu’une enzyme apparentée, AARS2, ne le pouvait pas. La surexpression d’AARS1 augmentait la marque lactate sur PD‑L1, réduisait la liaison de HUWE1 et l’ubbquitinylation, et stabilisait la protéine de point de contrôle. L’inhibition d’AARS1 produisait l’effet inverse et annulait l’impact stabilisant du lactate, indiquant que cette enzyme constitue le maillon crucial entre le métabolisme tumoral et la protection de PD‑L1.
Des astuces cellulaires aux opportunités thérapeutiques
Les conséquences biologiques de cette chimie ont été testées chez la souris. Des cellules tumorales ingénierées pour porter une version non lactylable de PD‑L1 étaient plus facilement tuées par des lymphocytes T CD8+ en culture et formaient des tumeurs beaucoup plus petites chez l’animal, avec une infiltration accrue de ces cellules tueuses. Les auteurs ont ensuite exploré le lactate de sodium (NaLa), un sel de lactate utilisé médicalement et courant dans les solutions intraveineuses. Dans des modèles murins de cancer du poumon, le NaLa seul n’accélérait pas la croissance tumorale, mais lorsqu’il était associé à une thérapie anti‑PD‑L1, il augmentait significativement la capacité du traitement à contrôler les tumeurs et favorisait la présence de lymphocytes CD8+ en leur sein. Dans des échantillons de patients atteints de cancer du poumon, des taux plus élevés de PD‑L1 portant la marque lactate étaient associés à des maladies plus avancées et à une survie réduite, suggérant que cette modification pourrait servir de biomarqueur pour des tumeurs agressives et éventuellement pour la réponse à l’immunothérapie.
Ce que cela signifie pour les patients et les thérapies futures
Pris ensemble, les résultats révèlent une chaîne directe d’événements : le métabolisme tumoral produit du lactate ; le lactate est utilisé pour marquer PD‑L1 en un point précis ; cette étiquette empêche la destruction de la protéine et aide les tumeurs à étouffer les lymphocytes T. Cependant, cette même stabilisation peut rendre les tumeurs plus sensibles aux médicaments ciblant PD‑L1. Sur le plan pratique, ce travail identifie la lactylation — et l’enzyme AARS1 qui la catalyse — comme de nouveaux leviers pour ajuster la protection de PD‑L1 sur les cellules cancéreuses. En mesurant cette marque dans les tumeurs des patients et en concevant des traitements pour la moduler, les cliniciens pourraient un jour mieux prédire qui bénéficiera de l’immunothérapie et associer les bloqueurs de points de contrôle à des interventions métaboliques pour transformer le déchet énergétique du cancer en faiblesse thérapeutique.
Citation: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Mots-clés: PD-L1, lactate, immunité tumorale, modification post‑traductionnelle, cancer du poumon non à petites cellules