Clear Sky Science · es
La lactilación estabiliza PD-L1 para promover la evasión inmune tumoral y el crecimiento celular
Por qué importa esta historia sobre el cáncer
La inmunoterapia contra el cáncer ha transformado el tratamiento de muchos pacientes, sin embargo solo una minoría obtiene beneficios duraderos. Este estudio desvela un truco químico oculto que los tumores emplean para protegerse del sistema inmune —y sugiere una forma sorprendentemente simple de volver ese truco en su contra. Al revelar cómo un subproducto metabólico común, el lactato, ayuda a los tumores a esconderse de las células T citotóxicas, el trabajo apunta a nuevas estrategias para mejorar la eficacia de las terapias inmunes actuales y ampliar su alcance.
Cómo se comunican las células cancerosas con el sistema inmune
Nuestro sistema inmunitario se basa en “apretones de manos” moleculares entre células para decidir cuándo atacar y cuándo mantenerse al margen. Uno de los más importantes es la interacción entre una proteína en las células tumorales llamada PD-L1 y su pareja PD-1 en las células T. Cuando PD-L1 abunda en las células cancerosas, indica a las células T que se retiren, permitiendo que el tumor crezca sin control. Los fármacos que bloquean PD-1 o PD-L1 pueden liberar ese freno, pero su éxito a menudo depende de cuánto PD-L1 muestre el tumor. Entender qué controla los niveles de PD-L1 en las células cancerosas es, por tanto, fundamental para predecir y mejorar las respuestas a estos tratamientos.
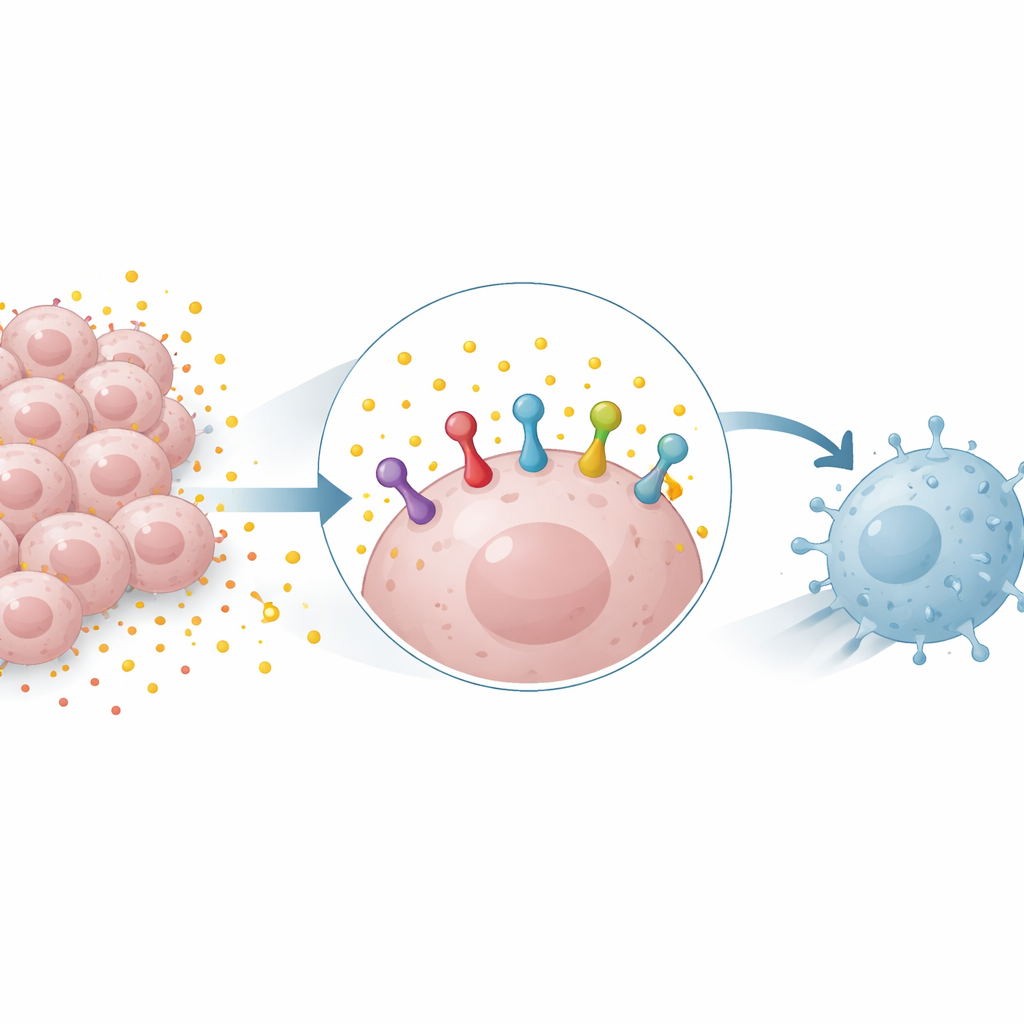
Un desperdicio de combustible que se vuelve arma
Muchos tumores dependen en gran medida de un proceso de combustión de azúcares llamado glucólisis, que genera grandes cantidades de lactato. Considerado durante mucho tiempo principalmente como un residuo metabólico, ahora se reconoce al lactato como una molécula señalizadora activa. Los investigadores encontraron que añadir lactato a células de cáncer de pulmón y de mama aumentaba la cantidad de proteína PD-L1, mientras que bloquear la glucólisis la reducía. Este efecto apareció tanto en células humanas como de ratón y podía ocurrir incluso cuando el lactato no aumentaba la actividad del gen PD-L1, lo que implica que el lactato estabilizaba la proteína PD-L1 ya existente en lugar de limitarse a activar su producción.
Una pequeña etiqueta química que protege a PD-L1
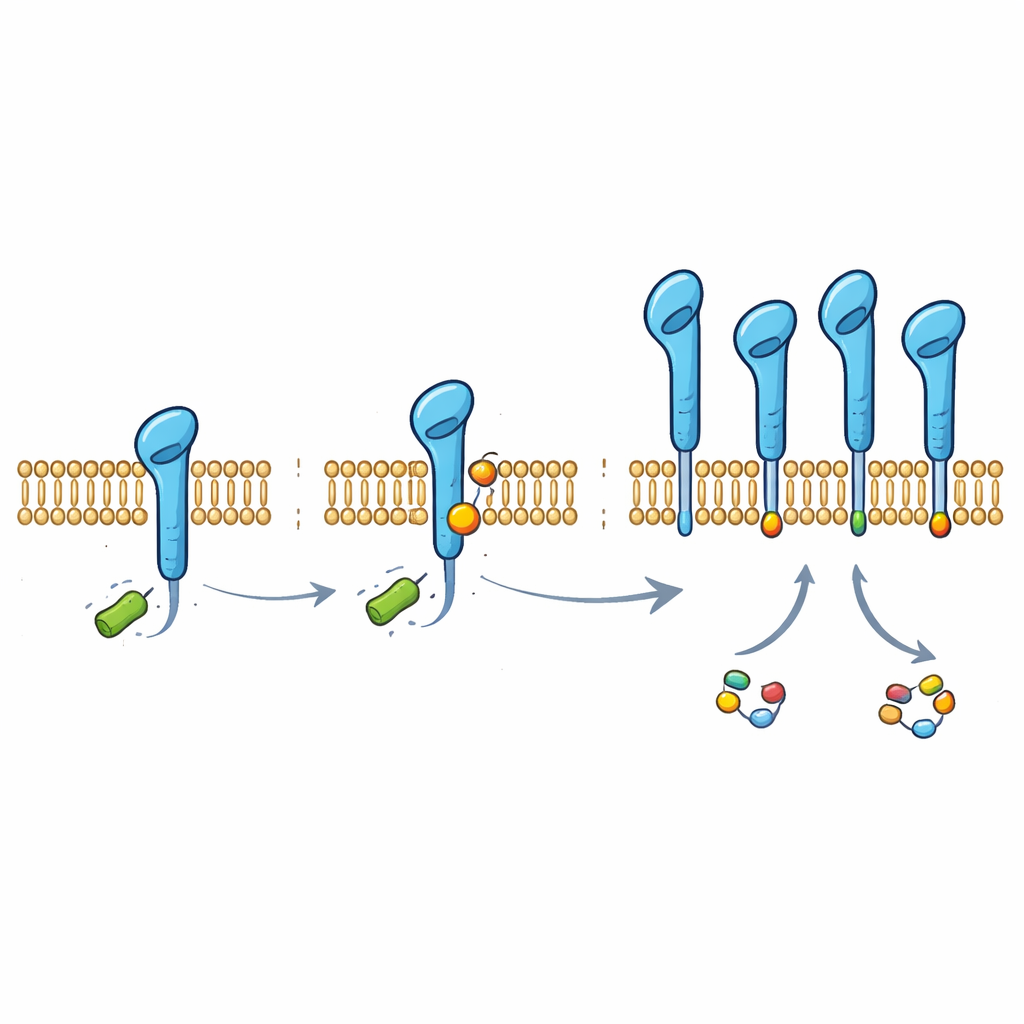
Al profundizar, el equipo descubrió que PD-L1 porta una pequeña etiqueta química derivada del lactato, unida a un bloque concreto de la proteína (una lisina en la posición 280). Esta etiqueta, llamada lactilación, se encontró en PD-L1 dentro de varias líneas celulares de cáncer de pulmón y en células normales de las vías respiratorias. Cuando los científicos mutaron esa única lisina para que no pudiera modificarse, PD-L1 perdió la mayor parte de su protección dependiente del lactato y se volvió más susceptible a la degradación. Normalmente, una maquinaria molecular llamada HUWE1 marca a PD-L1 para su eliminación añadiendo cadenas de otra pequeña molécula, ubiquitina, en una posición cercana. La nueva etiqueta basada en lactato interfiere físicamente con el acceso de HUWE1, impidiendo que se adhiera esta “etiqueta de desecho” y, de ese modo, protegiendo a PD-L1 de su degradación.
La enzima que escribe la etiqueta de lactato
Para entender cómo se añade esta etiqueta, los investigadores buscaron enzimas que pudieran usar directamente el lactato como donante. Identificaron a la alanyl‑ARNt sintetasa 1 (AARS1), una enzima habitual de la síntesis proteica, como la “escritora” clave de la lactilación de PD-L1. En experimentos in vitro y en células, AARS1 pudo unir un grupo lactato a la cola de PD-L1, mientras que una enzima relacionada, AARS2, no lo hizo. La sobreexpresión de AARS1 aumentó la etiqueta de lactato en PD-L1, redujo la unión de HUWE1 y el marcado con ubiquitina, y estabilizó la proteína del punto de control. Silenciar AARS1 tuvo el efecto contrario y anuló el impacto estabilizador del lactato, lo que indica que esta enzima es el eslabón crucial entre el metabolismo tumoral y la protección de PD-L1.
De los trucos celulares a oportunidades terapéuticas
Las consecuencias biológicas de esta química se probaron en ratones. Las células tumorales diseñadas para portar una versión de PD-L1 no lactilable fueron más fácilmente eliminadas por células CD8+ en cultivo y formaron tumores mucho más pequeños en animales, con mayor infiltración de estas células citotóxicas. Los autores exploraron después el lactato sódico (NaLa), una sal médica del lactato ya común en fluidos intravenosos. En modelos murinos de cáncer de pulmón, NaLa por sí solo no aceleró el crecimiento tumoral, pero cuando se combinó con terapia anti‑PD‑L1 potenció significativamente la capacidad del tratamiento para controlar los tumores e incrementó la presencia de células CD8+ en su interior. En muestras de pacientes con cáncer de pulmón, niveles más altos de PD-L1 con la etiqueta de lactato se asociaron con enfermedad más avanzada y peor supervivencia, lo que sugiere que esta modificación podría servir como biomarcador de tumores agresivos y, posiblemente, de respuesta a la inmunoterapia.
Qué supone esto para pacientes y terapias futuras
En conjunto, los hallazgos revelan una cadena de eventos directa: el metabolismo tumoral produce lactato; el lactato se usa para etiquetar PD-L1 en un único sitio; esta etiqueta bloquea la destrucción de la proteína y ayuda a los tumores a silenciar a las células T. Sin embargo, esa misma estabilización puede hacer que los tumores sean más sensibles a los fármacos dirigidos contra PD-L1. En términos prácticos, este trabajo propone la lactilación —y la enzima AARS1 que la impulsa— como nuevas palancas para ajustar la intensidad con que PD-L1 protege a las células cancerosas. Midiendo esta etiqueta en tumores de pacientes y diseñando tratamientos que la modulen, los clínicos podrían algún día predecir mejor quién se beneficiará de la inmunoterapia y combinar inhibidores del punto de control con intervenciones metabólicas para convertir el propio residuo energético del cáncer en una debilidad terapéutica.
Cita: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Palabras clave: PD-L1, lactato, inmunidad tumoral, modificación postraduccional, cáncer de pulmón no microcítico