Clear Sky Science · ru
Лактилювання стабилизирует PD-L1, способствуя уклонению опухоли от иммунитета и росту клеток
Почему эта история о раке важна
Иммунотерапия рака преобразила лечение многих пациентов, но лишь меньшинство получает длительную пользу. В этом исследовании обнаружен скрытый химический трюк, которым опухоли пользуются, чтобы защититься от иммунной системы — и предложен удивительно простой способ обратить этот трюк против самой опухоли. Показав, как обычный метаболит — лактат — помогает опухолям скрываться от киллерных Т‑клеток, работа указывает на новые стратегии, которые могут повысить эффективность существующих иммунотерапий и сделать их доступными для большего числа пациентов.
Как раковые клетки общаются с иммунной системой
Наша иммунная система опирается на молекулярные «рукопожатия» между клетками, чтобы решить, когда атаковать, а когда отступить. Одно из важнейших — взаимодействие белка на опухолевых клетках PD‑L1 и его партнёра PD‑1 на Т‑клетках. Когда PD‑L1 в избытке на раковых клетках, он приказывает Т‑клеткам отступить, позволяя опухоли расти без сопротивления. Препараты, блокирующие PD‑1 или PD‑L1, могут снять этот тормоз, но их успех часто зависит от того, сколько PD‑L1 демонстрирует опухоль. Поэтому понимание того, что контролирует уровни PD‑L1 на раковых клетках, имеет ключевое значение для прогнозирования и улучшения ответа на эти терапии.
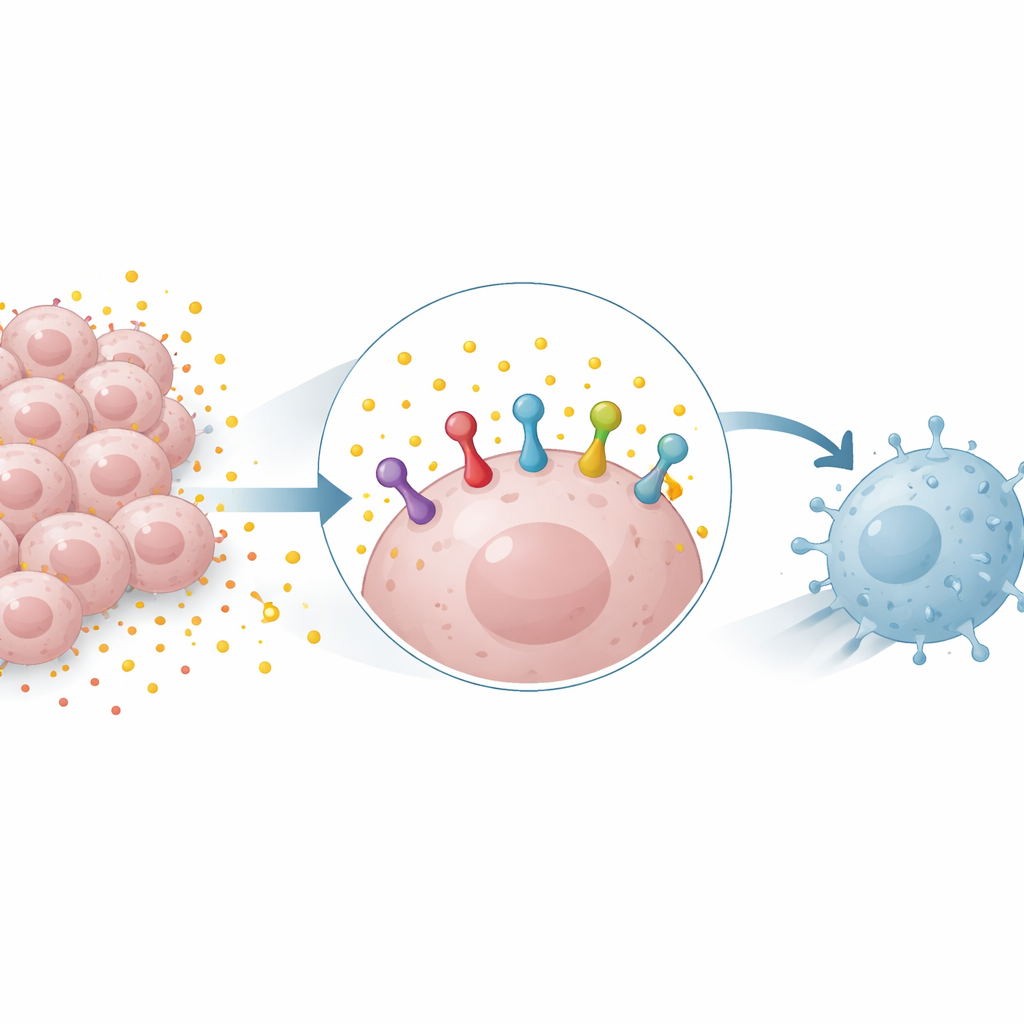
Отходы топлива, ставшие оружием
Многие опухоли сильно зависят от гликолиза — процесса расщепления сахара, в ходе которого образуется большое количество лактата. Долгое время лактат считали главным образом метаболическим отходом, но теперь его признают активным сигнальным молекулой. Исследователи обнаружили, что добавление лактата в культуры клеток легких и молочной железы повышало содержание белка PD‑L1, тогда как блокада гликолиза снижала его. Этот эффект проявлялся как в человеческих, так и в мышиных клетках и мог происходить даже тогда, когда лактат не повышал активность гена PD‑L1, что указывает на то, что лактат стабилизирует существующий белок PD‑L1, а не просто усиливает его синтез.
Крошечный химический ярлык, защищающий PD-L1
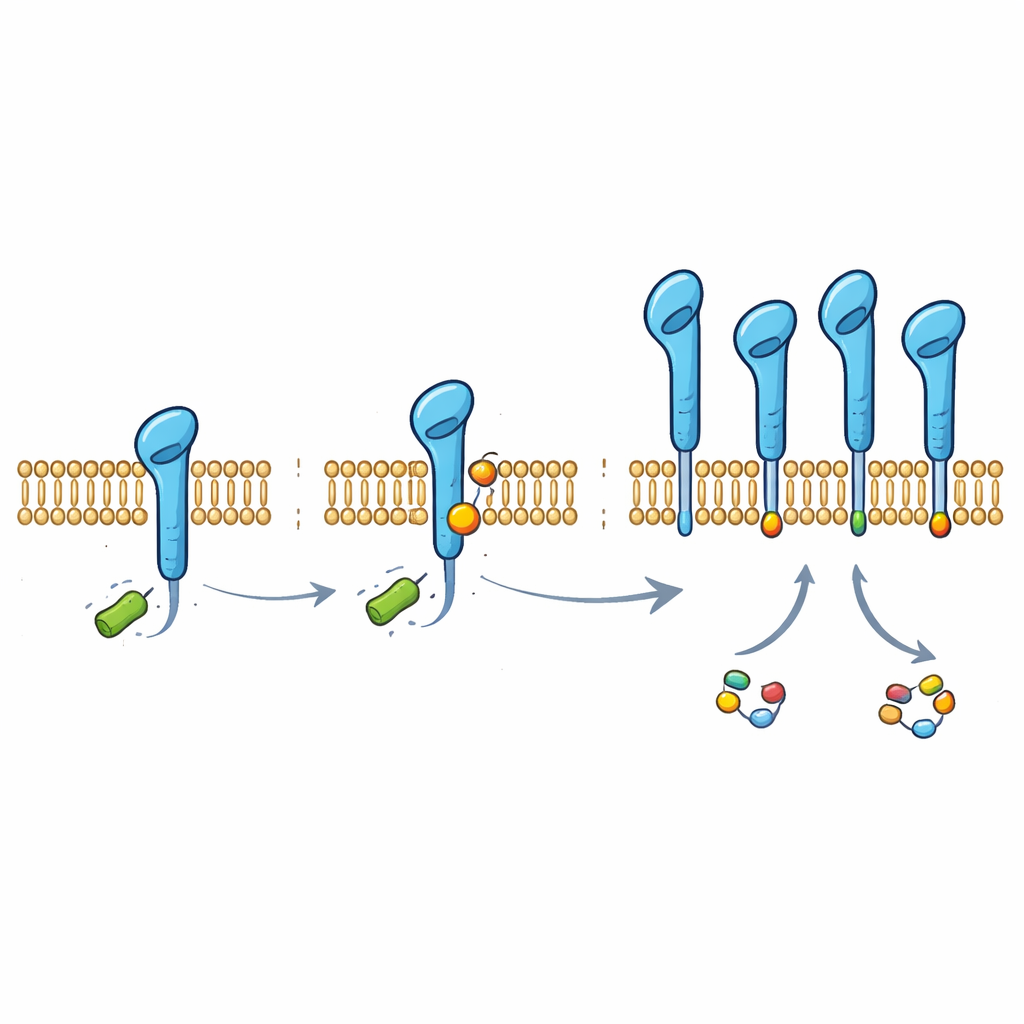
Углубившись, команда выяснила, что PD‑L1 несёт небольшой химический ярлык, происходящий от лактата, прикреплённый к одной конкретной аминокислоте белка (лизину на позиции 280). Этот ярлык, называемый лактилювання (лактилированием), обнаружили на PD‑L1 в нескольких линиях клеток рака легкого и в нормальных клетках дыхательных путей. Когда учёные изменили этот единичный лизин так, чтобы он больше не мог модифицироваться, PD‑L1 лишился большей части лактат‑зависимой защиты и стал легче поддаваться разрушению клеткой. В норме молекулярная «машина» HUWE1 помечает PD‑L1 для утилизации, присоединяя цепочки другого небольшого белка — убиквитина — в близкой позиции. Новый лактат‑основной ярлык физически мешает доступу HUWE1, предотвращая прикрепление этой «метки мусора» и тем самым оберегая PD‑L1 от распада.
Фермент, который пишет лактат‑ярлык
Чтобы понять, как этот ярлык добавляется, исследователи искали ферменты, способные использовать лактат прямо в качестве донора. Они выявили аланил‑тРНК синтетазу 1 (AARS1) — обычный фермент синтеза белка — как ключевого «писца» лактилювання PD‑L1. В пробирочных экспериментах и в клетках AARS1 мог прикреплять лактатную группу к хвосту PD‑L1, тогда как связанный фермент AARS2 этого не делал. Переэкспрессия AARS1 увеличивала количество лактат‑ярлыка на PD‑L1, снижала связывание HUWE1 и убиквитинирование и стабилизировала контрольную молекулу. Подавление AARS1 давало обратный эффект и сводило на нет стабилизирующее влияние лактата, что указывает на то, что этот фермент является важной связью между метаболизмом опухоли и защитой PD‑L1.
От клеточных уловок к терапевтическим возможностям
Биологические последствия этой химии проверяли на мышах. Опухолевые клетки, запрограммированные нести версию PD‑L1, не поддающуюся лактилюванню, легче убивались CD8+ Т‑клетками в культуре и формировали значительно меньшие опухоли у животных с более выраженной инфильтрацией этими киллерными клетками. Авторы также изучали натрий лактат (NaLa) — медицинскую соль лактата, уже широко используемую в инфузионных растворах. В моделях рака легкого у мышей NaLa сам по себе не ускорял рост опухолей, но в сочетании с терапией против PD‑L1 он значительно усиливал способность лечения контролировать опухоли и увеличивал присутствие CD8+ Т‑клеток в них. В образцах легочного рака пациентов более высокий уровень PD‑L1 с лактат‑ярлыком ассоциировался с более продвинутой стадией заболевания и худшей выживаемостью, что говорит о потенциальном использовании этой модификации как биомаркера агрессивных опухолей и, возможно, ответа на иммунотерапию.
Что это значит для пациентов и будущих терапий
В целом результаты выявляют прямую цепочку событий: метаболизм опухоли производит лактат; лактат используется для маркировки PD‑L1 в одной точке; этот ярлык блокирует разрушение белка и помогает опухолям заглушать Т‑клетки. Вместе с тем такая стабилизация может сделать опухоли более уязвимыми для препаратов, нацеленных на PD‑L1. Практически, работа предлагает лактилювання — и фермент AARS1, который его обеспечивает — как новые рычаги для регулирования того, насколько сильно PD‑L1 защищает раковые клетки. Измеряя этот ярлык в опухолях пациентов и разрабатывая подходы, которые его тонко корректируют, клиницисты в будущем, возможно, смогут точнее прогнозировать, кто получит пользу от иммунотерапии, и сочетать блокаторы контрольных точек с вмешательствами в метаболизм, превращая топливо‑отходы рака в терапевтическую слабость.
Цитирование: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Ключевые слова: PD-L1, молочная кислота, опухолевый иммунитет, посттрансляционная модификация, немелкоклеточный рак легкого