Clear Sky Science · it
La lattilazione stabilizza PD-L1 per favorire l’evasione immunitaria tumorale e la crescita cellulare
Perché questa storia sul cancro è importante
L’immunoterapia oncologica ha trasformato il trattamento per molti pazienti, ma solo una minoranza trae benefici duraturi. Questo studio mette in luce un trucco chimico nascosto che i tumori usano per proteggersi dal sistema immunitario—e suggerisce un modo sorprendentemente semplice per rivoltare quel trucco contro il cancro. Rivelando come un comune prodotto del metabolismo, il lattato, aiuti i tumori a nascondersi dalle cellule T citotossiche, il lavoro indica nuove strategie per rendere le terapie immunitarie attuali più efficaci e fruibili da più pazienti.
Come le cellule tumorali comunicano con il sistema immunitario
Il nostro sistema immunitario si affida a “stretti di mano” molecolari tra cellule per decidere quando attaccare e quando fermarsi. Uno dei più importanti è l’interazione tra una proteina sulle cellule tumorali chiamata PD-L1 e il suo partner PD-1 sulle cellule T. Quando PD-L1 è abbondante sulle cellule tumorali, segnala alle cellule T di ritirarsi, permettendo al tumore di crescere indisturbato. Farmaci che bloccano PD-1 o PD-L1 possono rimuovere questo freno, ma il loro successo dipende spesso da quanto PD-L1 il tumore espone. Capire cosa controlla i livelli di PD-L1 sulle cellule tumorali è quindi centrale per prevedere e migliorare la risposta a questi trattamenti.
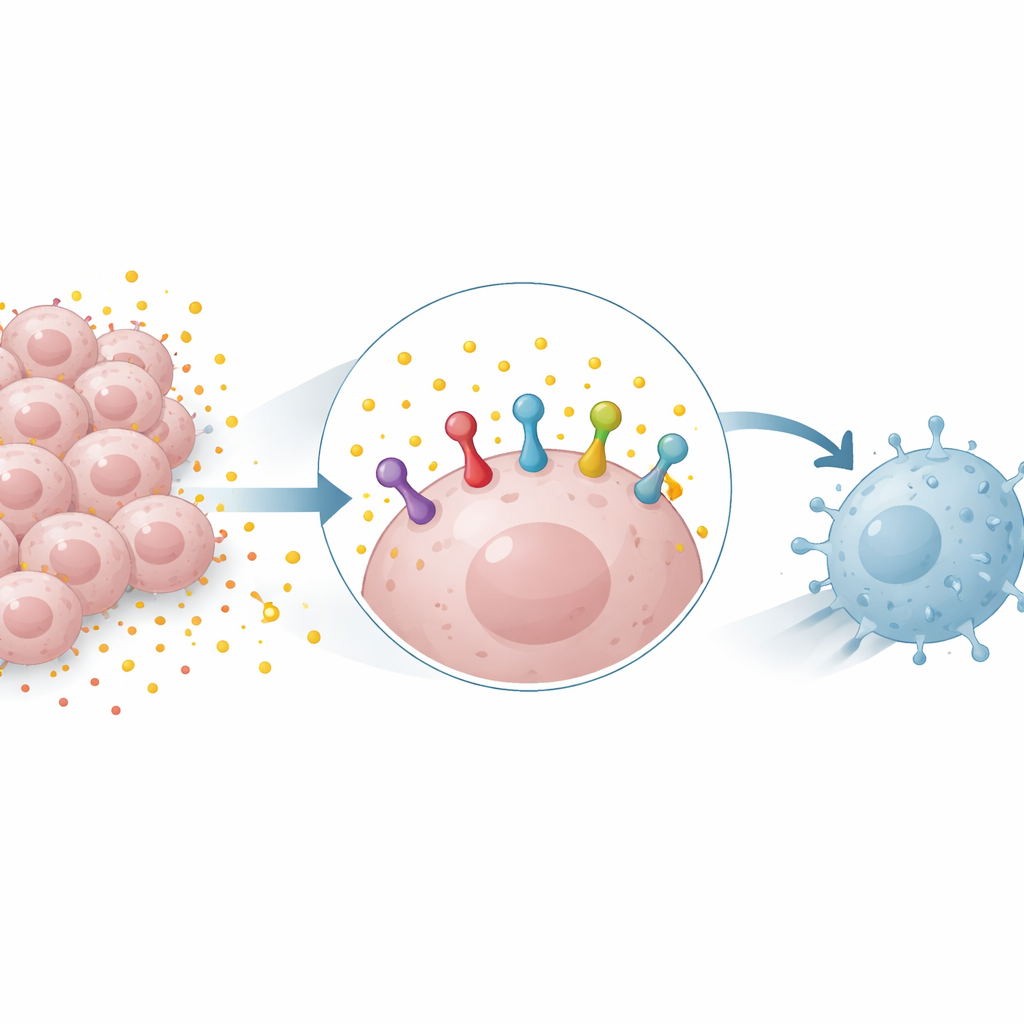
Un rifiuto energetico che diventa arma
Molti tumori dipendono in misura rilevante da un processo di combustione dello zucchero chiamato glicolisi, che produce grandi quantità di lattato. A lungo considerato soprattutto un rifiuto metabolico, il lattato è oggi riconosciuto come un attivo molecolare segnale. I ricercatori hanno scoperto che aggiungere lattato a cellule di tumore polmonare e mammario aumentava la quantità della proteina PD-L1, mentre bloccare la glicolisi la riduceva. Questo effetto è stato osservato sia in cellule umane sia murine e poteva verificarsi anche quando il lattato non aumentava l’attività genica di PD-L1, suggerendo che il lattato stabilizzava la proteina PD-L1 già presente piuttosto che limitarsi ad attivarne la produzione.
Un piccolo tag chimico che protegge PD-L1
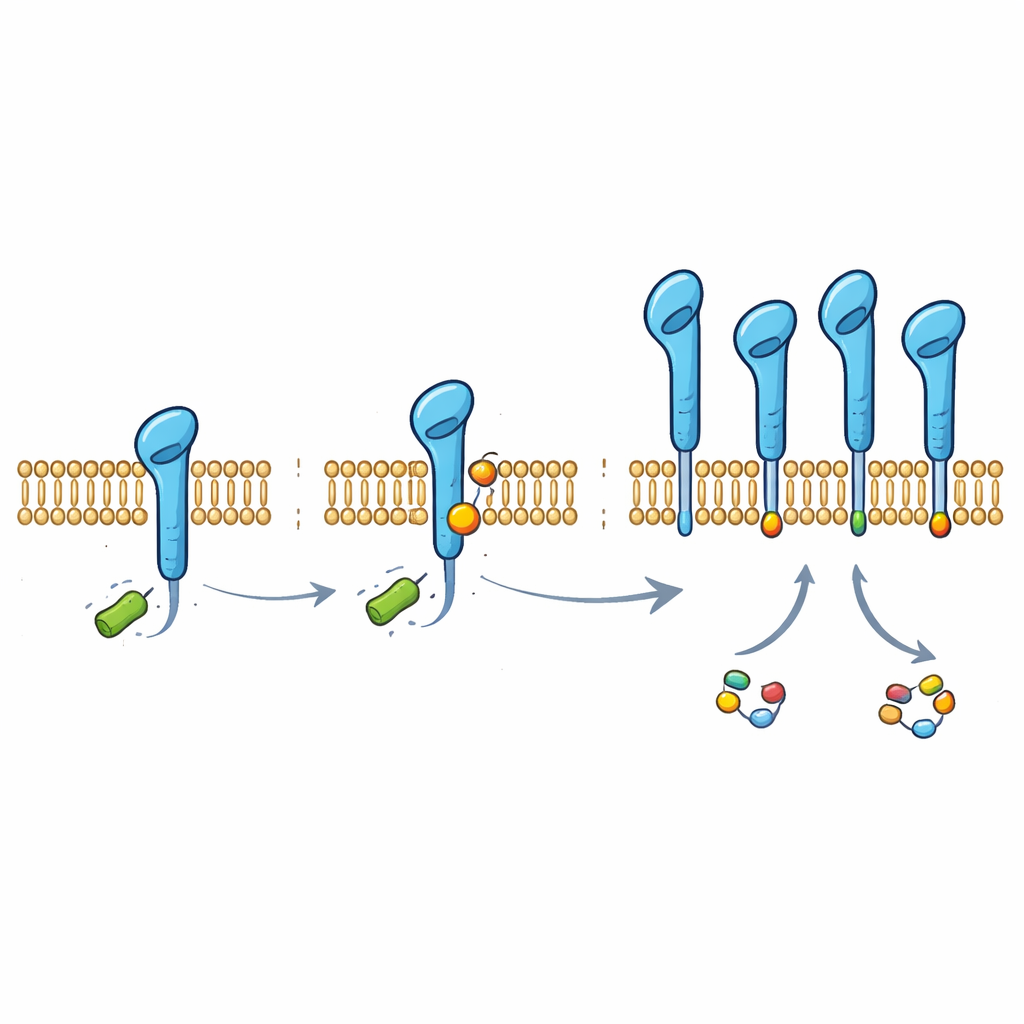
Approfondendo, il team ha scoperto che PD-L1 porta un piccolo tag chimico derivato dal lattato, attaccato a un particolare amminoacido della proteina (una lisina in posizione 280). Questo tag, chiamato lattilazione, è stato rilevato su PD-L1 in diverse linee cellulari di cancro polmonare e in cellule delle vie aeree normali. Quando gli scienziati hanno modificato quella singola lisina in modo che non potesse più essere alterata, PD-L1 ha perso gran parte della protezione dipendente dal lattato ed è diventata più facile da degradare per la cellula. Normalmente, una macchina molecolare chiamata HUWE1 marca PD-L1 per lo smaltimento aggiungendo catene di un’altra piccola molecola, l’ubiquitina, in una posizione vicina. Il nuovo tag a base di lattato interferisce fisicamente con l’accesso di HUWE1, impedendo l’apposizione di questa “etichetta di scarto” e proteggendo così PD-L1 dalla degradazione.
L’enzima che scrive il tag di lattato
Per capire come viene aggiunto questo tag, i ricercatori hanno cercato enzimi in grado di usare direttamente il lattato come donatore. Hanno identificato l’alanyl-tRNA sintetasi 1 (AARS1), un enzima normalmente coinvolto nella sintesi proteica, come il principale “scrittore” della lattilazione di PD-L1. In esperimenti in provetta e in cellule, AARS1 è stato in grado di attaccare un gruppo lattato alla coda di PD-L1, mentre un enzima correlato, AARS2, non poteva farlo. La sovraespressione di AARS1 aumentava il tag di lattato su PD-L1, riduceva il legame e il tagging con ubiquitina da parte di HUWE1 e stabilizzava la proteina checkpoint. Il silenziamento di AARS1 aveva l’effetto opposto e annullava l’impatto stabilizzante del lattato, indicando che questo enzima è il collegamento cruciale tra metabolismo tumorale e protezione di PD-L1.
Da trucchi cellulari a opportunità terapeutiche
Le conseguenze biologiche di questa chimica sono state testate nei topi. Cellule tumorali ingegnerizzate per esprimere una versione di PD-L1 non lattilabile venivano uccise più facilmente da cellule CD8+ in coltura e formavano tumori molto più piccoli negli animali, con maggiore infiltrazione di queste cellule citotossiche. Gli autori hanno quindi esplorato il lattato di sodio (NaLa), un sale di lattato usato in ambito medico e già comune nei fluidi endovena. Nei modelli murini di cancro polmonare, NaLa da solo non accelerava la crescita tumorale, ma se combinato con terapia anti-PD-L1 aumentava significativamente la capacità del trattamento di controllare i tumori e incrementava la presenza di cellule CD8+ al loro interno. In campioni di pazienti con cancro polmonare, livelli più elevati di PD-L1 portante il tag di lattato erano associati a malattia più avanzata e sopravvivenza peggiore, suggerendo che questa modifica potrebbe servire da biomarcatore per tumori aggressivi e, possibilmente, per la risposta all’immunoterapia.
Cosa significa per i pazienti e per le terapie future
Nel loro insieme, i risultati rivelano una catena diretta di eventi: il metabolismo tumorale produce lattato; il lattato viene usato per taggare PD-L1 in un singolo punto; questo tag blocca la distruzione della proteina e aiuta i tumori a silenziare le cellule T. Tuttavia, quella stessa stabilizzazione può rendere i tumori più visibili ai farmaci che mirano PD-L1. In termini pratici, questo lavoro propone la lattilazione—e l’enzima AARS1 che la promuove—come nuove leve per modulare quanto fortemente PD-L1 protegge le cellule cancerose. Misurando questo tag nei tumori dei pazienti e progettando trattamenti che lo modulino, i clinici potrebbero un giorno prevedere meglio chi beneficerà dell’immunoterapia e associare gli inibitori dei checkpoint a interventi metabolici per trasformare lo stesso rifiuto energetico del cancro in una vulnerabilità terapeutica.
Citazione: Liang, L., Zong, Y., Huang, J. et al. Lactylation stabilizes PD-L1 to promote tumor immune evasion and cell growth. Cell Death Dis 17, 335 (2026). https://doi.org/10.1038/s41419-026-08589-1
Parole chiave: PD-L1, lattato, immunità tumorale, modifica post-traduzionale, carcinoma polmonare non a piccole cellule