Clear Sky Science · zh
与癌症相关的 SF3B1 突变通过破坏核内肌动蛋白网络的组织抑制 DNA 修复
细胞如何维护 DNA 的完整性
我们的细胞内的 DNA 每天都会因辐射、化学物质和正常代谢而受到划伤、断裂和应力。健康细胞通常能够很有效地修补这些损伤。但在许多癌症中,这一修复系统部分失灵。这项研究揭示了一个令人惊讶的新原因:剪接蛋白上的单一常见突变破坏了细胞核内部的支撑网络,减缓了 DNA 修复并助长了癌症的生长。
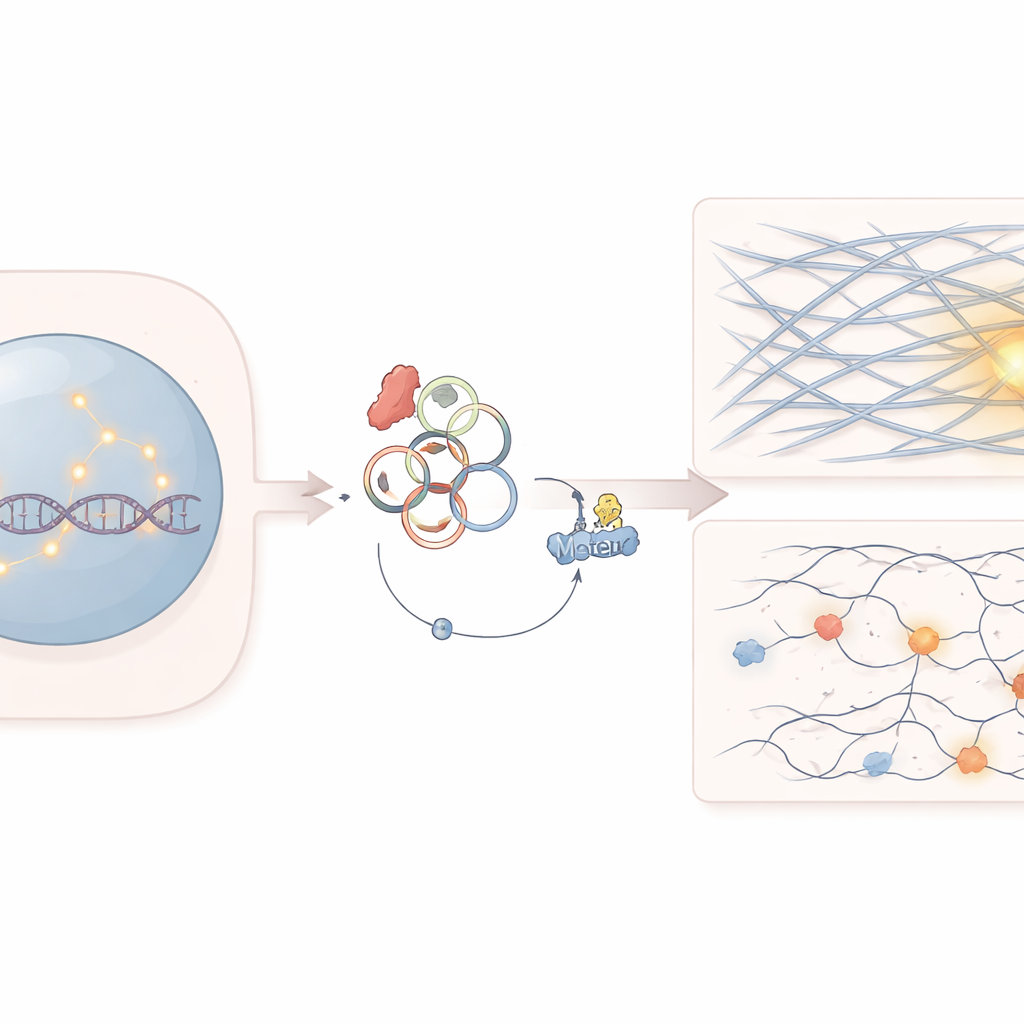
隐藏在癌细胞中的薄弱环节
这项工作聚焦于名为 SF3B1 的基因,它参与细胞中 RNA 信息的加工。SF3B1 的突变在几种血液癌和实体瘤中很常见。医生早已知道这些突变使癌细胞对某些针对 DNA 修复的药物(如 PARP 抑制剂)异常敏感。然而,为什么这些细胞在修复断裂的 DNA 时会出现困难,尤其是基因组高度致密区域中产生的那些更难修复的断裂,尚未完全明了。
环状 RNA 与马达蛋白的作用
研究人员发现,SF3B1 突变改变了某些 RNA 分子的拼接方式,增加了名为 circATP9B 的环状 RNA 的产生。与典型的线性 RNA 不同,环状 RNA 形成闭合环,可作为蛋白的“海绵”或诱饵。在这里,circATP9B 与一种名为 MYH9 的马达蛋白结合,MYH9 通常帮助组织肌动蛋白丝——这些结构性纤维因塑造细胞形态和驱动肌肉收缩而更为人所知。研究组表明,circATP9B 促使 MYH9 被标记并分解,降低了其蛋白水平,而并未改变其基因表达。
破坏核内的“道路网络”
在细胞核内,肌动蛋白可以组装成细细的丝状结构,像轨道一样。DNA 受损后,尤其是在紧密包装的“异染色质”中的断片,必须沿这些轨道移动到可以进行精确修复的安全区域。借助活细胞成像,科学家观察到标记 DNA 断裂和核内肌动蛋白的荧光标记。当 MYH9 水平降低时,辐射后通常丰富的核内肌动蛋白丝网络无法正常形成。结果,受损 DNA 位点移动更慢、行程更短、聚集效率降低,尤其影响依赖拷贝完整 DNA 作为模板的修复路径。这些迟缓且孤立的断裂在许多小时内未能解决。
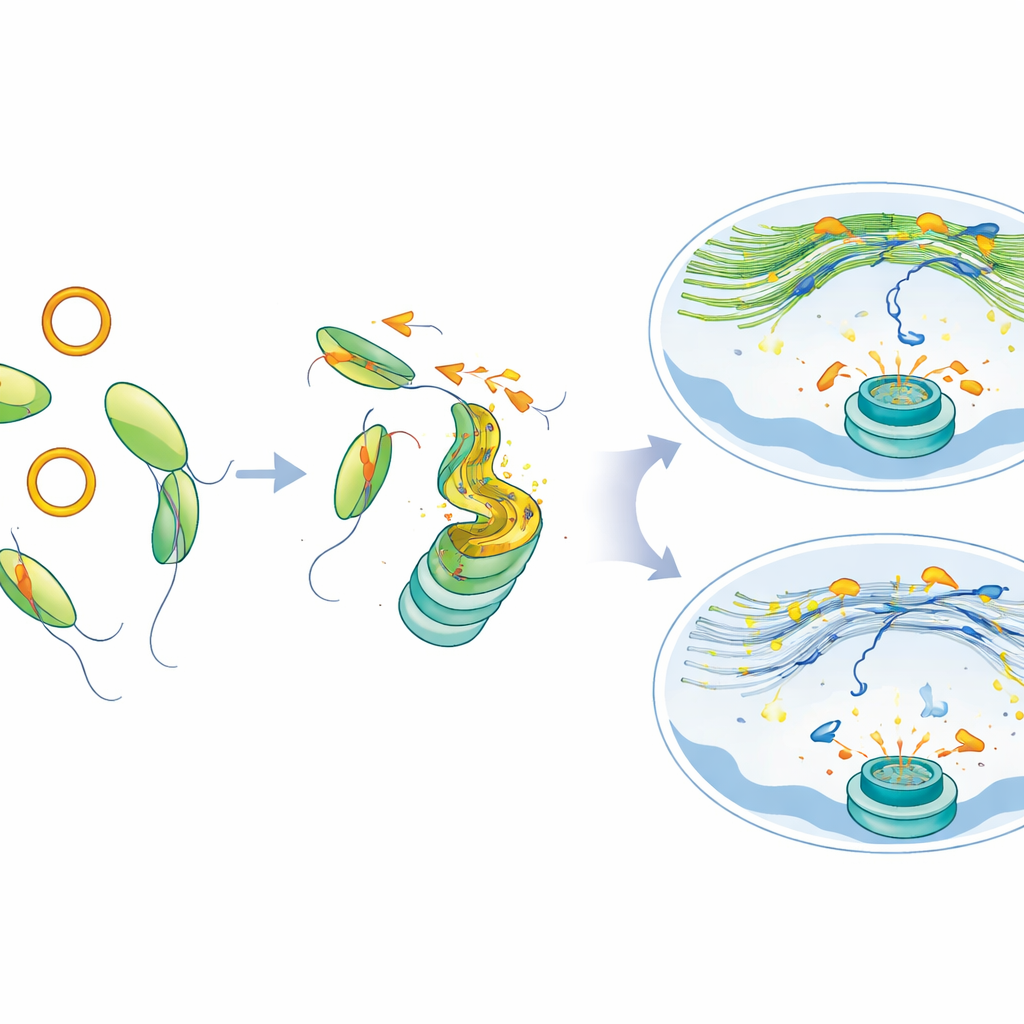
从修复失常到治疗机会
缺乏 MYH9 的细胞,或被迫大量产生 circATP9B 的细胞,累积持续的损伤标记和微小的额外细胞核——这些都是染色体断裂的迹象。这些细胞在培养皿和小鼠肿瘤模型中对 PARP 抑制剂也变得更脆弱,表明干扰该通路会使癌细胞在使用 DNA 修复药物时特别暴露。重要的是,当研究者恢复 MYH9 或降低 circATP9B 时,核内肌动蛋白网络得以恢复,DNA 断裂的移动和聚集趋于正常,即便在携带 SF3B1 突变的细胞中,修复也有所改善。
对患者意味着什么
简而言之,这项研究揭示了一种常见的癌症突变如何破坏细胞内部用于 DNA 修复的“铁路系统”。SF3B1 突变增强了一种环状 RNA——circATP9B,进而促使负责组织核内肌动蛋白轨道的 MYH9 马达蛋白被破坏。没有坚固的轨道,受损的 DNA 无法被高效地聚集和修复,这既让癌细胞基因组不稳定,也使它们更依赖剩余的修复途径。这一脆弱性有助于解释为何带有 SF3B1 突变的肿瘤对 PARP 抑制剂反应良好,并提示测量或针对 circATP9B 与 MYH9 未来可能有助于为癌症患者定制 DNA 损伤疗法。
引用: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
关键词: DNA 修复, 环状 RNA, 核内肌动蛋白, SF3B1 突变, 癌症治疗