Clear Sky Science · it
La mutazione SF3B1 associata al cancro sopprime la riparazione del DNA alterando l’organizzazione della rete di actina nucleare
Come le cellule mantengono il DNA in forma
Ogni giorno, il DNA nelle nostre cellule viene scheggiato, tagliato e sollecitato da radiazioni, sostanze chimiche e dal normale metabolismo. Le cellule sane sono in genere molto efficaci nel riparare questi danni. Ma in molti tumori quel sistema di riparazione è parzialmente compromesso. Questo studio mette in luce una nuova e sorprendente ragione: una singola e comune mutazione in una proteina del splicing manda fuori strada una rete di supporto interna nel nucleo cellulare, rallentando la riparazione del DNA e favorendo la crescita del cancro.
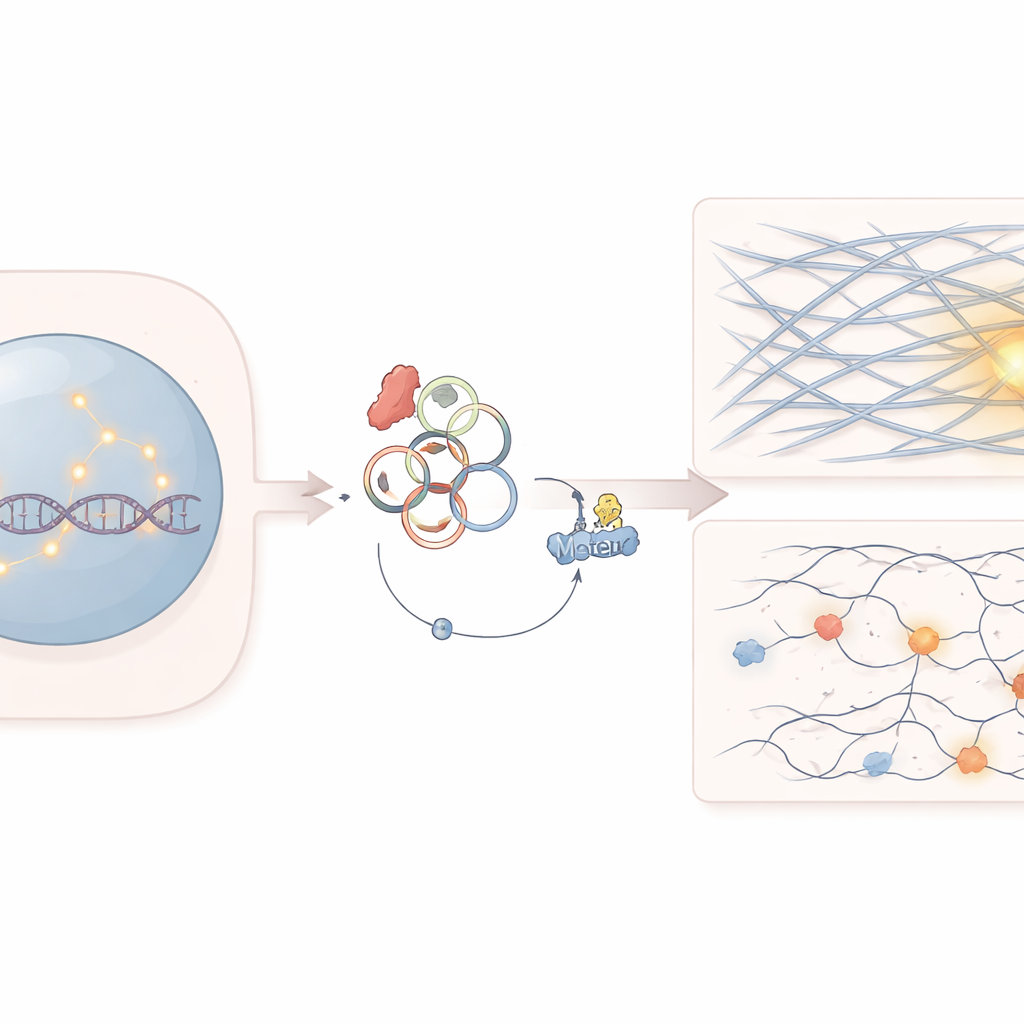
Un punto debole nascosto nelle cellule tumorali
Il lavoro si concentra su un gene chiamato SF3B1, che aiuta a processare i messaggi di RNA nelle cellule. Le mutazioni in SF3B1 sono comuni in diversi tumori del sangue e in tumori solidi. I medici sapevano già che queste mutazioni rendono le cellule tumorali particolarmente sensibili a certi farmaci che colpiscono la riparazione del DNA, come gli inibitori di PARP. Tuttavia non era del tutto chiaro perché queste cellule incontrino difficoltà nel riparare le rotture del DNA, in particolare quelle più difficili da correggere che si formano in regioni densamente impacchettate del genoma.
Il ruolo dell’RNA circolare e di una proteina motrice
I ricercatori hanno scoperto che la mutazione di SF3B1 altera il modo in cui alcuni RNA vengono cuciti insieme, aumentando la produzione di un RNA circolare chiamato circATP9B. A differenza degli RNA lineari tipici, gli RNA circolari formano anelli chiusi e possono agire da spugne o esche per le proteine. In questo caso, circATP9B si lega a una proteina motrice chiamata MYH9, che normalmente contribuisce a organizzare i filamenti di actina—lo stesso tipo di fibre strutturali note per dare forma alle cellule e alimentare la contrazione muscolare. Il gruppo ha mostrato che circATP9B favorisce il marchio e la degradazione di MYH9, riducendone i livelli senza modificare l’espressione genica.
La rottura della rete stradale nucleare
All’interno del nucleo, l’actina può assemblarsi in filamenti sottili che funzionano come binari. Dopo che il DNA è danneggiato, i pezzi rotti, specialmente nella «eterocromatina» densamente impacchettata, devono muoversi lungo questi binari verso zone più sicure dove può avvenire una riparazione accurata. Usando immagini in cellule vive, gli scienziati hanno osservato marcatori fluorescenti che evidenziano le rotture del DNA e l’actina nucleare. Quando MYH9 veniva ridotto, la solita fitta rete di filamenti di actina nucleare non riusciva a formarsi correttamente dopo le radiazioni. Di conseguenza, i punti di DNA danneggiato si muovevano più lentamente, percorrevano distanze minori e si raggruppavano meno efficacemente, soprattutto per la via di riparazione che si basa sul copiare DNA integro come modello. Queste rotture lente e isolate restavano irrisolte per molte ore.
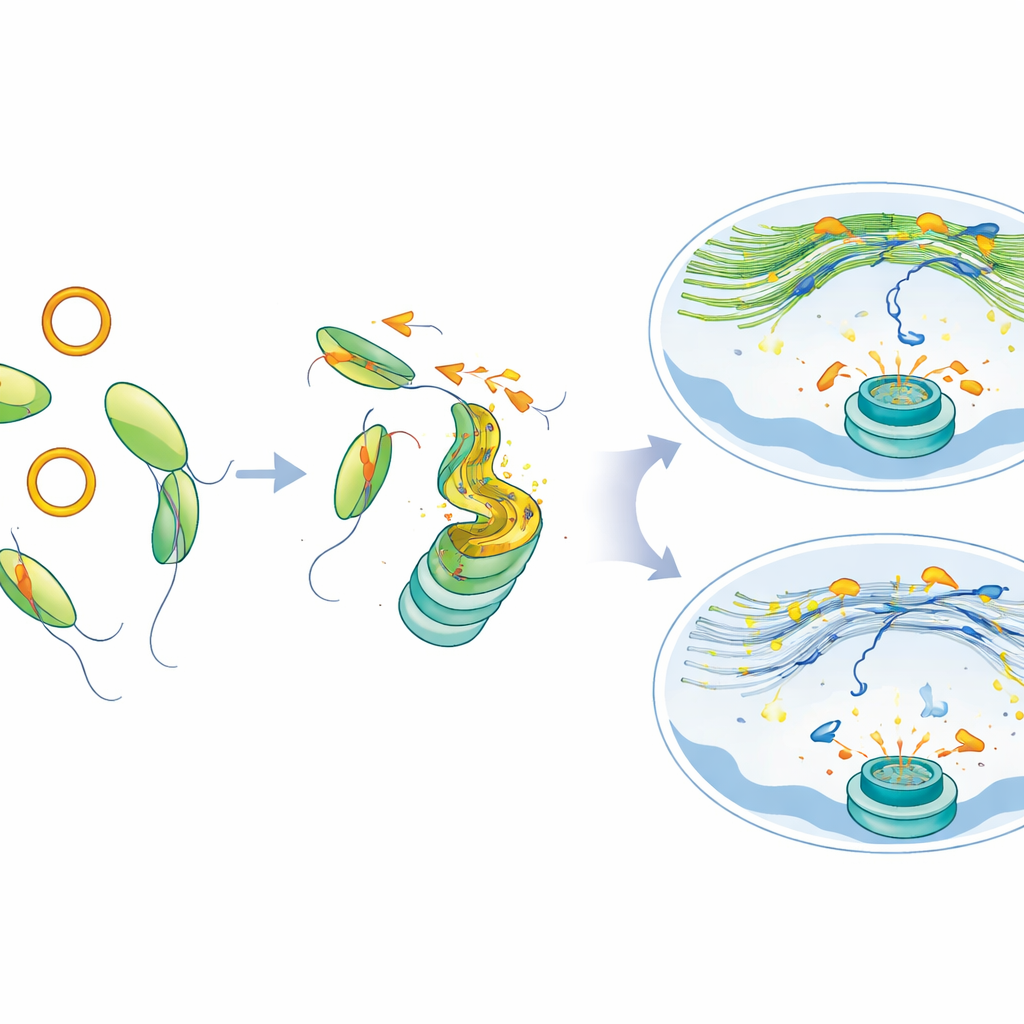
Dalla riparazione difettosa a un’opportunità terapeutica
Le cellule prive di MYH9, o che venivano indotte a produrre quantità eccessive di circATP9B, accumulate segni persistenti di danno e piccoli nuclei aggiuntivi—segni di cromosomi che si frammentano. Queste cellule diventavano anche più vulnerabili agli inibitori di PARP, sia in colture cellulari sia in modelli tumorali murini, il che significa che interferire con questo percorso lascia le cellule tumorali particolarmente esposte quando si utilizzano farmaci che colpiscono la riparazione del DNA. Importante, quando i ricercatori hanno ripristinato MYH9 o ridotto circATP9B, la rete di actina nucleare si è riavviata, le rotture del DNA si sono mosse e raggruppate più normalmente e la riparazione è migliorata anche nelle cellule portatrici della mutazione SF3B1.
Cosa significa per i pazienti
In termini semplici, questo studio rivela che una mutazione comune nel cancro può sabotare il «sistema ferroviario» interno della cellula per la riparazione del DNA. La mutazione SF3B1 aumenta un RNA circolare, circATP9B, che a sua volta porta alla distruzione della proteina motrice MYH9 che aiuta a organizzare i binari di actina nel nucleo. Senza binari stabili, il DNA rotto non può essere efficacemente raccolto e riparato, lasciando le cellule tumorali geneticamente instabili ma anche più dipendenti dalle vie di riparazione rimaste. Questa vulnerabilità aiuta a spiegare perché i tumori con mutazioni SF3B1 rispondono bene agli inibitori di PARP e suggerisce che misurare o mirare a circATP9B e MYH9 potrebbe un giorno aiutare a personalizzare le terapie che danneggiano il DNA per i pazienti oncologici.
Citazione: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Parole chiave: Riparazione del DNA, RNA circolare, actina nucleare, mutazione SF3B1, terapia del cancro