Clear Sky Science · pl
Mutacja SF3B1 związana z rakiem hamuje naprawę DNA przez zakłócenie organizacji sieci aktyny jądrowej
Jak komórki dbają o kształt DNA
Codziennie DNA w naszych komórkach ulega nacięciom, pęknięciom i uszkodzeniom wywołanym promieniowaniem, chemikaliami oraz normalnym metabolizmem. Zdrowe komórki zwykle bardzo skutecznie naprawiają te uszkodzenia. Jednak w wielu nowotworach ten system naprawczy jest częściowo zaburzony. Badanie to ujawnia zaskakujący, nowy powód tego stanu: pojedyncza, powszechna mutacja w białku zaangażowanym w składanie RNA destabilizuje wewnętrzną sieć wspierającą wewnątrz jądra komórkowego, spowalniając naprawę DNA i sprzyjając rozwojowi nowotworu.
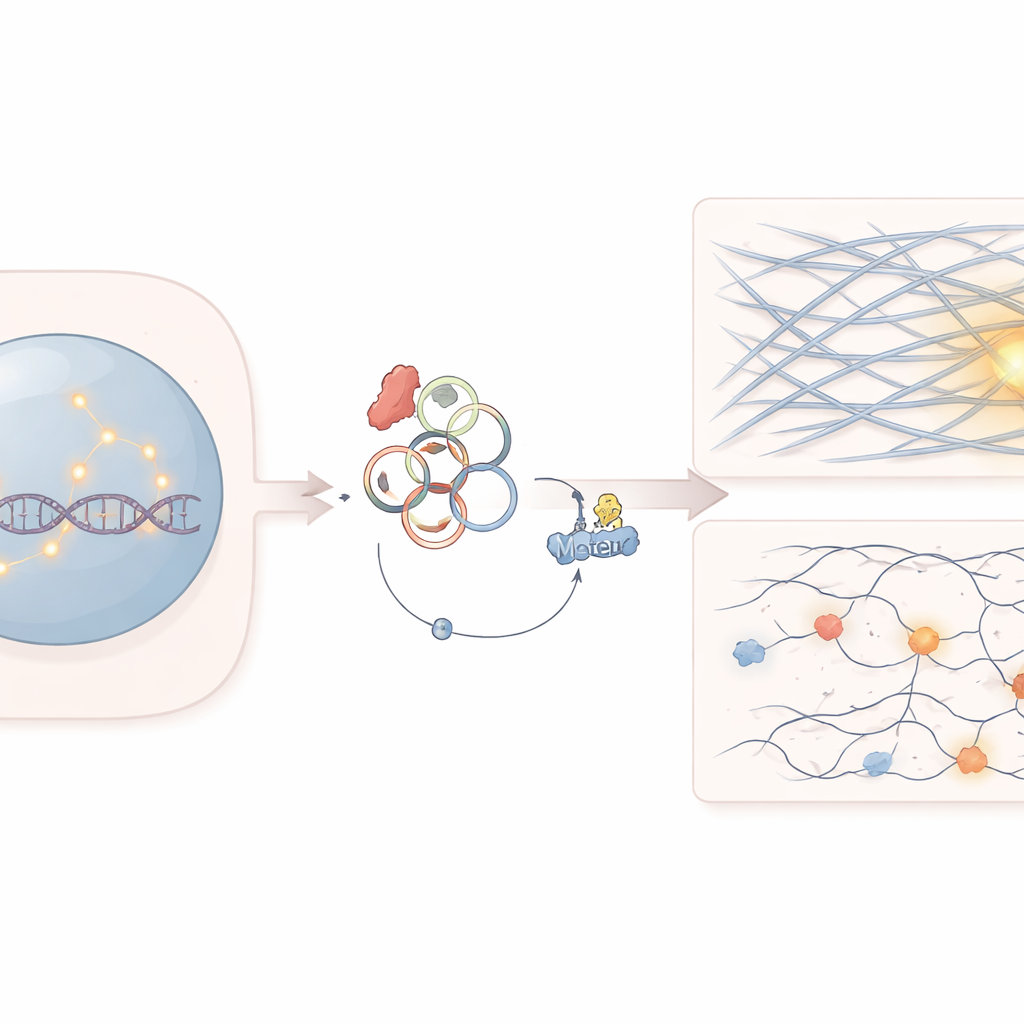
Ukryty słaby punkt komórek nowotworowych
Prace koncentrują się na genie SF3B1, który uczestniczy w przetwarzaniu komunikatów RNA w komórkach. Mutacje w SF3B1 są częste w kilku nowotworach krwi i guzach litych. Lekarze wiedzieli już, że te mutacje czynią komórki nowotworowe wyjątkowo wrażliwymi na niektóre leki celujące w naprawę DNA, takie jak inhibitory PARP. Jednak dlaczego komórkom tym trudniej jest naprawiać zerwane nici DNA, szczególnie trudniejsze do naprawienia pęknięcia powstające w gęsto upakowanych rejonach genomu, nie było w pełni wyjaśnione.
Rola RNA kołowego i białka motorowego
Naukowcy odkryli, że mutacja SF3B1 zmienia sposób łączenia niektórych cząsteczek RNA, zwiększając produkcję RNA kołowego o nazwie circATP9B. W przeciwieństwie do typowego liniowego RNA, RNA kołowe tworzą zamknięte pętle i mogą działać jak gąbki lub przynęty dla białek. W tym przypadku circATP9B wiąże się z białkiem motorowym o nazwie MYH9, które zwykle pomaga organizować filamenty aktynowe — te same włókna strukturalne znane z nadawania kształtu komórkom i napędzania skurczu mięśni. Zespół wykazał, że circATP9B sprzyja znakowaniu MYH9 do degradacji, zmniejszając jego poziomy bez zmiany ekspresji genu.
Zakłócenie „kolejowej” sieci jądrowej
W jądrze aktyna może polimeryzować w cienkie filamenty pełniące rolę torów. Po uszkodzeniu DNA oderwane fragmenty, zwłaszcza w ściśle upakowanej „heterochromatynie”, muszą przemieszczać się po tych torach do bezpieczniejszych stref, gdzie możliwa jest dokładna naprawa. Przy użyciu obrazowania komórek na żywo naukowcy obserwowali świecące markery uwidaczniające przerwy w DNA i aktynę jądrową. Gdy poziom MYH9 został obniżony, zwykle gęsta sieć filamentów aktynowych w jądrze nie tworzyła się prawidłowo po naświetleniu. W rezultacie miejsca pęknięć DNA poruszały się wolniej, przebywały krótsze dystanse i rzadziej grupowały się efektywnie, szczególnie w ścieżce naprawy bazującej na kopiowaniu nieuszkodzonego DNA jako matrycy. Te spowolnione, odizolowane uszkodzenia pozostawały nierozwiązane przez wiele godzin.
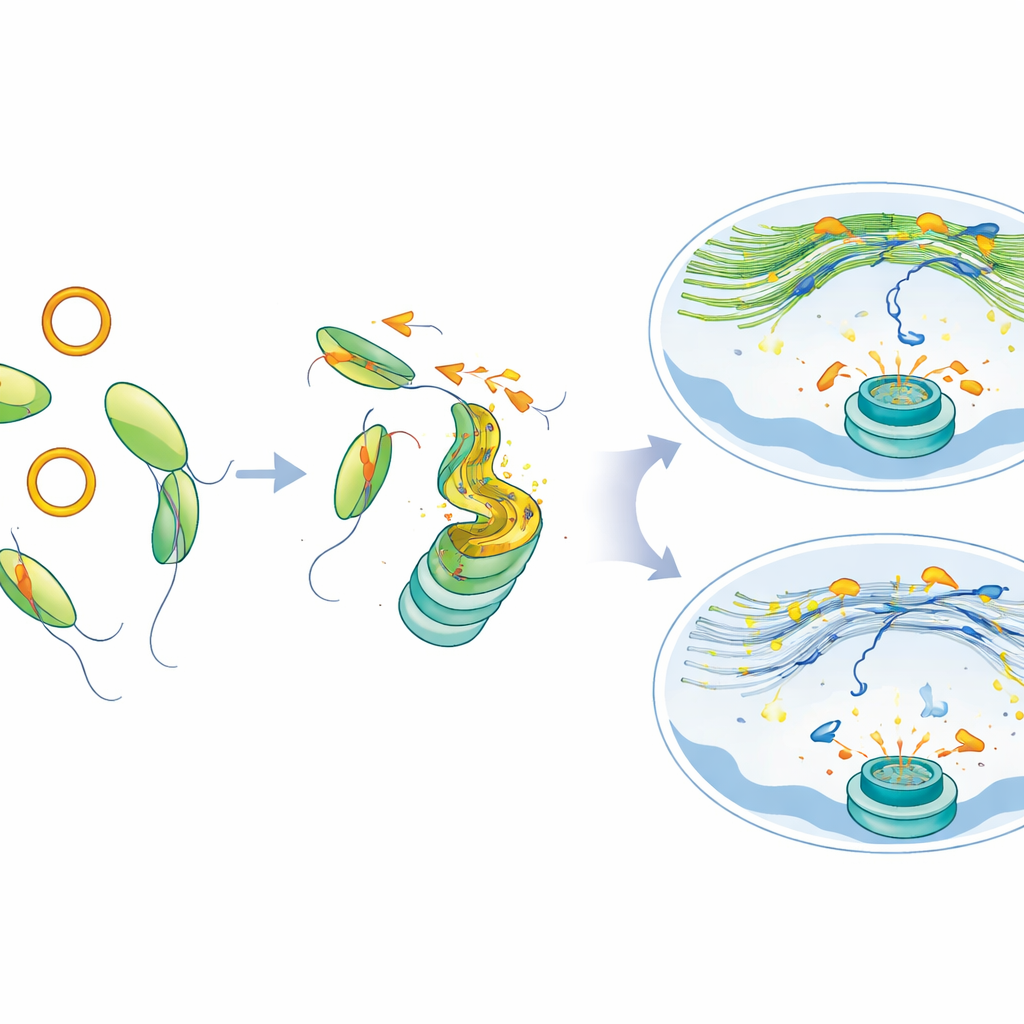
Od wadliwej naprawy do możliwości terapeutycznej
Komórki pozbawione MYH9 lub komórki zmuszone do produkcji nadmiaru circATP9B gromadziły trwałe markery uszkodzeń i drobne dodatkowe jądra — oznaki rozpadu chromosomów. Komórki te stały się także bardziej wrażliwe na inhibitory PARP, zarówno w hodowlach komórkowych, jak i w modelach nowotworowych u myszy, co oznacza, że zakłócenie tej ścieżki pozostawia komórki nowotworowe szczególnie odsłonięte podczas stosowania leków hamujących naprawę DNA. Co ważne, gdy badacze przywrócili MYH9 lub zredukowali circATP9B, sieć aktyny jądrowej odzyskała funkcję, przerwy w DNA poruszały się i grupowały bardziej normalnie, a naprawa poprawiła się nawet w komórkach z mutacją SF3B1.
Co to oznacza dla pacjentów
W prostych słowach, to badanie pokazuje, że powszechna mutacja nowotworowa może sabotować wewnętrzny „system kolejowy” komórki odpowiedzialny za naprawę DNA. Mutacja SF3B1 zwiększa poziom RNA kołowego circATP9B, który z kolei niszczy białko motorowe MYH9 pomagające organizować tory z aktyny w jądrze. Bez stabilnych torów uszkodzone fragmenty DNA nie mogą być efektywnie zbliżane i naprawiane, co pozostawia komórki nowotworowe genetycznie niestabilne, ale też bardziej zależne od pozostałych szlaków naprawczych. Ta słabość pomaga wyjaśnić, dlaczego guzy z mutacjami SF3B1 dobrze reagują na inhibitory PARP, i sugeruje, że mierzenie lub celowanie w circATP9B i MYH9 mogłoby w przyszłości pomóc dobierać terapie uszkadzające DNA dla pacjentów z rakiem.
Cytowanie: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Słowa kluczowe: Naprawa DNA, RNA kołowy, aktyna jądrowa, mutacja SF3B1, terapia przeciwnowotworowa