Clear Sky Science · ru
Ассоциированная с раком мутация SF3B1 угнетает ремонт ДНК, нарушая организацию сети ядерного актина
Как клетки сохраняют форму своей ДНК
Каждый день ДНК в наших клетках подвергается надрезам, разрывам и стрессу от излучения, химических веществ и нормального метаболизма. Здоровые клетки обычно очень хорошо восстанавливают такие повреждения. Но во многих случаях при раке эта система ремонта частично нарушена. В этом исследовании обнаружена неожиданная новая причина: одна распространённая мутация в белке сплайсинга срывает внутреннюю опорную сеть внутри ядра клетки, замедляя ремонт ДНК и способствуя росту опухоли.
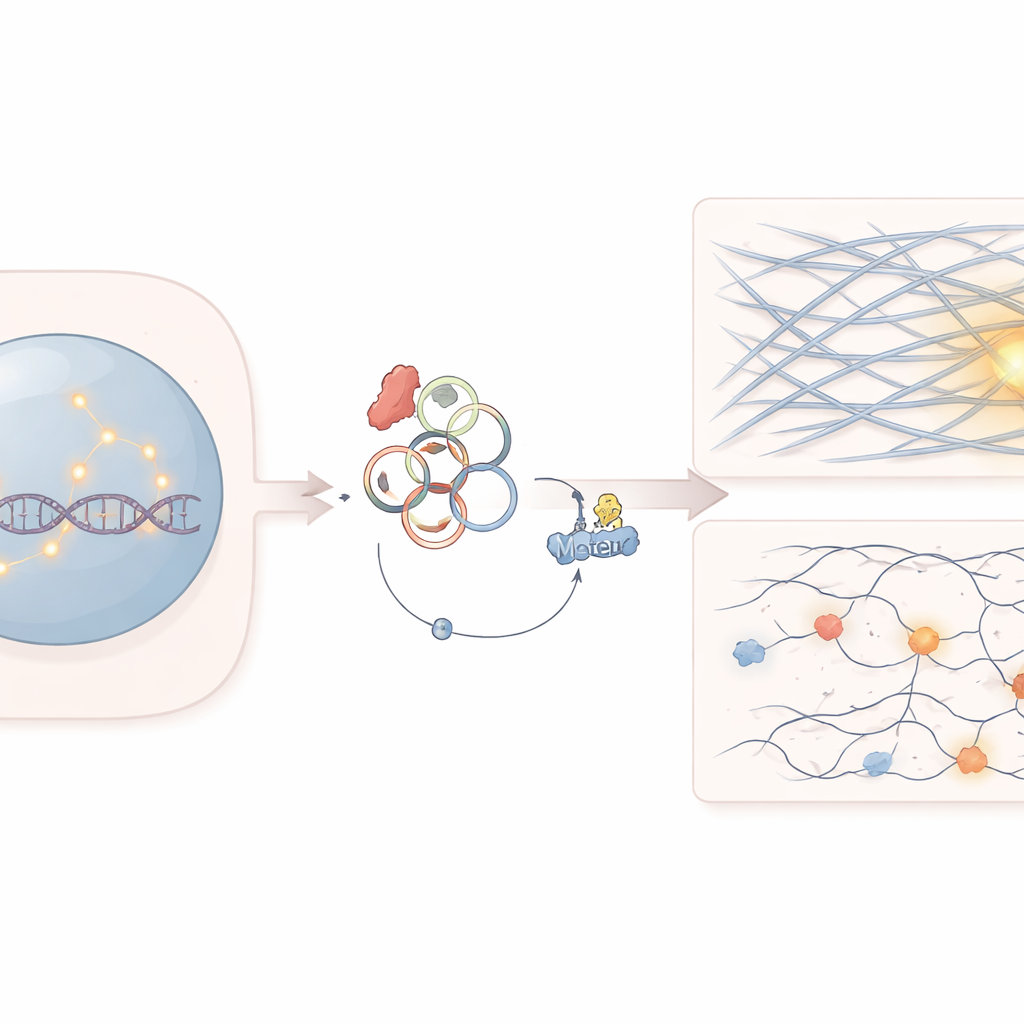
Скрытая уязвимость в раковых клетках
Работа сосредоточена на гене SF3B1, который участвует в обработке РНК-сообщений в клетках. Мутации в SF3B1 часто встречаются при нескольких кроветворных и солидных опухолях. Врачи уже знали, что эти мутации делают раковые клетки особенно чувствительными к некоторым препаратам, нацеленным на ремонт ДНК, например ингибиторам PARP. Однако причина, по которой этим клеткам трудно ремонтировать разрывы ДНК, особенно те, что возникают в плотно упакованных участках генома, была понята не полностью.
Роль круговой РНК и моторного белка
Исследователи обнаружили, что мутация SF3B1 меняет способ склеивания некоторых молекул РНК, увеличивая продукцию круговой РНК под названием circATP9B. В отличие от обычной линейной РНК, круговые РНК образуют замкнутые петли и могут действовать как губки или приманки для белков. В данном случае circATP9B связывается с моторным белком MYH9, который обычно помогает организовывать актиновые нити — те самые структурные волокна, известные формированием формы клеток и обеспечением сокращения мышц. Команда показала, что circATP9B способствует пометке MYH9 для разрушения и его деградации, снижая уровень белка без изменения экспрессии гена.
Разрыв ядерной «дорожной сети»
Внутри ядра актин может собираться в тонкие филаменты, которые действуют как рельсы. После повреждения ДНК фрагменты, особенно в плотно упакованном «гетерохроматине», должны перемещаться по этим путям в более безопасные зоны, где может произойти точный ремонт. С помощью живой визуализации учёные наблюдали светящиеся маркеры, которые выделяют разрывы ДНК и ядерный актин. При снижении уровня MYH9 обычно плотная сеть ядерных актиновых филаментов не формировалась должным образом после облучения. В результате повреждённые участки ДНК двигались медленнее, проходили меньшие расстояния и реже образовывали кластеры, особенно в случае пути ремедиации, основанного на копировании неповреждённой молекулы ДНК как шаблона. Эти вялые, изолированные разрывы оставались нерешёнными в течение многих часов.
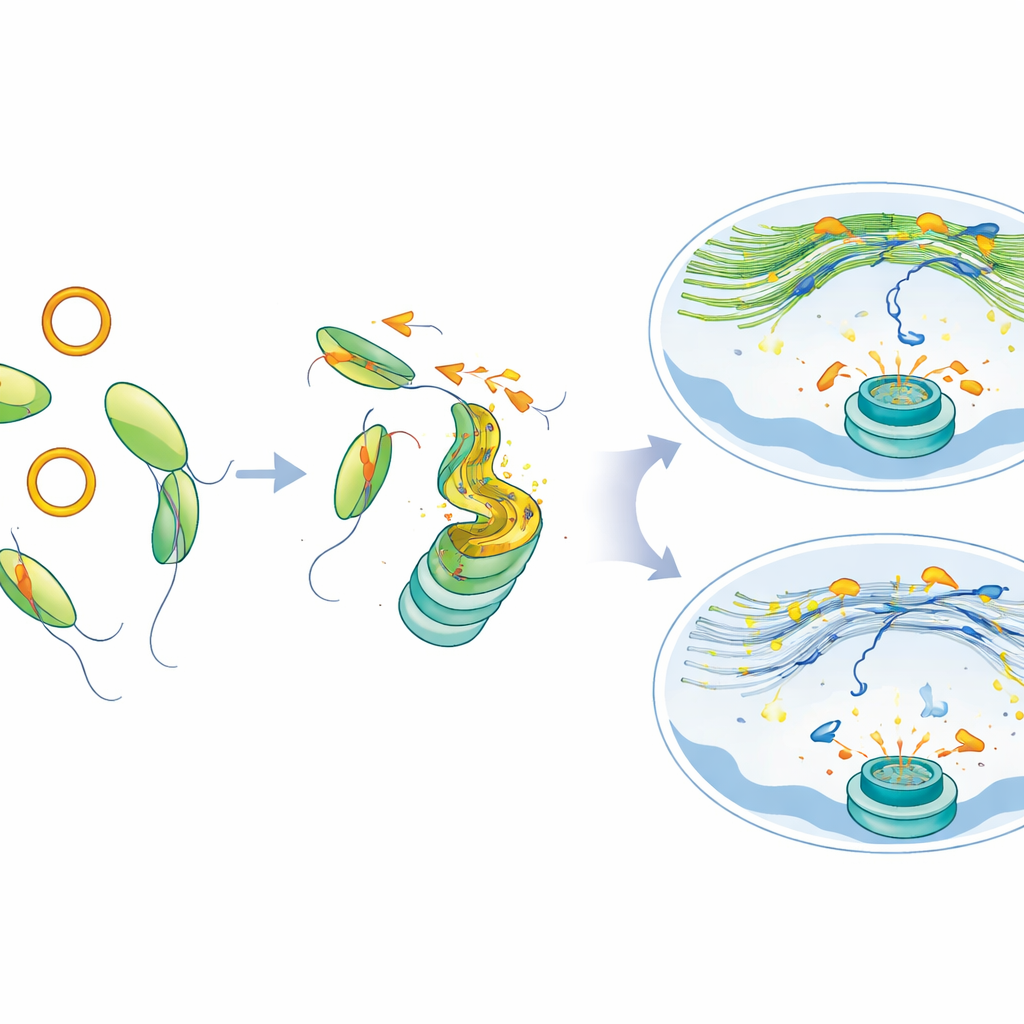
От неправильного ремонта к терапевтической возможности
Клетки с недостатком MYH9 или клетки, вынужденно продуцирующие избыток circATP9B, накапливали устойчивые маркеры повреждений и мелкие дополнительные ядра — признаки разрыва хромосом. Эти клетки также становились более уязвимыми к ингибиторам PARP как в культурах, так и в моделях опухолей на мышах, что означает: вмешательство в этот путь делает раковые клетки особенно уязвимыми при применении препаратов, нарушающих ремонт ДНК. Важно, что при восстановлении MYH9 или снижении уровня circATP9B сеть ядерного актина восстанавливалась, разрывы ДНК перемещались и объединялись более нормально, и ремонт улучшался даже в клетках с мутацией SF3B1.
Что это значит для пациентов
Проще говоря, исследование показывает, что распространённая раковая мутация может парализовать внутреннюю «железнодорожную систему» клетки для ремонта ДНК. Мутация SF3B1 увеличивает уровень круговой РНК circATP9B, которая, в свою очередь, разрушает моторный белок MYH9, помогающий организовывать актиновые рельсы в ядре. Без прочных рельсов повреждённая ДНК не может эффективно собираться и восстанавливаться, что делает раковые клетки генетически нестабильными, но одновременно более зависимыми от оставшихся путей ремонта. Эта уязвимость помогает объяснить, почему опухоли с мутациями SF3B1 хорошо реагируют на ингибиторы PARP, и указывает на то, что измерение или нацеливание на circATP9B и MYH9 может в будущем помочь персонализировать применения препаратов, повреждающих ДНК, у пациентов с раком.
Цитирование: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Ключевые слова: Ремонт ДНК, круговая РНК, ядерный актин, мутация SF3B1, терапия рака