Clear Sky Science · sv
Cancerassocierad SF3B1-mutation undertrycker DNA-reparation genom att störa organisationen av det nukleära aktinnätverket
Hur celler håller sitt DNA i form
Varje dag utsätts DNA i våra celler för hack, klipp och påfrestningar från strålning, kemikalier och normal ämnesomsättning. Friska celler är vanligtvis mycket bra på att lappa ihop denna skada. Men i många cancerformer är reparationssystemet delvis skadat. Denna studie avslöjar en överraskande ny förklaring: en enda, vanlig mutation i ett splitsningsprotein kastar omkull ett internt stödnätverk inne i cellkärnan, vilket fördröjer DNA-reparation och hjälper cancern att växa.
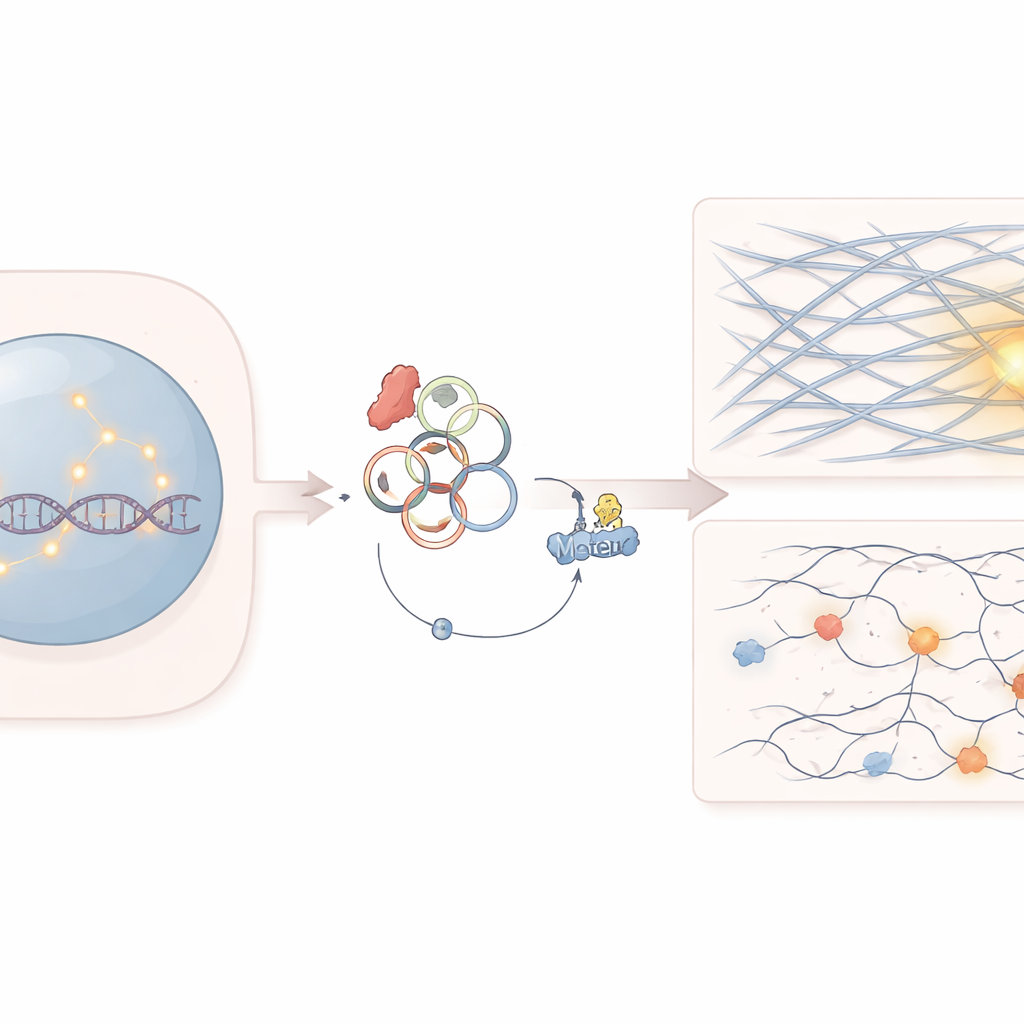
En dold svag punkt i cancerceller
Arbetet fokuserar på en gen som kallas SF3B1, som hjälper till att bearbeta RNA-meddelanden i cellerna. Mutationer i SF3B1 är vanliga i flera blodcancerformer och solida tumörer. Läkare visste redan att dessa mutationer gör cancerceller ovanligt känsliga för vissa läkemedel som riktar sig mot DNA-reparation, såsom PARP-hämmare. Men varför dessa celler har svårt att reparera brutet DNA, särskilt svårare att åtgärda brott som uppstår i tätt packade regioner av genomet, var inte fullständigt begripet.
Rollen för cirkulärt RNA och ett motorprotein
Forskarna upptäckte att SF3B1-mutation förändrar hur vissa RNA-molekyler sys ihop och ökar produktionen av ett cirkulärt RNA kallat circATP9B. Till skillnad från typiskt linjärt RNA bildar cirkulära RNA slutna slingor och kan fungera som svampar eller lockbeten för proteiner. Här binder circATP9B till ett motorprotein som heter MYH9, vilket normalt hjälper till att organisera aktinfilament—samma typ av strukturella fibrer som är bättre kända för att forma celler och driva muskelkontraktion. Teamet visade att circATP9B främjar märkning och nedbrytning av MYH9, vilket minskar dess nivåer utan att ändra dess genuttryck.
Att bryta det nukleära vägnätet
Inne i kärnan kan aktin montera sig till tunna filament som fungerar som spår. Efter att DNA skadats måste brutna bitar, särskilt i tätt packad ”heterokromatin”, förflyttas längs dessa spår till säkrare zoner där noggrann reparation kan ske. Med hjälp av levande cellavbildning följde forskarna lysande markörer som framhäver DNA-brott och nukleärt aktin. När MYH9 minskade bildades inte den normalt rika väven av nukleära aktinfilament på rätt sätt efter strålning. Som ett resultat rörde sig de brutna DNA-fläckarna långsammare, färdades kortare sträckor och klustrades mindre effektivt, särskilt för den reparationsväg som förlitar sig på att kopiera intakt DNA som mall. Dessa långsamma, isolerade brott förblev olösta i många timmar.
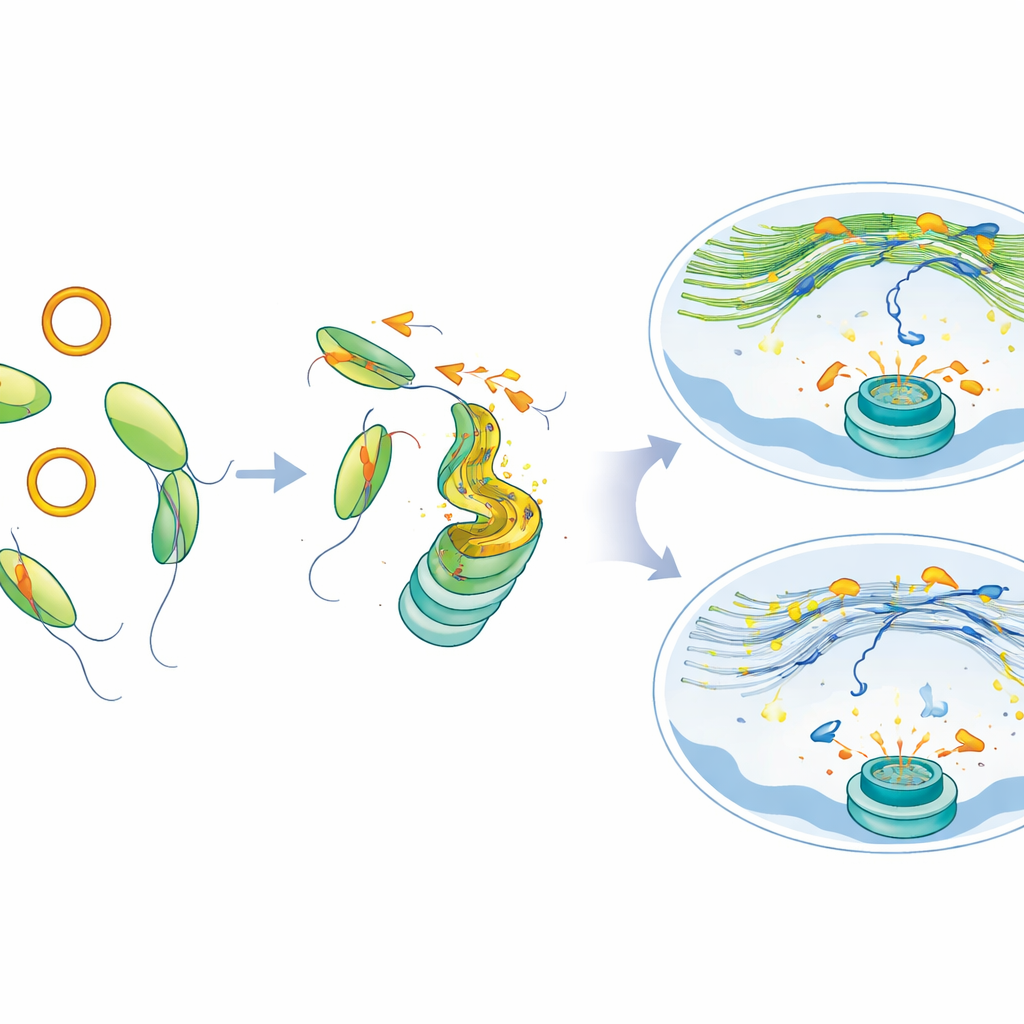
Från felaktig reparation till behandlingsmöjlighet
Celler utan MYH9, eller celler som tvingades producera överskott av circATP9B, samlade på sig bestående skademarkörer och små extra kärnor—tecken på att kromosomer fragmenterats. Dessa celler blev också mer sårbara för PARP-hämmare, både i odlingsskålar och i musmodeller för tumörer, vilket innebär att störning av denna väg lämnar cancerceller särskilt utsatta när läkemedel som angriper DNA-reparation används. Viktigt är att när forskarna återställde MYH9 eller minskade circATP9B återhämtade sig det nukleära aktinnätverket, DNA-brotten rörde sig och klustrades mer normalt, och reparationen förbättrades även i celler med SF3B1-mutation.
Vad detta betyder för patienter
Enkelt uttryckt visar denna studie att en vanlig cancer‑mutation kan sabotera cellens interna ”järnvägssystem” för DNA-reparation. SF3B1-mutation ökar ett cirkulärt RNA, circATP9B, som i sin tur förstör MYH9-motorproteinet som hjälper till att organisera aktinspår i kärnan. Utan stabila spår kan inte brutet DNA effektivt föras samman och lagas, vilket lämnar cancerceller genetiskt instabila men också mer beroende av återstående reparationsvägar. Denna sårbarhet hjälper till att förklara varför tumörer med SF3B1-mutationer svarar väl på PARP-hämmare och tyder på att mätning eller riktning mot circATP9B och MYH9 en dag kan hjälpa till att skräddarsy DNA-skadande behandlingar för cancerpatienter.
Citering: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Nyckelord: DNA-reparation, cirkulärt RNA, nukleärt aktin, SF3B1-mutation, cancerbehandling