Clear Sky Science · he
המוטציה ב-SF3B1 המקושרת לסרטן מדכאת תיקון DNA על-ידי שיבוש ארגון רשת האקטין הגרעינית
איך תאים שומרים על מבנה ה-DNA שלהם
כל יום, ה-DNA בתאים שלנו ננעץ, נחתך ונחשף ללחצים מקרינה, כימיקלים ותהליכים מטבוליים שגרתיים. תאים בריאים בדרך כלל מצטיינים בתיקון הנזקים האלה. אבל ברבות מהמחלות הסרטן המערכת הזו חלקית תקולה. המחקר הזה חושף סיבה מפתיעה נוספת: מוטציה אחת נפוצה בחלבון הספלייסינג מפרקת רשת תמיכה פנימית בתוך גרעין התא, מאיטה את תיקון ה-DNA ותומכת בצמיחת הסרטן.
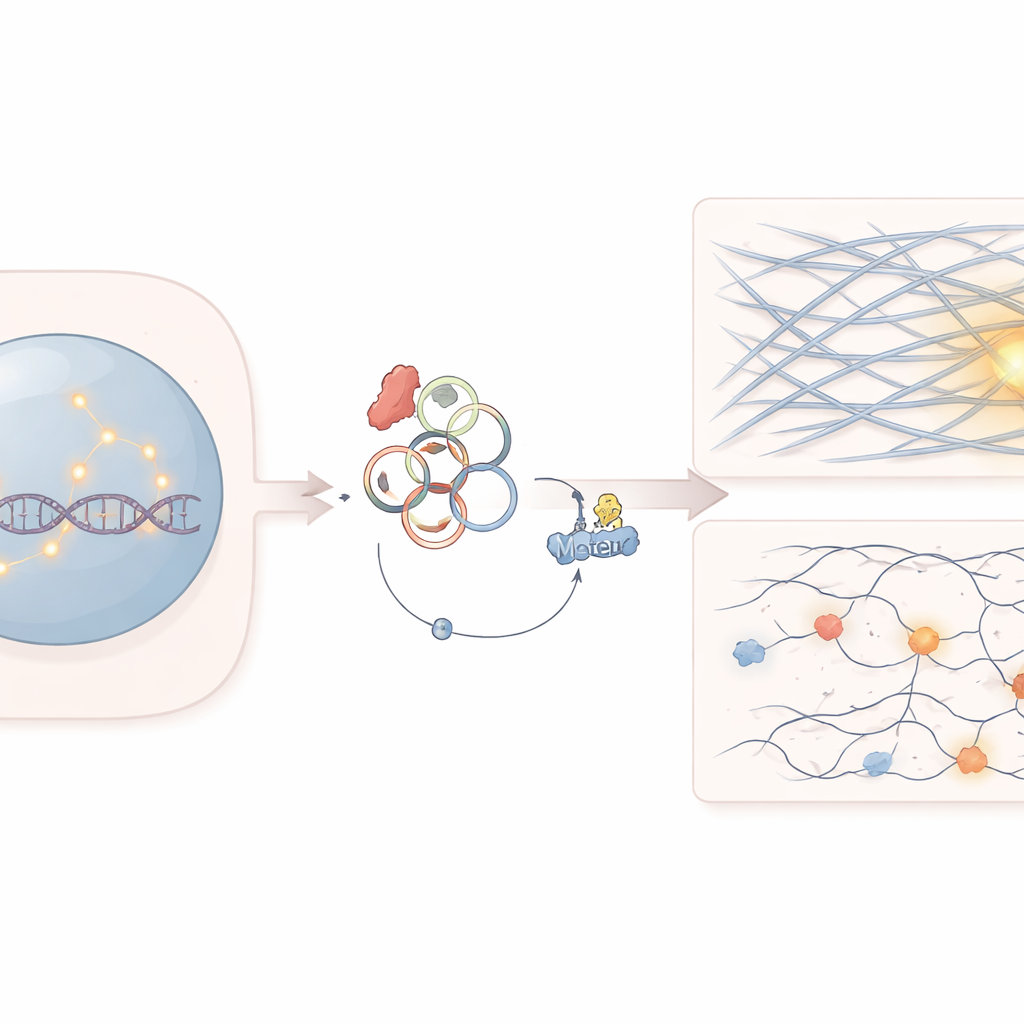
נקודת תורפה נסתרת בתאי סרטן
העבודה מתמקדת בגן בשם SF3B1, שעוזר לעבד מסרי RNA בתאים. מוטציות ב-SF3B1 נפוצות במספר סרטן דם ובגידולים מוצקים. הרופאים כבר ידעו שמוטציות אלה הופכות תאי סרטן לרגישים במיוחד לתרופות שפוגעות בתיקון ה-DNA, כמו מעכבי PARP. עם זאת, מדוע תאים אלה מתקשים לתקן שברים ב-DNA, ובמיוחד שברים שקשה לתקן שמופיעים באזורים דחוסים של הגנום, לא היה מובן במלואו.
תפקיד של RNA מעגלי וחלבון מנוע
החוקרים גילו שהמוטציה ב-SF3B1 משנה את הדרך שבה חלק ממולקולות ה-RNA מרכיבות את עצמן, ומגבירה את ייצורו של RNA מעגלי בשם circATP9B. בניגוד ל-RNA קווי טיפוסי, RNA מעגלי יוצר לולאות סגורות ויכול לשמש כספוג או כפתיון לחלבונים. כאן, circATP9B קושר חלבון מנוע בשם MYH9, שבדרך כלל מסייע לארגן פילמנטים של אקטין—אותם סיבים מבניים המוכרים יותר מעיצוב תאים והנעת כיווץ שריר. הצוות הראה כי circATP9B מעודד סימון ופירוק של MYH9, מה שמקטין את רמתו ללא שינוי בביטוי הגן שלו.
שבירת "רשת הכבישים" הגרעינית
בתוך הגרעין, אקטין יכול להתארגן לפילמנטים דקים שפועלים כמסילות. לאחר נזק ל-DNA, קטעים שבורים, במיוחד ב"הטרוכרומטין" הדחוס, חייבים לנוע לאורך מסילות אלה לאזורים בטוחים שבהם ניתן לבצע תיקון מדויק. בעזרת הדמיה בתאים חיים, המדענים צפו בסמנים מנצנצים שמדגישים שברים ב-DNA ואקטין גרעיני. כאשר MYH9 הוּרַד, רשת הפילמנטים העשירה של האקטין הגרעיני נכשלה להתהוות כראוי לאחר קרינה. כתוצאה מכך, הנקודות של ה-DNA השבור נעו לאט יותר, נסעו מרחקים קצרים יותר והתאספו בפחות יעילות, במיוחד עבור מסלול התיקון שתלוי בהעתקת DNA שלם כתבנית. שבירות איטיות ומבודדות אלה נותרו בלתי פתורות למשך שעות רבות.
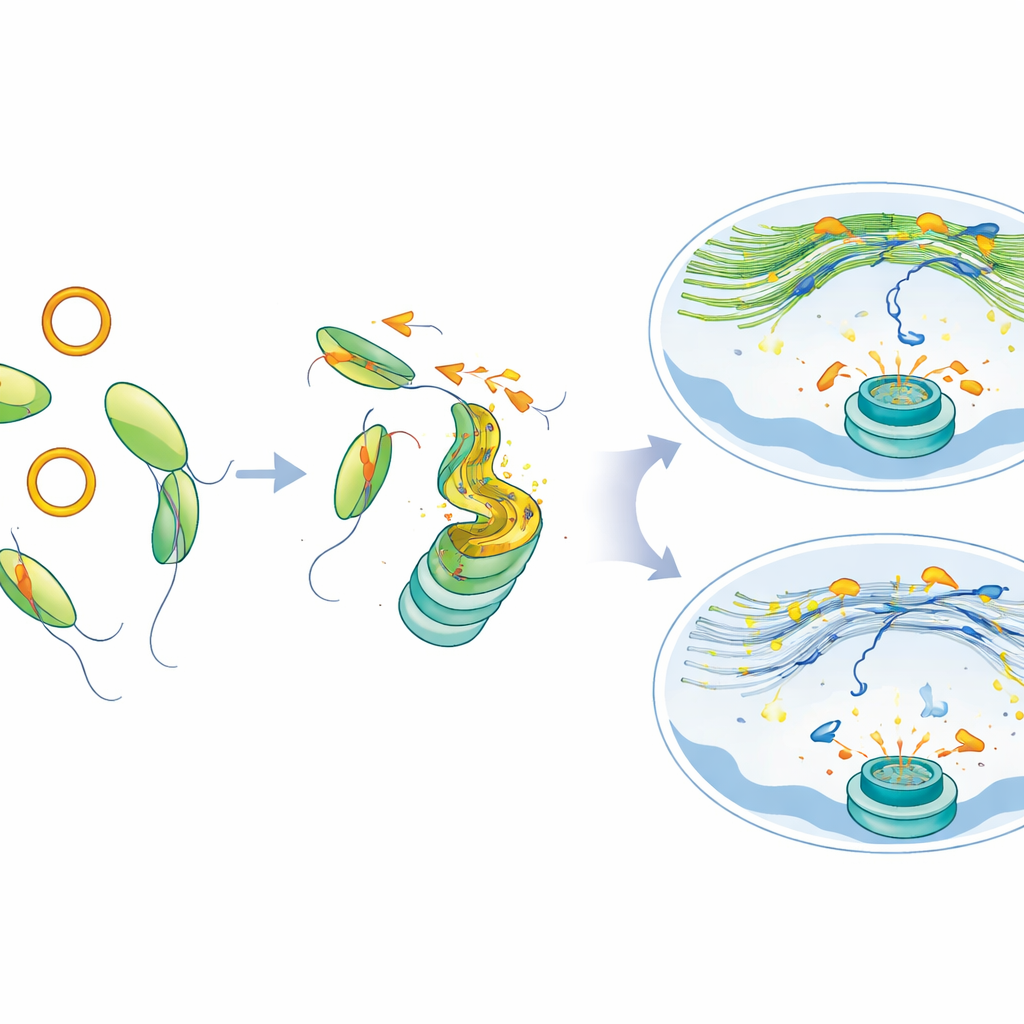
מגרימת תיקון לקידום הזדמנות טיפולית
תאים חסרי MYH9, או תאים שאולצו לייצר עודף circATP9B, צברו סימני נזק מתמשכים וגרעינים קטנים נוספים—סימנים לקרעי כרומוזומים. תאים אלה גם הפכו לפגיעים יותר למעכבי PARP, הן בתרביות ובשורות ניסויים בעכברים עם גידולים, כלומר התערבות בדרך זו הופכת תאי סרטן לחשופים במיוחד כאשר משתמשים בתרופות שנועדו לפגוע בתיקון ה-DNA. חשוב לציין, כששיקמו את MYH9 או הקטינו את circATP9B, רשת האקטין הגרעינית חזרה להתהוות, שברי ה-DNA נעו והתאספו בצורה יותר נורמלית, והתיקון השתפר אפילו בתאים שנשאו את מוטציית SF3B1.
מה המשמעות עבור מטופלים
בלי מורכבות: המחקר מראה שמוטציה נפוצה בסרטן יכולה לפגוע ב"מערכת הרכבות" הפנימית של התא שאחראית על תיקון ה-DNA. מוטציית SF3B1 מגבירה RNA מעגלי, circATP9B, שמצידו הורס את חלבון המנוע MYH9 שעוזר לארגן מסילות אקטין בגרעין. ללא מסילות יציבות, שברי DNA לא ניתנים לאיסוף ולתיקון ביעילות, מה שמשאיר את תאי הסרטן בלתי יציבים גנטית אך גם יותר תלויים במסלולי תיקון ששרדו. פגיעות זו מסייעת להסביר מדוע גידולים עם מוטציות ב-SF3B1 מגיבים באופן טוב למעכבי PARP, ומציעה שמדידה או מטרה של circATP9B ו-MYH9 עשויה בעתיד לסייע להתאים טיפולים הפוגעים ב-DNA למטופלים בסרטן.
ציטוט: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
מילות מפתח: תיקון DNA, RNA מעגלי, אקטין גרעיני, מוטציית SF3B1, טיפול בסרטן