Clear Sky Science · fr
La mutation associée au cancer SF3B1 supprime la réparation de l’ADN en perturbant l’organisation du réseau d’actine nucléaire
Comment les cellules maintiennent l’intégrité de leur ADN
Chaque jour, l’ADN de nos cellules est éraflé, coupé et soumis à des contraintes par les radiations, les produits chimiques et le métabolisme normal. Les cellules saines sont généralement très efficaces pour colmater ces dégâts. Mais dans de nombreux cancers, ce système de réparation est partiellement défaillant. Cette étude révèle une raison nouvelle et surprenante : une seule mutation fréquente dans une protéine d’épissage perturbe un réseau de soutien interne à l’intérieur du noyau cellulaire, ralentissant la réparation de l’ADN et favorisant la progression tumorale.
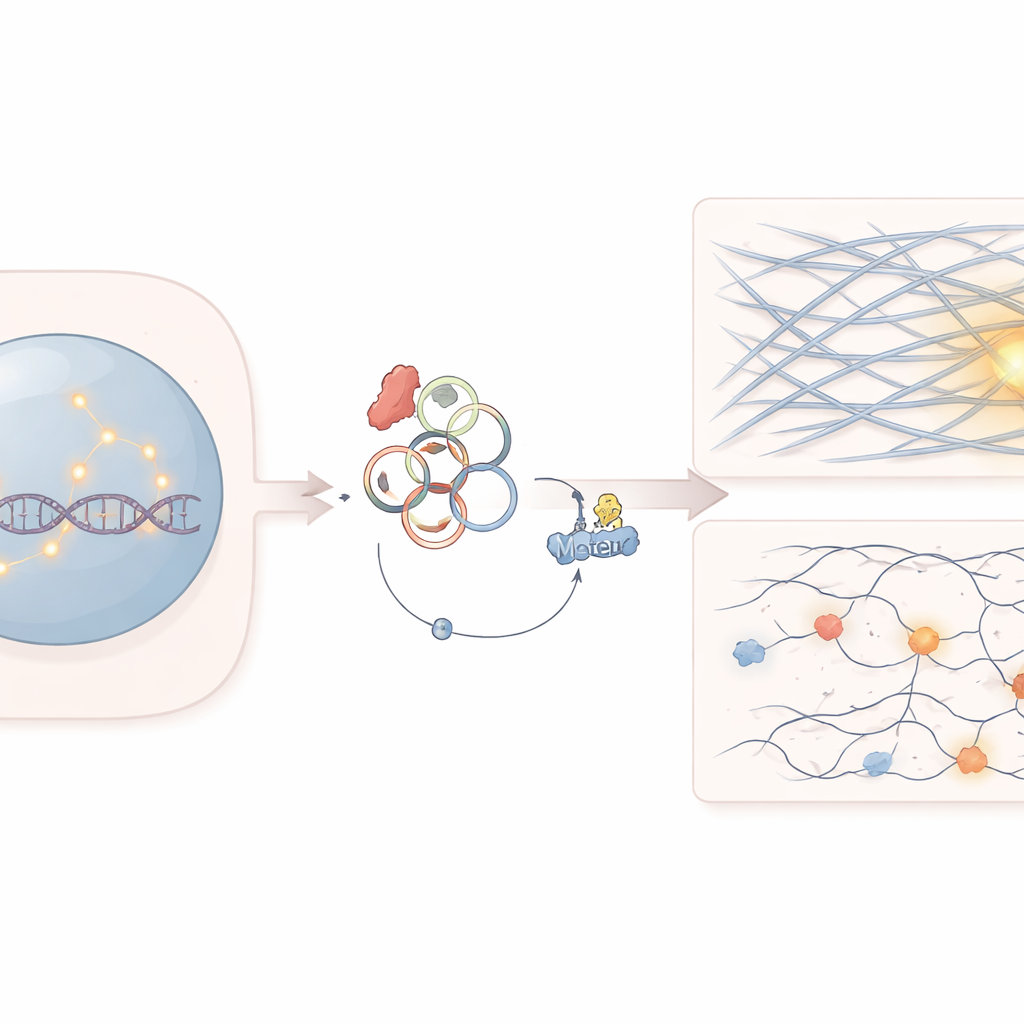
Une faiblesse cachée des cellules cancéreuses
Les travaux se concentrent sur un gène appelé SF3B1, qui participe au traitement des messages ARN dans les cellules. Les mutations de SF3B1 sont fréquentes dans plusieurs cancers du sang et tumeurs solides. Les cliniciens savaient déjà que ces mutations rendent les cellules cancéreuses exceptionnellement sensibles à certains médicaments ciblant la réparation de l’ADN, comme les inhibiteurs de PARP. En revanche, pourquoi ces cellules peinent à réparer l’ADN brisé, en particulier les cassures difficiles à réparer qui apparaissent dans les régions fortement compactées du génome, restait mal élucidé.
Le rôle de l’ARN circulaire et d’une protéine motrice
Les chercheurs ont découvert que la mutation de SF3B1 modifie la façon dont certains ARN sont assemblés, favorisant la production d’un ARN circulaire nommé circATP9B. Contrairement aux ARN linéaires habituels, les ARN circulaires forment des boucles fermées et peuvent agir comme des éponges ou des leurres pour des protéines. Ici, circATP9B se lie à une protéine motrice nommée MYH9, qui aide normalement à organiser les filaments d’actine — ces fibres structurelles mieux connues pour façonner les cellules et alimenter la contraction musculaire. L’équipe a montré que circATP9B favorise le marquage puis la dégradation de MYH9, réduisant ses niveaux sans modifier l’expression du gène.
La destruction du réseau routier nucléaire
À l’intérieur du noyau, l’actine peut s’assembler en filaments fins qui servent de voies. Après une lésion de l’ADN, les fragments cassés, notamment dans l’« hétérochromatine » dense, doivent se déplacer le long de ces voies vers des zones plus sûres où une réparation précise peut avoir lieu. Grâce à l’imagerie en cellules vivantes, les scientifiques ont suivi des marqueurs lumineux qui mettent en évidence les cassures d’ADN et l’actine nucléaire. Lorsque MYH9 était réduit, la toile normalement abondante de filaments d’actine nucléaire ne se formait pas correctement après irradiation. En conséquence, les foyers d’ADN brisé se déplaçaient plus lentement, parcouraient de plus courtes distances et se regrouperaient moins efficacement, en particulier pour la voie de réparation qui s’appuie sur le copier-coller d’un ADN intact comme matrice. Ces cassures ralenties et isolées sont restées non résolues pendant de nombreuses heures.
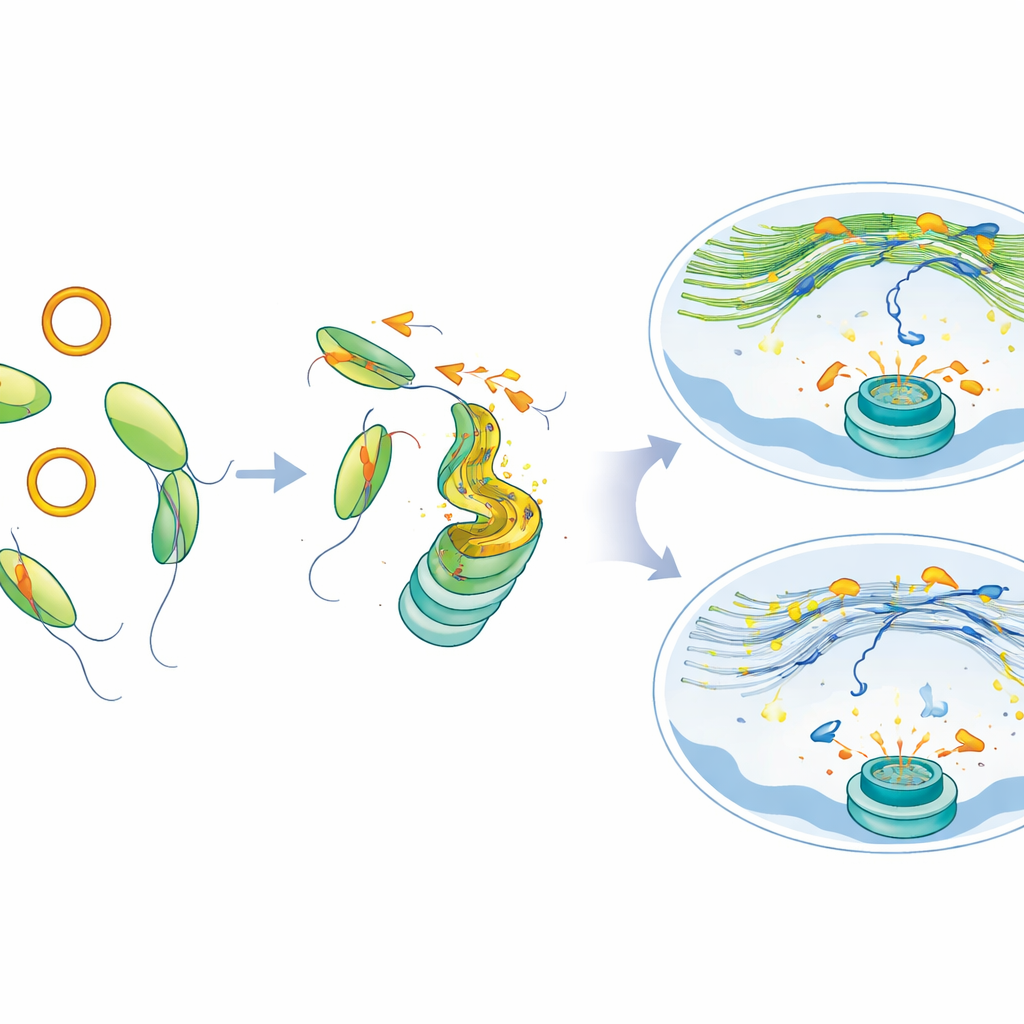
De la réparation défaillante à une opportunité thérapeutique
Les cellules dépourvues de MYH9, ou celles contraintes de produire un excès de circATP9B, accumulaient des marques de dommages persistants et de petites noyaux supplémentaires — signes d’éclatement chromosomique. Ces cellules devenaient également plus vulnérables aux inhibiteurs de PARP, tant en culture qu’au sein de modèles tumoraux murins, ce qui signifie que perturber cette voie expose particulièrement les cellules cancéreuses lorsque des médicaments ciblant la réparation de l’ADN sont utilisés. Fait important, lorsque les chercheurs ont restauré MYH9 ou réduit circATP9B, le réseau d’actine nucléaire s’est reconstitué, les cassures d’ADN se sont déplacées et regroupées de façon plus normale, et la réparation s’est améliorée même dans des cellules porteuses de la mutation SF3B1.
Ce que cela signifie pour les patients
En termes simples, cette étude montre qu’une mutation cancéreuse courante peut saboter le « réseau ferroviaire » interne de la cellule dédié à la réparation de l’ADN. La mutation SF3B1 augmente un ARN circulaire, circATP9B, qui détruit à son tour la protéine motrice MYH9, laquelle organise les voies d’actine dans le noyau. Sans voies solides, l’ADN brisé ne peut pas être efficacement rapproché et réparé, laissant les cellules cancéreuses génétiquement instables mais aussi plus dépendantes des voies de réparation restantes. Cette vulnérabilité aide à expliquer pourquoi les tumeurs avec mutation SF3B1 répondent bien aux inhibiteurs de PARP et suggère que mesurer ou cibler circATP9B et MYH9 pourrait un jour aider à adapter les traitements endommageant l’ADN pour les patients atteints de cancer.
Citation: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Mots-clés: Réparation de l’ADN, ARN circulaire, actine nucléaire, mutation SF3B1, thérapie contre le cancer