Clear Sky Science · nl
SF3B1-mutatie geassocieerd met kanker onderdrukt DNA-herstel door de organisatie van het nucleaire actinenetwerk te verstoren
Hoe cellen hun DNA in goede staat houden
Dagelijks wordt het DNA in onze cellen geknipt, beschadigd en blootgesteld aan stress door straling, chemicaliën en normale stofwisseling. Gezonde cellen zijn doorgaans erg goed in het herstellen van deze schade. Maar in veel vormen van kanker is dat herstelmechanisme gedeeltelijk defect. Deze studie onthult een verrassende nieuwe reden waarom: een enkele, veelvoorkomende mutatie in een splice-eiwit brengt een intern steunnetwerk binnen de celkern uit balans, vertraagt DNA-herstel en bevordert zo de groei van kanker.
Een verborgen zwakke plek in kankercellen
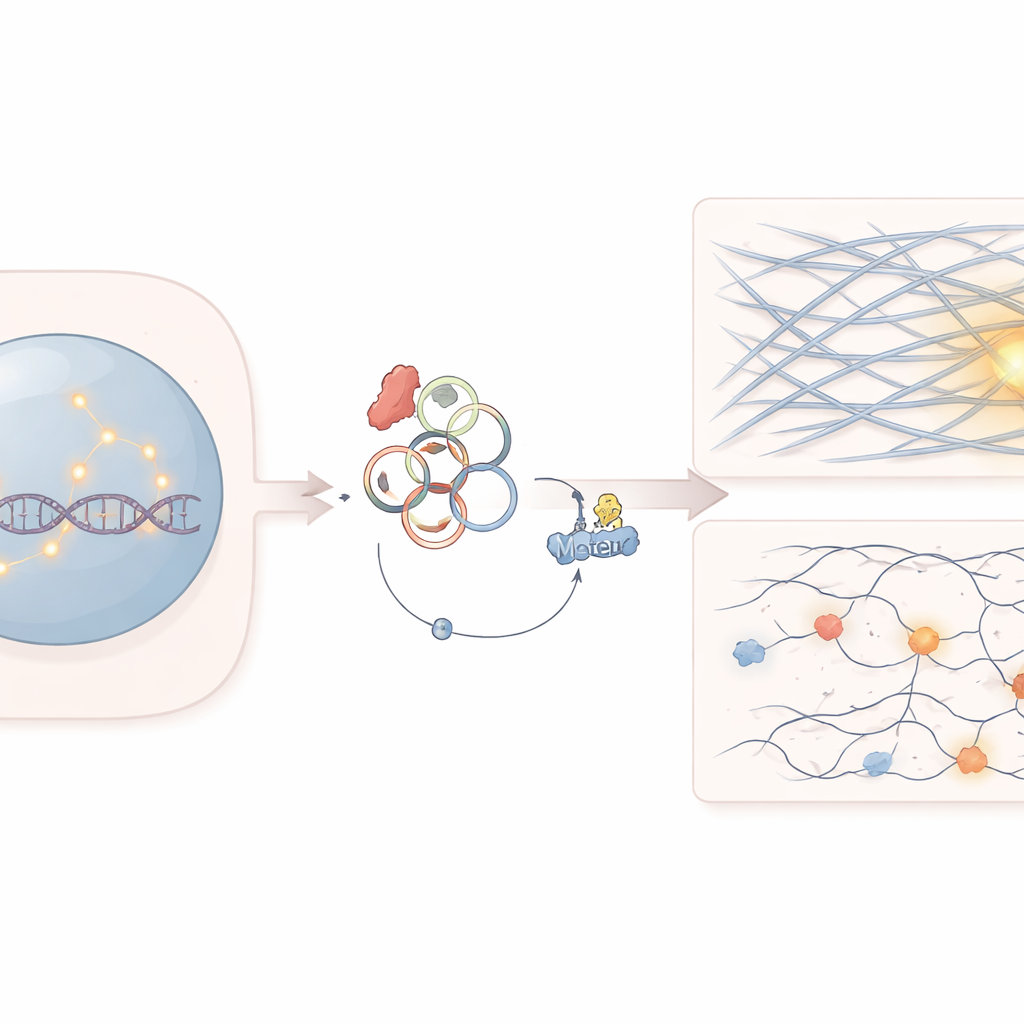
De studie richt zich op een gen dat SF3B1 heet en dat helpt bij het verwerken van RNA-boodschappen in cellen. Mutaties in SF3B1 komen veel voor bij verschillende bloedkankers en solide tumoren. Artsen wisten al dat deze mutaties kankercellen uitzonderlijk gevoelig maken voor bepaalde geneesmiddelen die DNA-herstel remmen, zoals PARP-remmers. Waarom deze cellen echter moeite hebben met het repareren van gebroken DNA, vooral de moeilijker te herstellen breuken die ontstaan in dicht opgevouwen delen van het genoom, was nog niet volledig verklaard.
De rol van circulair RNA en een motorproteïne
De onderzoekers ontdekten dat de SF3B1-mutatie verandert hoe sommige RNA-moleculen aan elkaar worden gezet, waardoor de productie van een circulair RNA genaamd circATP9B toeneemt. In tegenstelling tot doorgaans lineair RNA vormen circulaire RNA’s gesloten lussen en kunnen ze functioneren als sponzen of lokmiddelen voor eiwitten. Hier bindt circATP9B aan een motorproteïne genaamd MYH9, dat normaal helpt bij het organiseren van actinefilamenten—dezelfde soort structurele vezels die bekend zijn van celvorming en spiercontractie. Het team toonde aan dat circATP9B aanzet tot markering en afbraak van MYH9, waardoor de hoeveelheid van dit eiwit daalt zonder dat de genexpressie verandert.
De nucleaire spoorbaan kapotmaken
In de celkern kan actine zich ordenen in fijne filamenten die als sporen fungeren. Na DNA-schade moeten de gebroken stukken, vooral in strak verpakte “heterochromatine”, langs deze sporen verplaatst worden naar veiligere zones waar nauwkeurig herstel kan plaatsvinden. Met live-celbeeldvorming volgden de wetenschappers oplichtende merkers die DNA-breuken en nucleair actine markeren. Wanneer MYH9 verminderd was, vormde het normaliter rijke netwerk van nucleaire actinefilamenten zich na straling niet goed. Als gevolg daarvan bewogen de beschadigde DNA-locaties langzamer, legden ze kortere afstanden af en clusteren ze minder efficiënt, met name voor het herstelpad dat afhankelijk is van het kopiëren van intact DNA als sjabloon. Deze trage, geïsoleerde breuken bleven vele uren onbehandeld.
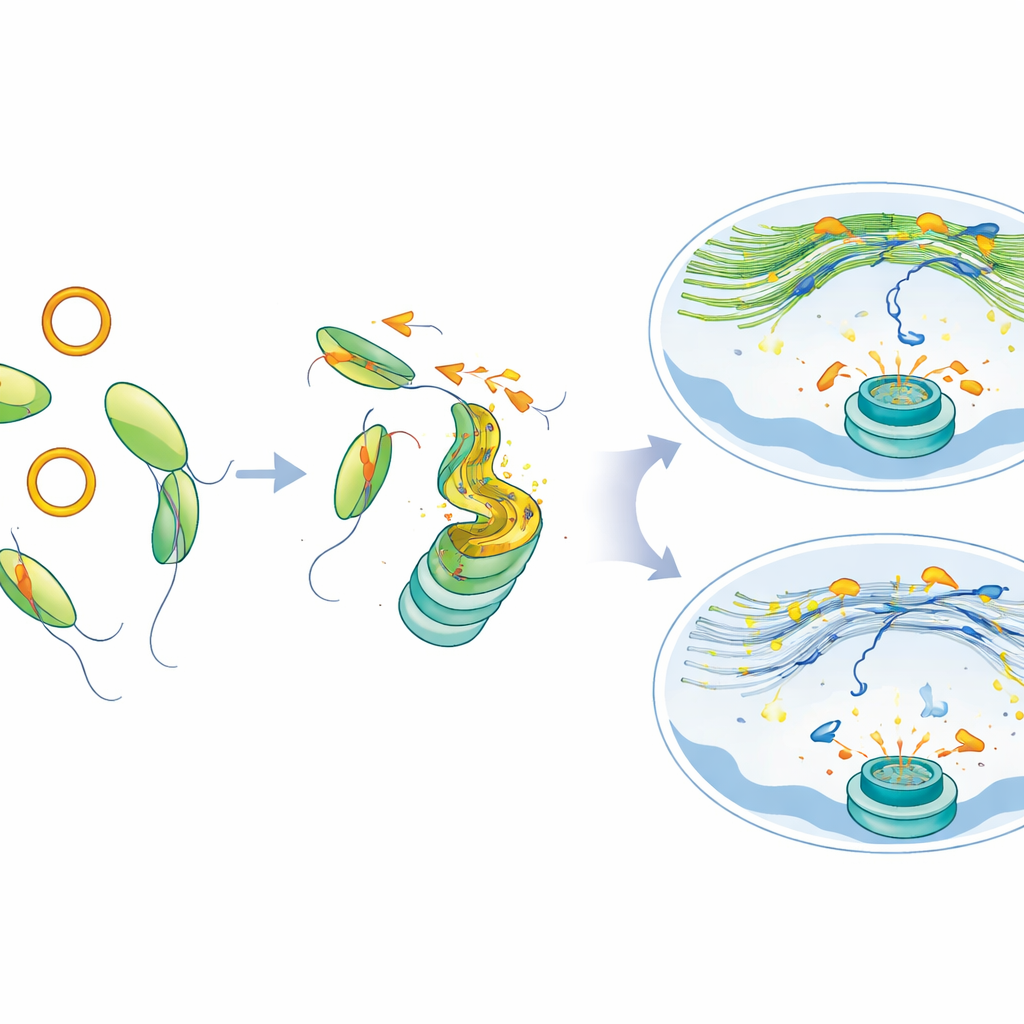
Van falend herstel naar behandelbare kans
Cellen zonder MYH9, of cellen die gedwongen werden grote hoeveelheden circATP9B te produceren, stapelden aanhoudende schadekenmerken en kleine extra kernen op—tekens dat chromosomen uiteen vallen. Deze cellen werden ook gevoeliger voor PARP-remmers, zowel in kweek als in muismodellen met tumoren, wat betekent dat het verstoren van deze route kankercellen extra blootstelt wanneer middelen die DNA-schade benutten worden toegepast. Belangrijk is dat wanneer de onderzoekers MYH9 herstelden of circATP9B verminderden, het nucleaire actinenetwerk terugkeerde, DNA-breuken weer normaler bewogen en clusteren, en het herstel verbeterde, zelfs in cellen met de SF3B1-mutatie.
Wat dit betekent voor patiënten
In eenvoudige bewoordingen laat deze studie zien dat een veelvoorkomende kankermutatie het interne “spoorwegsysteem” van de cel voor DNA-herstel kan saboteren. De SF3B1-mutatie verhoogt een circulair RNA, circATP9B, dat op zijn beurt het MYH9-motorproteïne vernietigt dat helpt bij het organiseren van actinesporen in de kern. Zonder stevige sporen kunnen beschadigde DNA-fragmenten niet efficiënt bij elkaar worden gebracht en gerepareerd, waardoor kankercellen genetisch instabiel raken maar ook meer afhankelijk van de resterende herstelroutes. Deze kwetsbaarheid verklaart waarom tumoren met SF3B1-mutaties goed reageren op PARP-remmers en suggereert dat het meten of gericht benaderen van circATP9B en MYH9 mogelijk kan helpen bij het afstemmen van DNA-schadelijke therapieën voor kankerpatiënten.
Bronvermelding: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Trefwoorden: DNA-herstel, circulair RNA, nucleair actine, SF3B1-mutatie, kankertherapie