Clear Sky Science · pt
Mutação associada ao câncer em SF3B1 suprime o reparo do DNA ao desorganizar a rede de actina nuclear
Como as Células Mantêm o DNA em Boa Forma
Todos os dias, o DNA em nossas células é riscado, cortado e estressado por radiação, substâncias químicas e pelo metabolismo normal. Células saudáveis costumam ser muito boas em consertar esses danos. Mas em muitos cânceres, esse sistema de reparo está parcialmente comprometido. Este estudo revela uma nova e surpreendente razão para isso: uma única mutação comum em uma proteína de splicing desvia uma rede de suporte interna dentro do núcleo da célula, retardando o reparo do DNA e favorecendo o crescimento do câncer.
Um Ponto Fraco Oculto nas Células Cancerosas
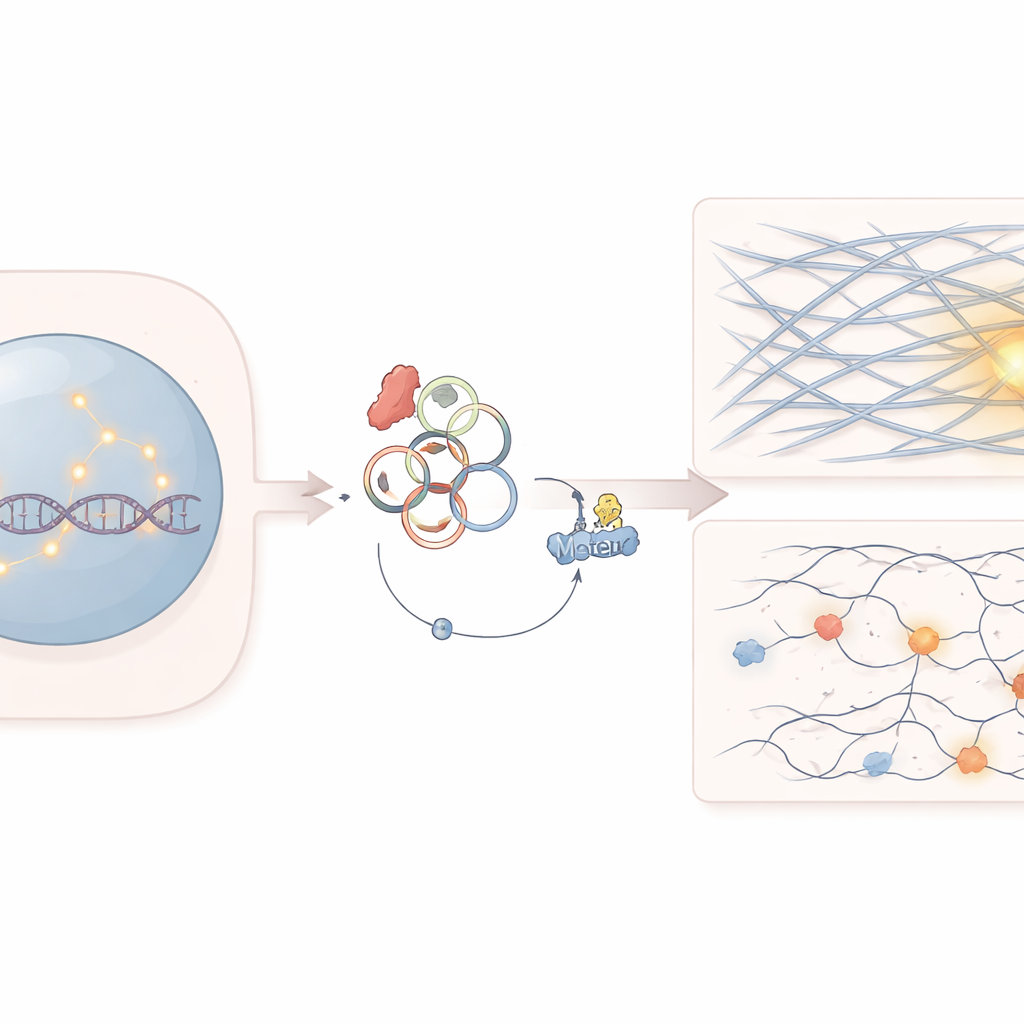
O trabalho centra-se em um gene chamado SF3B1, que auxilia no processamento de mensagens de RNA nas células. Mutações em SF3B1 são comuns em vários cânceres hematológicos e tumores sólidos. Os médicos já sabiam que essas mutações tornam as células cancerosas incomumente sensíveis a certos medicamentos que visam o reparo do DNA, como inibidores de PARP. No entanto, por que essas células têm dificuldade em reparar quebras de DNA, especialmente as mais difíceis que surgem em regiões densamente compactadas do genoma, não era totalmente compreendido.
O Papel do RNA Circular e de uma Proteína Motora
Os pesquisadores descobriram que a mutação em SF3B1 altera a forma como alguns RNAs são emendados, aumentando a produção de um RNA circular chamado circATP9B. Ao contrário do RNA linear típico, os RNAs circulares formam laços fechados e podem atuar como esponjas ou iscas para proteínas. Aqui, o circATP9B se liga a uma proteína motora chamada MYH9, que normalmente ajuda a organizar filamentos de actina—o mesmo tipo de fibras estruturais mais conhecidas por moldar células e impulsionar a contração muscular. A equipe demonstrou que o circATP9B incentiva a marcação e a degradação de MYH9, reduzindo seus níveis sem alterar a expressão do gene.
Quebrando a Rede Rodoviária do Núcleo
Dentro do núcleo, a actina pode se montar em filamentos finos que funcionam como trilhos. Após danos ao DNA, fragmentos quebrados, especialmente em heterocromatina compacta, precisam se mover por esses trilhos até zonas mais seguras onde o reparo preciso pode ocorrer. Usando imagem de células vivas, os cientistas observaram marcadores brilhantes que destacam quebras de DNA e actina nuclear. Quando MYH9 foi reduzida, a teia normalmente rica de filamentos de actina nuclear deixou de se formar adequadamente após radiação. Como resultado, os pontos de DNA quebrado se moveram mais lentamente, percorreram distâncias menores e se agruparam com menos eficiência, particularmente para a via de reparo que depende da cópia de DNA intacto como molde. Essas quebras lentas e isoladas permaneceram sem solução por muitas horas.
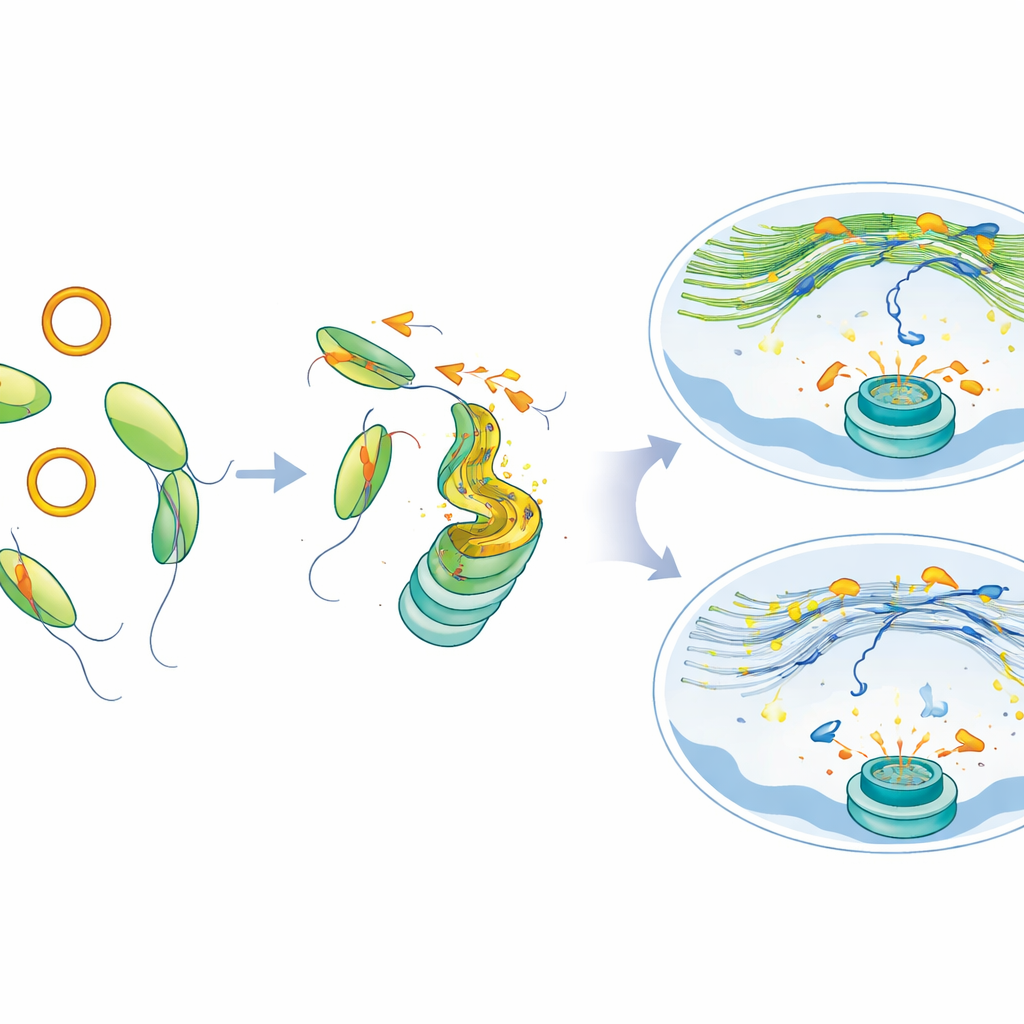
Do Reparo Defeituoso à Oportunidade Terapêutica
Células sem MYH9, ou células forçadas a produzir excesso de circATP9B, acumularam marcas persistentes de dano e pequenos núcleos extras—sinais de que cromossomos se fragmentaram. Essas células também se tornaram mais vulneráveis a inibidores de PARP, tanto em cultura quanto em modelos de tumor em camundongos, o que significa que interferir nessa via deixa as células cancerosas especialmente expostas quando medicamentos que afetam o reparo do DNA são usados. Importante, quando os pesquisadores restauraram MYH9 ou reduziram circATP9B, a rede de actina nuclear se recuperou, as quebras de DNA se moveram e se agruparam de forma mais normal, e o reparo melhorou mesmo em células com a mutação SF3B1.
O Que Isso Significa para Pacientes
Em termos simples, este estudo revela que uma mutação comum no câncer pode sabotar o “sistema ferroviário” interno da célula para o reparo do DNA. A mutação em SF3B1 aumenta um RNA circular, circATP9B, que por sua vez destrói a proteína motora MYH9 que ajuda a organizar os trilhos de actina no núcleo. Sem trilhos sólidos, o DNA quebrado não pode ser eficientemente reunido e consertado, deixando as células cancerosas geneticamente instáveis, mas também mais dependentes das rotas de reparo remanescentes. Essa vulnerabilidade ajuda a explicar por que tumores com mutações em SF3B1 respondem bem a inibidores de PARP e sugere que medir ou direcionar circATP9B e MYH9 pode um dia ajudar a personalizar terapias que danificam o DNA para pacientes com câncer.
Citação: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Palavras-chave: reparo do DNA, RNA circular, actina nuclear, mutação SF3B1, terapia contra o câncer