Clear Sky Science · de
Mit Krebs assoziierte SF3B1-Mutation hemmt die DNA-Reparatur, indem sie die Organisation des nukleären Actin-Netzwerks stört
Wie Zellen ihre DNA in Form halten
Jeden Tag wird die DNA in unseren Zellen durch Strahlung, Chemikalien und normalen Stoffwechsel angeritzt, geschnitten und belastet. Gesunde Zellen sind in der Regel sehr geschickt darin, diese Schäden zu reparieren. In vielen Krebsarten ist dieses Reparatursystem jedoch teilweise gestört. Diese Studie legt einen überraschenden neuen Grund dafür offen: Eine einzige, häufige Mutation in einem Spleißprotein bringt ein internes Stütznetzwerk im Zellkern durcheinander, verlangsamt die DNA-Reparatur und begünstigt so das Tumorwachstum.
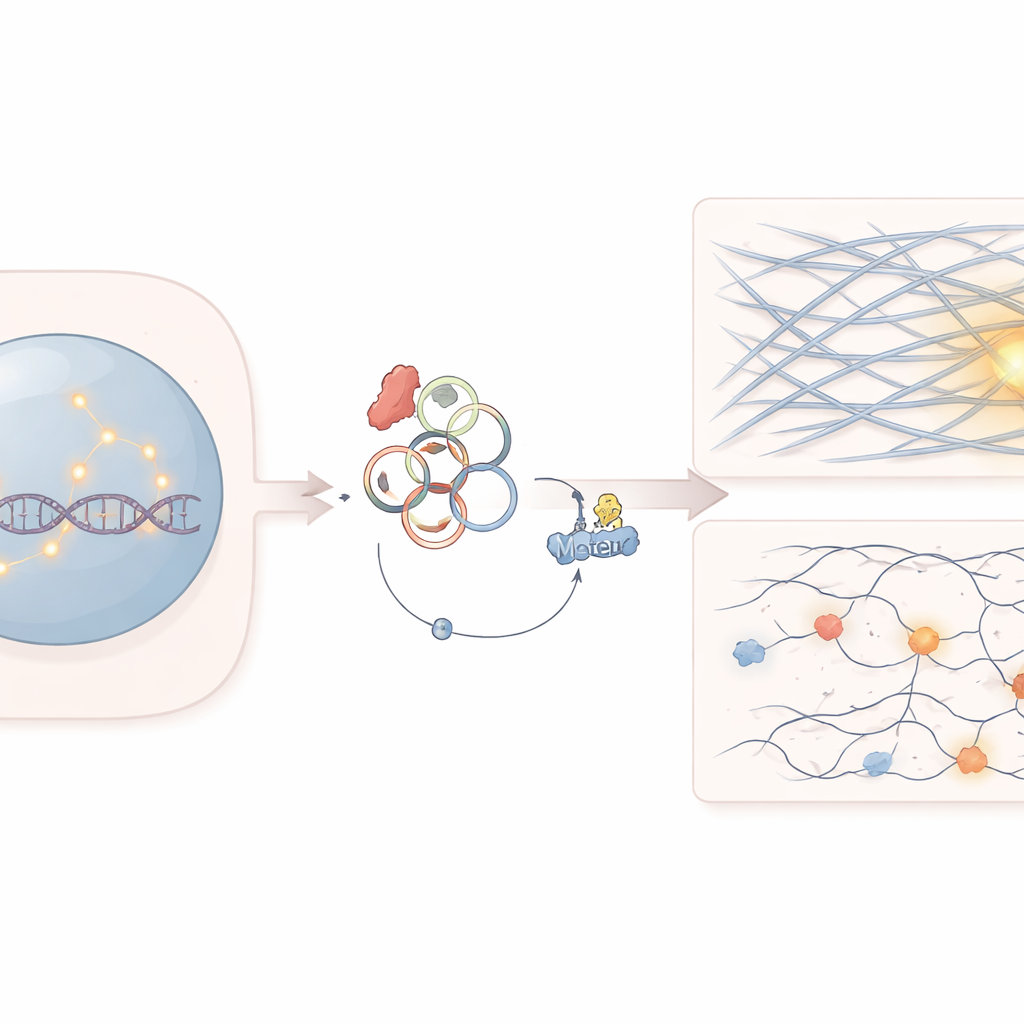
Eine verborgene Schwachstelle in Krebszellen
Die Arbeit konzentriert sich auf ein Gen namens SF3B1, das bei der Verarbeitung von RNA-Botschaften in Zellen hilft. Mutationen in SF3B1 treten häufig in mehreren Blutkrebserkrankungen und soliden Tumoren auf. Kliniker wussten bereits, dass diese Mutationen Krebszellen ungewöhnlich empfindlich gegenüber bestimmten Medikamenten machen, die die DNA-Reparatur angreifen, etwa PARP-Inhibitoren. Warum diese Zellen jedoch Probleme haben, beschädigte DNA zu reparieren—insbesondere schwerer zu behebende Brüche, die in dicht gepackten Bereichen des Genoms entstehen—war bislang nicht vollständig geklärt.
Die Rolle zirkulärer RNA und eines Motorproteins
Die Forschenden entdeckten, dass die SF3B1-Mutation die Art und Weise verändert, wie manche RNA-Moleküle zusammengesetzt werden, und so die Produktion einer zirkulären RNA namens circATP9B erhöht. Anders als typische lineare RNA bilden zirkuläre RNAs geschlossene Schleifen und können als Schwämme oder Köder für Proteine fungieren. Hier bindet circATP9B an ein Motorprotein namens MYH9, das normalerweise hilft, Actinfilamente zu organisieren—die gleichen Strukturfasern, die eher dafür bekannt sind, Zellen zu formen und Muskelkontraktion zu ermöglichen. Das Team zeigte, dass circATP9B dazu führt, dass MYH9 markiert und abgebaut wird, wodurch seine Proteinmenge sinkt, ohne dass sich seine Genexpression ändert.
Der Zusammenbruch des nukleären Straßen-Netzwerks
Im Zellkern kann Actin zu feinen Filamenten zusammengesetzt werden, die wie Schienen wirken. Nach einer DNA-Beschädigung müssen beschädigte Stücke, insbesondere in dicht gepacktem «Heterochromatin», entlang dieser Schienen zu sicheren Bereichen transportiert werden, in denen eine genaue Reparatur stattfinden kann. Mithilfe von Live‑Zell‑Bildgebung verfolgten die Wissenschaftler leuchtende Marker, die DNA‑Brüche und nukleäres Actin sichtbar machen. Wenn MYH9 reduziert war, bildete sich das normalerweise dichte Netz nukleärer Actinfilamente nach Bestrahlung nicht richtig. Infolgedessen bewegten sich die beschädigten DNA‑Stellen langsamer, legten kürzere Strecken zurück und gruppierten sich weniger effizient—insbesondere für den Reparaturweg, der auf Kopieren intakter DNA als Vorlage beruht. Diese trägen, isolierten Brüche blieben viele Stunden lang ungelöst.
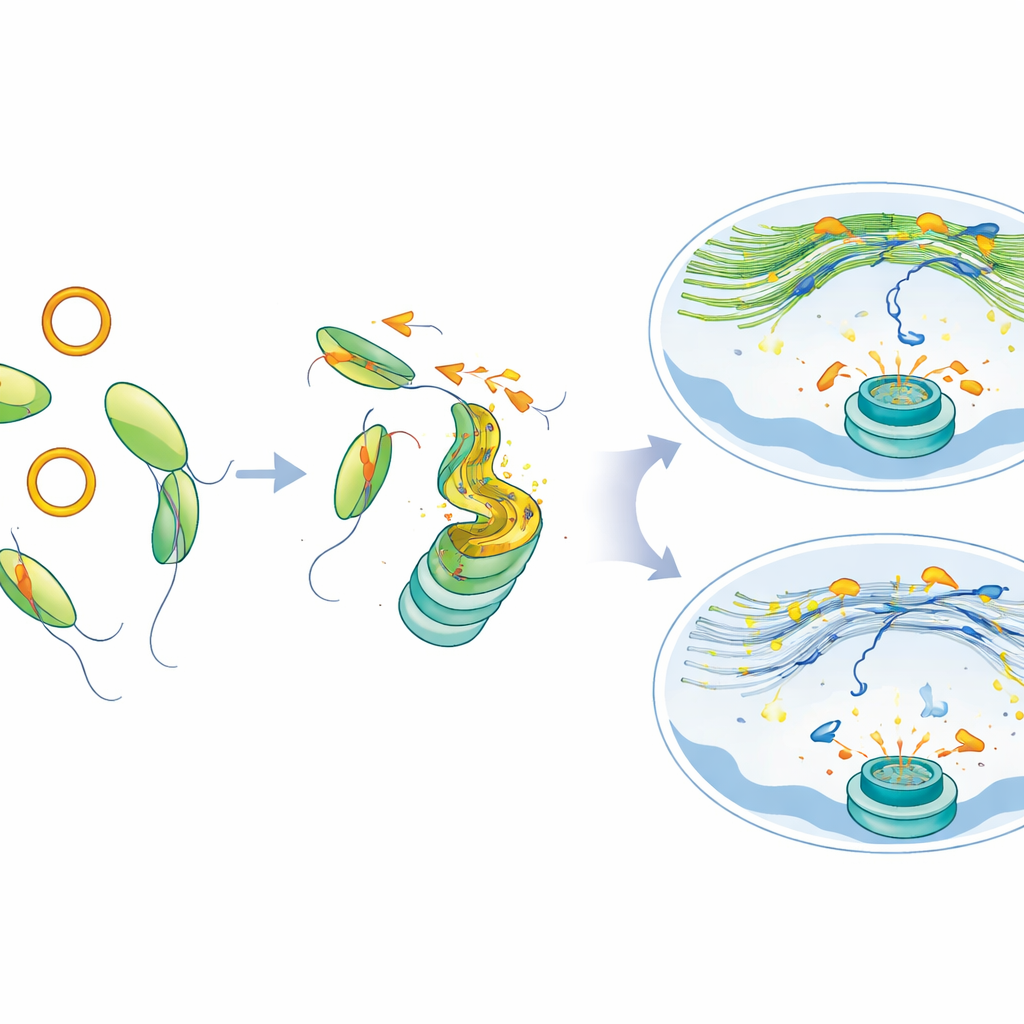
Von fehlerhafter Reparatur zur therapeutischen Chance
Zellen ohne MYH9 oder Zellen, die gezwungen wurden, vermehrt circATP9B zu produzieren, häuften persistente Schadensmarker und winzige zusätzliche Zellkerne an—Anzeichen für zerfallende Chromosomen. Diese Zellen wurden auch anfälliger für PARP-Inhibitoren, sowohl in Zellkulturen als auch in Maus-Tumormodellen. Das bedeutet, dass das Eingreifen in diesen Weg Krebszellen besonders verwundbar macht, wenn Medikamente zur Hemmung der DNA-Reparatur eingesetzt werden. Wichtig ist: Wenn die Forschenden MYH9 wiederherstellten oder circATP9B reduzierten, erholte sich das nukleäre Actin-Netzwerk, DNA‑Brüche bewegten und gruppierten sich wieder normaler, und die Reparatur verbesserte sich sogar in Zellen mit der SF3B1‑Mutation.
Was das für Patienten bedeutet
Vereinfacht gesagt zeigt diese Studie, dass eine häufige Krebs‑Mutation das interne «Eisenbahnsystem» der Zelle für die DNA-Reparatur sabotieren kann. Die SF3B1‑Mutation erhöht eine zirkuläre RNA, circATP9B, die wiederum das MYH9‑Motorprotein zerstört, das beim Organisieren der Actin‑Schienen im Kern hilft. Ohne stabile Schienen können beschädigte DNA‑Stellen nicht effizient zusammengeführt und repariert werden, wodurch Krebszellen genetisch instabil werden, aber zugleich stärker auf verbleibende Reparaturwege angewiesen sind. Diese Verwundbarkeit erklärt, warum Tumoren mit SF3B1‑Mutationen gut auf PARP‑Inhibitoren ansprechen, und deutet darauf hin, dass das Messen oder gezielte Beeinflussen von circATP9B und MYH9 eines Tages helfen könnte, DNA‑schädigende Therapien für Krebspatienten individuell anzupassen.
Zitation: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Schlüsselwörter: DNA-Reparatur, zirkuläre RNA, nukleäres Actin, SF3B1-Mutation, Krebstherapie