Clear Sky Science · ar
طفرة SF3B1 المرتبطة بالسرطان تُثبِّط إصلاح الـDNA عبر تعطيل تنظيم شبكة الأكتين النووية
كيف تحافظ الخلايا على سلامة الـDNA
يُتعرض الـDNA في خلايانا يومياً للشقوق والقطع والإجهاد بفعل الإشعاع والمواد الكيميائية والعمليات الأيضية الطبيعية. الخلايا السليمة جيدة عادة في رقع هذه الأضرار. لكن في العديد من السرطانات، يكون جزء من نظام الإصلاح هذا معطوباً جزئياً. تكشف هذه الدراسة عن سبب جديد ومفاجئ: طفرة واحدة شائعة في بروتين التوصيف (splicing) تُخرِّب شبكة دعم داخلية داخل نواة الخلية، مما يُبطئ إصلاح الـDNA ويسهم في نمو السرطان.
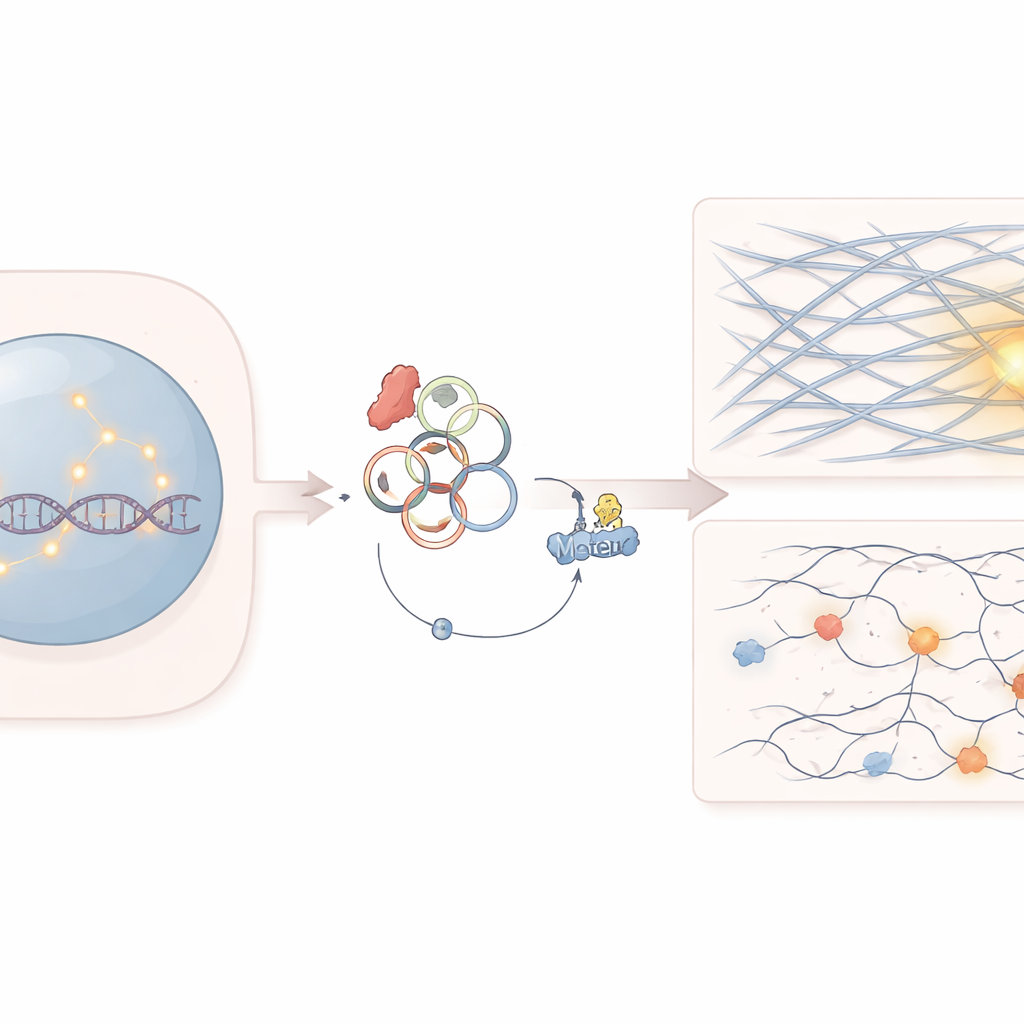
نقطة ضعف خفية في الخلايا السرطانية
تركز الدراسة على جين يُدعى SF3B1، الذي يساعد في معالجة رسائل الـRNA داخل الخلايا. طفرات في SF3B1 شائعة في عدد من سرطانات الدم والأورام الصلبة. كان الأطباء يعلمون أن هذه الطفرات تجعل الخلايا السرطانية حساسة بشكل غير عادي لبعض الأدوية التي تستهدف إصلاح الـDNA، مثل مثبطات PARP. ومع ذلك، لم يكن مفسراً تماماً لماذا تكافح هذه الخلايا في إصلاح الانكسارات، خاصة الانكسارات الأصعب إصلاحها التي تظهر في المناطق المكدسة بكثافة من الجينوم.
دور الـRNA الحلقي وبروتين محرك
اكتشف الباحثون أن طفرة SF3B1 تغيِّر طريقة ربط بعض جزيئات الـRNA، مما يزيد من إنتاج حمض نووي ريبوزي حلقي يُسمى circATP9B. على عكس الـRNA الخطي المعتاد، تُكوِّن الـRNAs الحلقية حلقات مغلقة ويمكن أن تعمل كإسفنج أو كمغريات للبروتينات. هنا، يرتبط circATP9B ببروتين محرك يُدعى MYH9، الذي يساعد عادة في تنظيم خيوط الأكتين—نفس الألياف البنيوية المعروفة بتشكيل الخلايا وتوليد انقباض العضلات. أظهر الفريق أن circATP9B يشجع على وسم MYH9 وتحطيمه، مما يخفض مستوياته دون تغيير تعبير الجين الخاص به.
تحطيم شبكة الطرق النووية
داخل النواة، يمكن للأكتين أن يتجمع إلى خيوط دقيقة تعمل كمسارات. بعد تلف الـDNA، يجب أن تتحرك الأجزاء المكسورة، خاصة في «الكروماتين المتراص» (heterochromatin)، على طول هذه المسارات إلى مناطق أكثر أماناً حيث يمكن أن يحدث إصلاح دقيق. باستخدام تصوير الخلايا الحية، راقب العلماء علامات متوهجة تُبرز شقوق الـDNA والأكتين النووي. عندما انخفضت مستويات MYH9، فشلت شبكة خيوط الأكتين النووية الغنية في التكوّن بشكل سليم بعد الإشعاع. ونتيجة لذلك، تحركت بؤر الـDNA المكسورة ببطء أكبر، قطعت مسافات أقصر، وتجمعت بكفاءة أقل، لا سيما في مسار الإصلاح الذي يعتمد على نسخ الشريط السليم كقالب. ظلت هذه الانكسارات البطيئة والمعزولة دون حل لساعات عديدة.
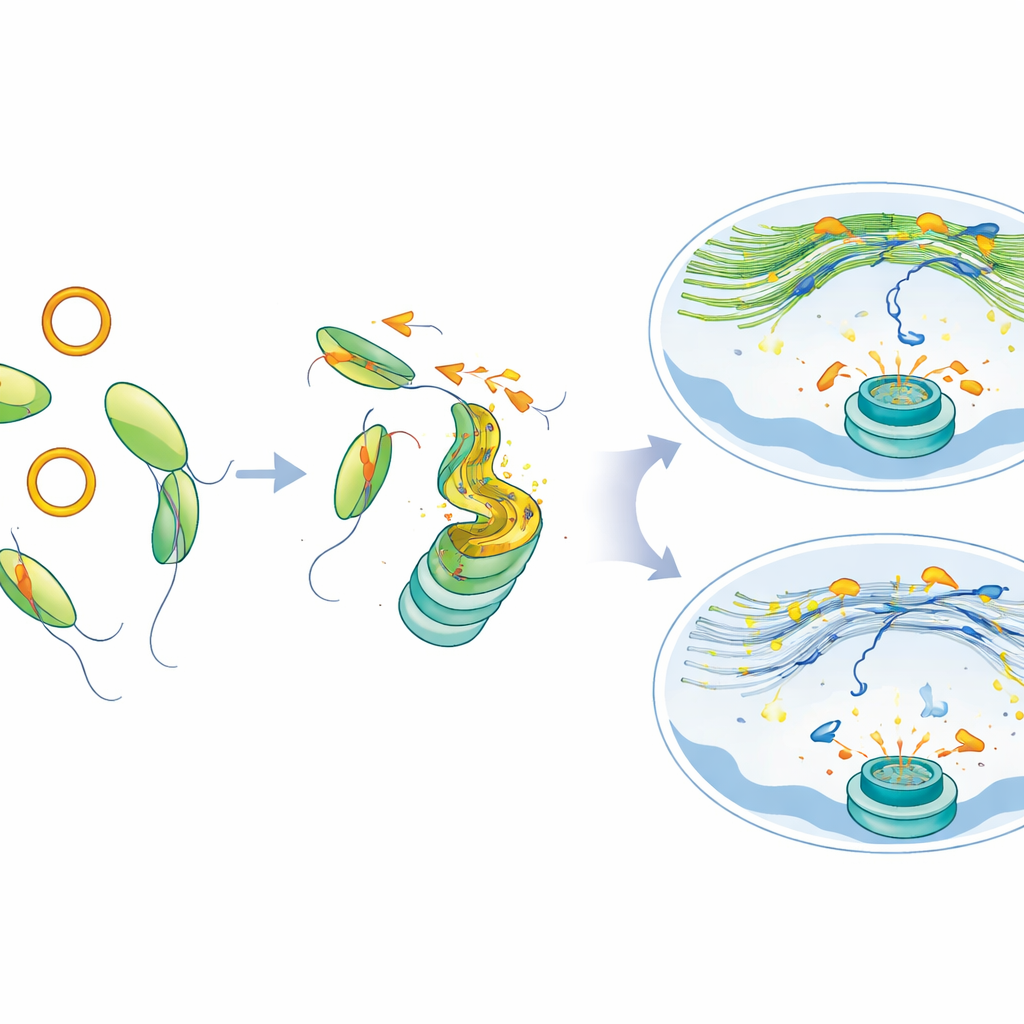
من إصلاح معطوب إلى فرصة علاجية
الخلايا التي تفتقر إلى MYH9، أو الخلايا التي أُجبرت على إنتاج فائض من circATP9B، تراكمت فيها علامات تلف مستمرة ونوى صغيرة إضافية—علامات على تفكك الكروموسومات. كما أصبحت هذه الخلايا أكثر عرضة لمثبطات PARP، سواء في الأطباق المختبرية أو في نماذج أورام الفئران، ما يعني أن التدخل في هذا المسار يجعل الخلايا السرطانية معرضة بشكل خاص عند استخدام أدوية تعطيل إصلاح الـDNA. ومن المهم أنه عندما أعاد الباحثون MYH9 أو قللوا مستويات circATP9B، استعادت شبكة الأكتين النووية تكوينها، وتحركت الانكسارات وتجمعت بشكل أقرب إلى الطبيعي، وتحسن الإصلاح حتى في الخلايا الحاملة لطفرة SF3B1.
ما الذي يعنيه هذا للمرضى
ببساطة، تكشف هذه الدراسة أن طفرة شائعة في السرطان يمكنها أن تُخرب «شبكة السكك الحديدية» الداخلية للخلايا اللازمة لإصلاح الـDNA. تزيد طفرة SF3B1 من مستوى الـRNA الحلقي circATP9B، الذي بدوره يدمر بروتين المحرك MYH9 الذي يساعد في تنظيم مسارات الأكتين داخل النواة. من دون مسارات ثابتة، لا يمكن جمع الانكسارات معاً وإصلاحها بكفاءة، ما يترك الخلايا السرطانية غير مستقرة جينياً لكنها أيضاً أتعس اعتماداً على طرق إصلاح متبقية. تساعد هذه النقطة الضعيفة في تفسير سبب استجابة الأورام الحاملة لطفرة SF3B1 جيداً لمثبطات PARP وتقترح أن قياس أو استهداف circATP9B وMYH9 قد يساعد في يوم ما على تخصيص العلاجات المدمرة للـDNA لمرضى السرطان.
الاستشهاد: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
الكلمات المفتاحية: إصلاح الحمض النووي, الحمض النووي الريبوزي الحلقي, الأكتين النووي, طفرة SF3B1, علاج السرطان