Clear Sky Science · tr
Kanserle ilişkili SF3B1 mutasyonu, nükleer aktin ağının düzenini bozarak DNA onarımını baskılıyor
Hücreler DNA’larını Nasıl Korur?
Her gün, hücrelerimizdeki DNA radyasyon, kimyasallar ve normal metabolizma nedeniyle yırtılır, kesilir ve hasar görür. Sağlıklı hücreler genellikle bu hasarları onarma konusunda oldukça iyidir. Ancak birçok kanserde bu onarım sistemi kısmen bozulmuştur. Bu çalışma şaşırtıcı yeni bir neden ortaya koyuyor: bir RNA işleme proteindeki tek, yaygın bir mutasyon hücre çekirdeği içindeki bir iç destek ağını bozar, DNA onarımını yavaşlatır ve kanserin ilerlemesine yardımcı olur.
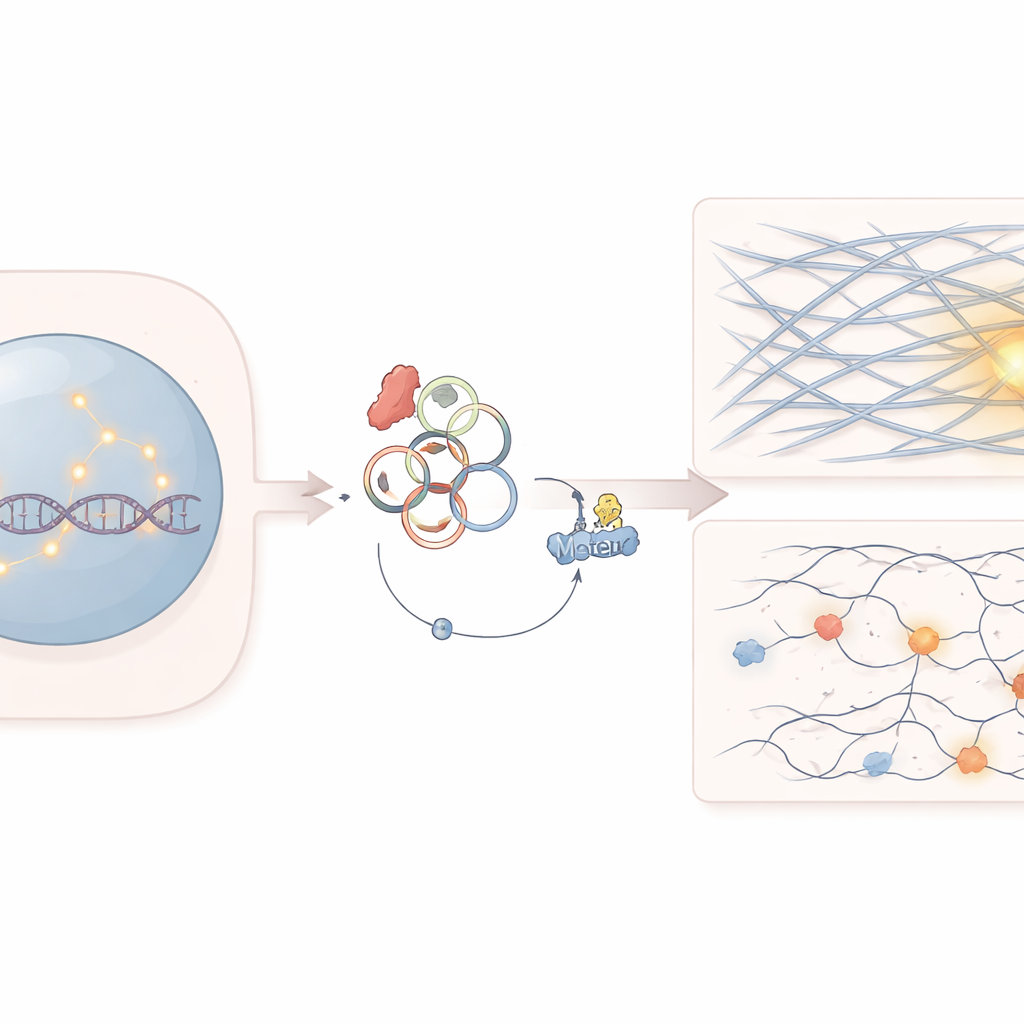
Kanser Hücrelerindeki Gizli Zayıf Nokta
Çalışmanın odağında SF3B1 adında bir gen var; bu gen hücrelerde RNA mesajlarının işlenmesine yardımcı olur. SF3B1’deki mutasyonlar birkaç kan kanseri ve katı tümörde yaygındır. Hekimler zaten bu mutasyonların kanser hücrelerini PARP inhibitörleri gibi DNA onarımını hedef alan bazı ilaçlara alışılmadık derecede hassas hale getirdiğini biliyordu. Ancak bu hücrelerin neden özellikle genomun sıkışık bölgelerinde ortaya çıkan ve onarılması daha zor kırılmalarla başa çıkmakta zorlandığı tam olarak anlaşılmamıştı.
Dairesel RNA ve Bir Motor Proteinin Rolü
Araştırmacılar, SF3B1 mutasyonunun bazı RNA molekullerinin birleştirilme biçimini değiştirdiğini ve circATP9B adlı bir dairesel RNA’nın üretimini artırdığını keşfettiler. Tipik doğrusal RNA’nın aksine, dairesel RNA’lar kapalı döngüler oluşturur ve proteinler için sünger veya yem görevi görebilirler. Burada circATP9B, normalde aktin filamentlerini organize etmeye yardımcı olan MYH9 adlı bir motor proteine bağlanıyor; aktin filamentleri hücreleri şekillendirmede ve kas kasılmasını sağlamakta bilinen yapısal liflerdir. Ekip, circATP9B’nin MYH9’u etiketlenmeye ve parçalanmaya yönlendirdiğini, böylece gen ekspresyonunu değiştirmeden MYH9 seviyelerini azalttığını gösterdi.
Nükleer Yol Ağının Bozulması
Çekirdek içinde aktin, ray gibi iş gören ince filamentlere birikebilir. DNA hasar gördüğünde, özellikle sıkışık "heterokromatin" bölgelerdeki kopan parçalar, doğru onarımın gerçekleşebileceği daha güvenli bölgelere bu raylar boyunca taşınmak zorundadır. Canlı hücre görüntülemesi kullanarak, bilim insanları DNA kırıklarını ve nükleer aktini vurgulayan parlayan işaretçileri izlediler. MYH9 azaldığında, radyasyondan sonra normalde oluşması beklenen zengin nükleer aktin ağı düzgün biçimde oluşmadı. Sonuç olarak, kırık DNA noktaları daha yavaş hareket etti, daha kısa mesafeler katetti ve özellikle sağlam DNA’yı şablon olarak kullanan onarım yoluyla ilişkili kümeleşme daha az verimli oldu. Bu yavaş ve izole kırılmalar saatlerce çözülmeden kaldı.
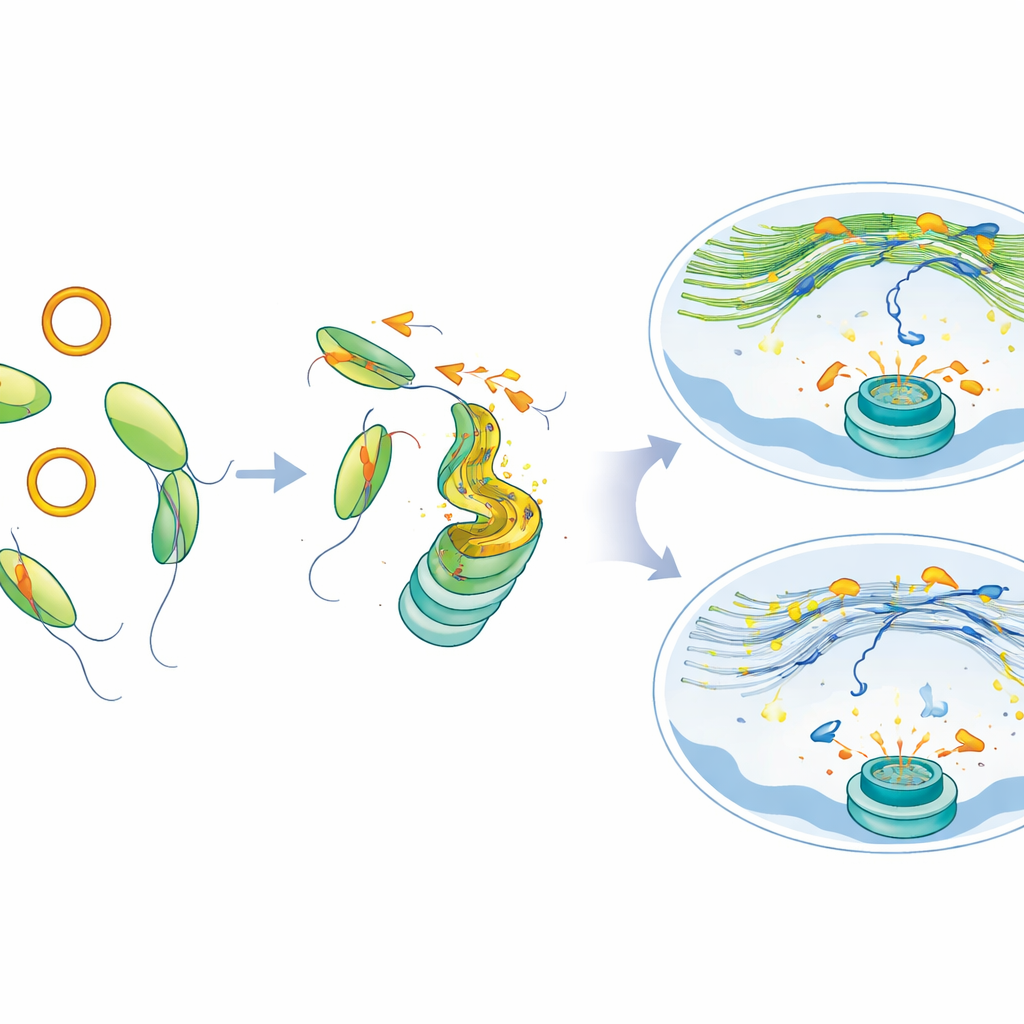
Hatalı Onarımdan Tedavi Fırsatına
MYH9 eksikliği olan hücreler veya aşırı circATP9B üretmeye zorlanan hücreler kalıcı hasar işaretleri ve küçük ekstra çekirdekler — kromozomların parçalandığının işaretleri — biriktirdi. Bu hücreler hem kültürde hem de fare tümör modellerinde PARP inhibitörlerine karşı daha hassas hale geldi; bu da bu yolun bozulmasının, DNA onarım ilaçları kullanıldığında kanser hücrelerini özellikle savunmasız bıraktığını gösteriyor. Önemli olarak, araştırmacılar MYH9’u geri getirdiklerinde veya circATP9B’yi azalttıklarında, nükleer aktin ağı toparlandı, DNA kırılmaları daha normal şekilde hareket etti ve kümelendi ve onarım SF3B1 mutasyonu taşıyan hücrelerde bile iyileşti.
Bu Hastalar İçin Ne Anlama Geliyor?
Basitçe söylemek gerekirse, bu çalışma yaygın bir kanser mutasyonunun hücrenin DNA onarımı için kullandığı iç “demiryolu sistemini” sabote edebileceğini ortaya koyuyor. SF3B1 mutasyonu, circATP9B adlı bir dairesel RNA’yı artırıyor; bu RNA da çekirdekteki aktin raylarını organize etmeye yardımcı olan MYH9 motor proteinini yok ediyor. Sağlam raylar olmadan, kırık DNA verimli şekilde bir araya getirilemez ve onarılamaz; bu da kanser hücrelerini genetik olarak istikrarsız bıraksa da kalan onarım yollarına daha bağımlı kılıyor. Bu zayıflık, SF3B1 mutasyonlu tümörlerin PARP inhibitörlerine iyi yanıt vermesini açıklamaya yardımcı oluyor ve circATP9B ile MYH9’un ölçülmesi veya hedeflenmesinin gelecekte DNA hasarına yol açan tedavileri kişiselleştirmede yardımcı olabileceğini gösteriyor.
Atıf: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Anahtar kelimeler: DNA onarımı, dairesel RNA, nükleer aktin, SF3B1 mutasyonu, kanser tedavisi