Clear Sky Science · es
La mutación asociada al cáncer en SF3B1 suprime la reparación del ADN al alterar la organización de la red de actina nuclear
Cómo las células mantienen su ADN en forma
Cada día, el ADN de nuestras células sufre cortes, roturas y tensiones por la radiación, químicos y el metabolismo normal. Las células sanas suelen ser muy eficaces reparando este daño. Pero en muchos cánceres, ese sistema de reparación está parcialmente dañado. Este estudio descubre una razón nueva y sorprendente: una única mutación frecuente en una proteína de empalme desbarata una red de soporte interna dentro del núcleo celular, ralentizando la reparación del ADN y favoreciendo el crecimiento tumoral.
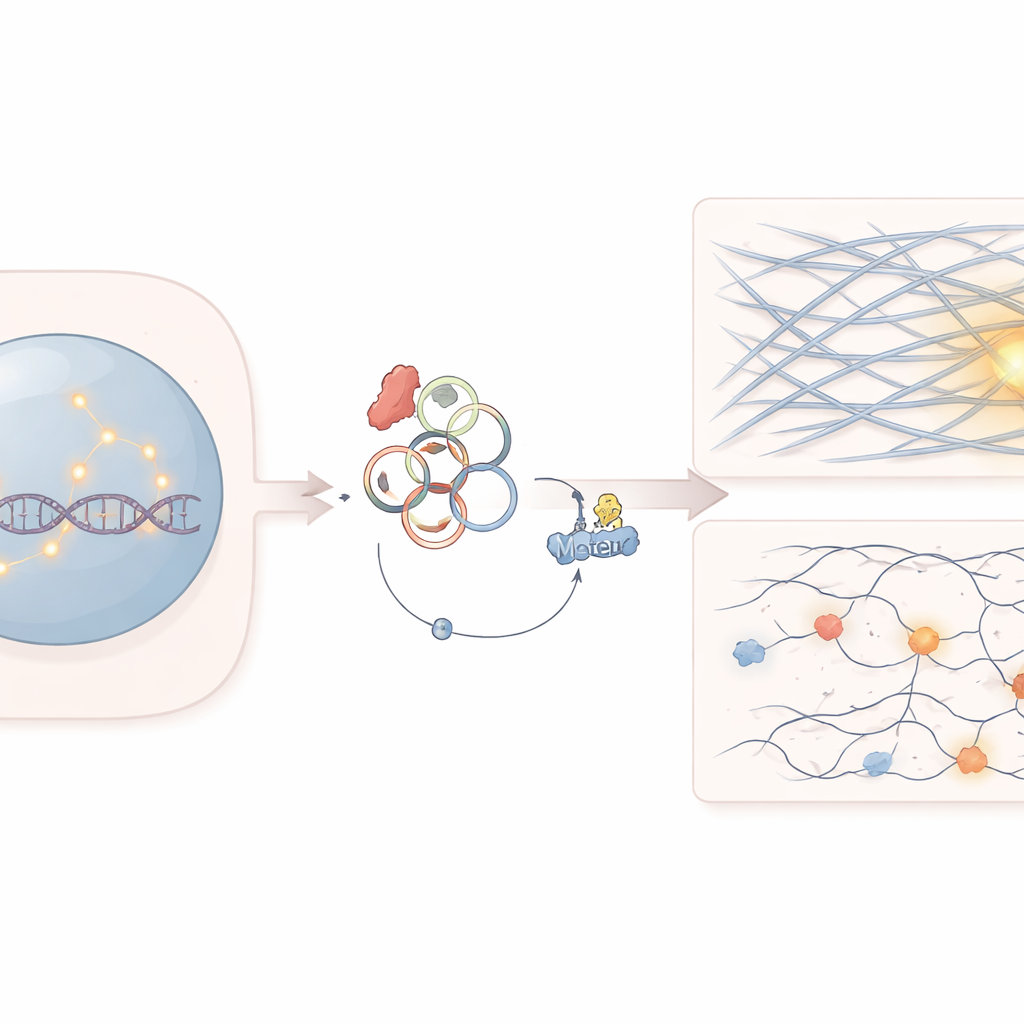
Un punto débil oculto en las células cancerosas
El trabajo se centra en un gen llamado SF3B1, que ayuda a procesar los mensajes de ARN en las células. Las mutaciones en SF3B1 son comunes en varias leucemias y tumores sólidos. Los médicos ya sabían que estas mutaciones hacen que las células cancerosas sean inusualmente sensibles a ciertos fármacos que atacan la reparación del ADN, como los inhibidores de PARP. Sin embargo, no se entendía del todo por qué estas células tienen dificultades para reparar roturas de ADN, especialmente las más difíciles que surgen en regiones densamente empaquetadas del genoma.
El papel del ARN circular y una proteína motora
Los investigadores descubrieron que la mutación en SF3B1 cambia la forma en que se cosen algunos ARN, aumentando la producción de un ARN circular llamado circATP9B. A diferencia del ARN lineal típico, los ARN circulares forman lazos cerrados y pueden actuar como esponjas o señuelos para proteínas. Aquí, circATP9B se une a una proteína motora llamada MYH9, que normalmente ayuda a organizar los filamentos de actina —el mismo tipo de fibras estructurales más conocidas por dar forma a las células y por la contracción muscular. El equipo demostró que circATP9B favorece el etiquetado y la degradación de MYH9, reduciendo sus niveles sin alterar la expresión génica.
Rompiendo la red viaria nuclear
Dentro del núcleo, la actina puede ensamblarse en finos filamentos que actúan como vías. Tras el daño en el ADN, los fragmentos rotos, sobre todo en la “heterocromatina” compacta, deben moverse por estas vías hacia zonas seguras donde puede realizarse una reparación precisa. Con microscopía de células vivas, los científicos siguieron marcadores fluorescentes que resaltan las roturas de ADN y la actina nuclear. Cuando MYH9 se redujo, la habitual y densa red de filamentos de actina nuclear no se formó adecuadamente tras la radiación. Como resultado, los puntos de rotura se movieron más despacio, recorrieron distancias menores y se agruparon con menos eficiencia, especialmente en la vía de reparación que depende de copiar ADN intacto como plantilla. Estas roturas lentas y aisladas permanecieron sin resolver durante muchas horas.
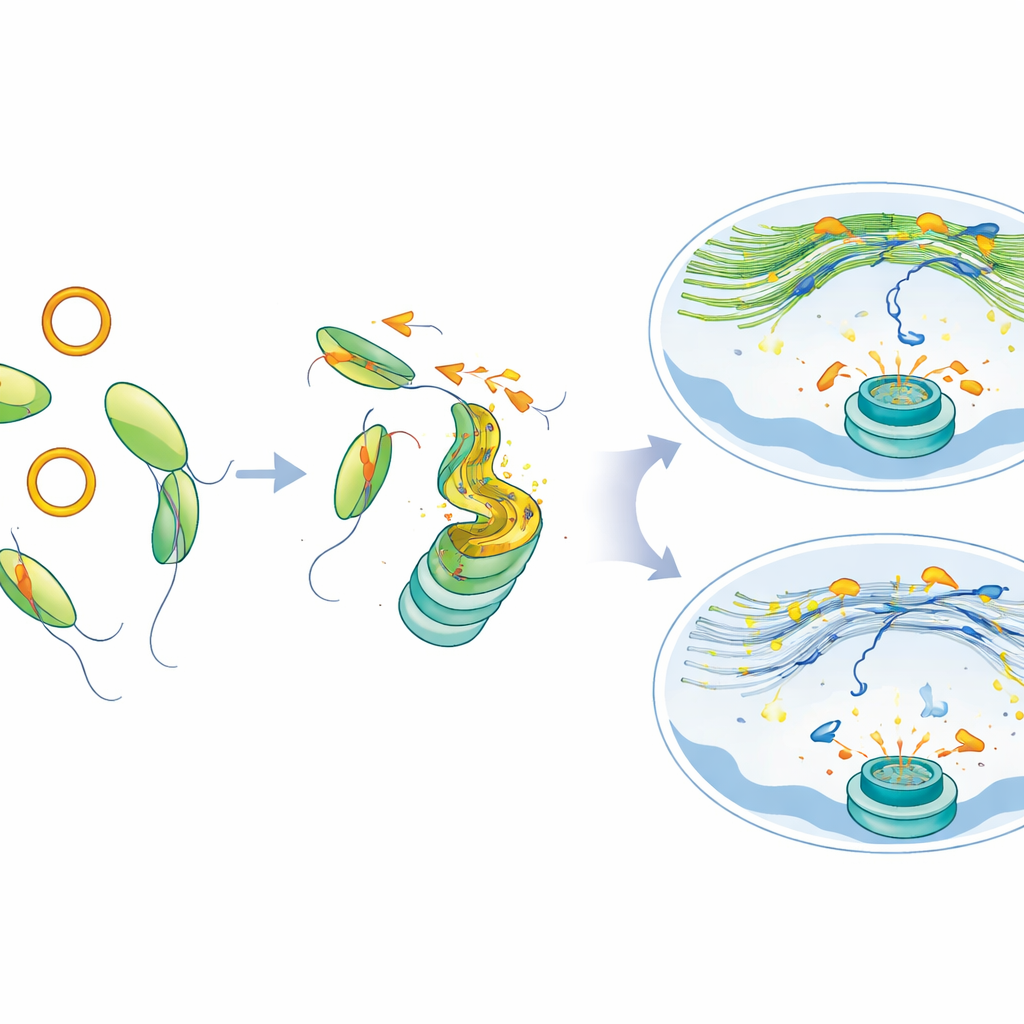
De la reparación defectuosa a una oportunidad terapéutica
Las células sin MYH9, o las forzadas a producir exceso de circATP9B, acumularon marcas persistentes de daño y pequeñas núcleos extra —signos de fragmentación cromosómica. Estas células también se volvieron más vulnerables a los inhibidores de PARP, tanto en cultivos como en modelos tumorales en ratón, lo que indica que interferir con esta vía deja a las células cancerosas especialmente expuestas cuando se usan fármacos que afectan la reparación del ADN. Importante, cuando los investigadores restauraron MYH9 o redujeron circATP9B, la red de actina nuclear se recuperó, las roturas de ADN se movieron y agruparon de forma más normal, y la reparación mejoró incluso en células con la mutación SF3B1.
Qué significa esto para los pacientes
En términos sencillos, este estudio revela que una mutación frecuente en cáncer puede sabotar el “sistema ferroviario” interno de la célula para la reparación del ADN. La mutación en SF3B1 aumenta un ARN circular, circATP9B, que a su vez destruye la proteína motora MYH9 que ayuda a organizar las vías de actina en el núcleo. Sin vías firmes, el ADN roto no puede reunirse y repararse con eficacia, dejando a las células cancerosas genéticamente inestables pero también más dependientes de las rutas de reparación que quedan. Esta vulnerabilidad ayuda a explicar por qué los tumores con mutaciones en SF3B1 responden bien a los inhibidores de PARP y sugiere que medir o dirigir circATP9B y MYH9 podría algún día ayudar a personalizar las terapias que dañan el ADN para los pacientes con cáncer.
Cita: Qian, R., Zhao, Z., Sun, X. et al. Cancer-associated SF3B1 mutation suppresses DNA repair by disrupting the organization of nuclear actin network. Cell Death Dis 17, 334 (2026). https://doi.org/10.1038/s41419-026-08569-5
Palabras clave: Reparación del ADN, ARN circular, actina nuclear, mutación SF3B1, terapia contra el cáncer