Clear Sky Science · zh
低剂量放疗与PD-1抑制联合,通过肿瘤中性粒细胞的抗肿瘤重编程在晚期非小细胞肺癌中实现持久生存
将机体的第一响应者转向对抗肺癌
大多数人把放疗和免疫疗法视为对抗癌症的两种独立武器。这项研究展示了如何通过精细调整放射剂量并与一种常用免疫疗法药物配合,重新编程一个出乎意料的盟友——中性粒细胞(一种白细胞)——以帮助晚期肺癌患者显著延长生存期。
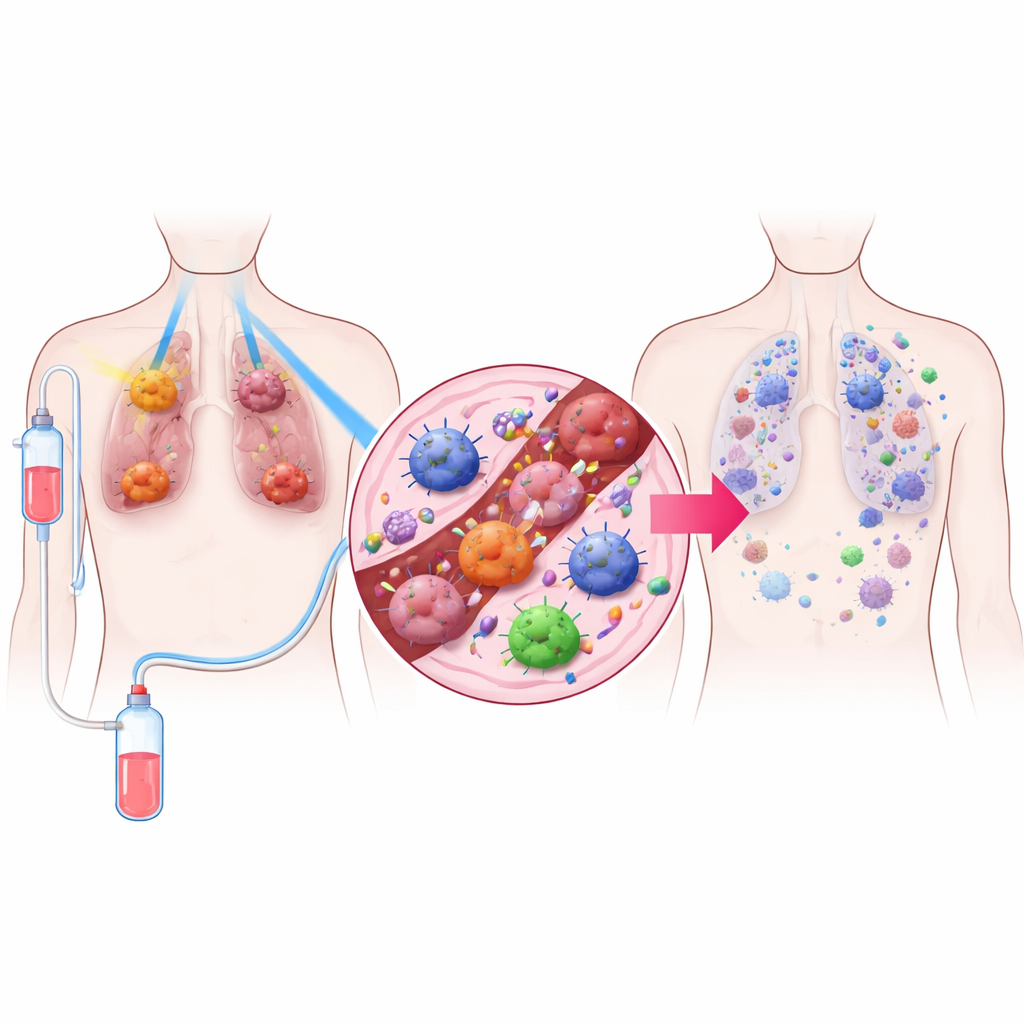
三部分治疗策略
研究人员设计了一种称为TRIDENT的治疗方案,结合了三种要素。首先,对大的肺肿瘤施以非常低剂量的放疗,这些剂量不足以直接杀死大量细胞,但能改变肿瘤微环境的行为。其次,对较小的肿瘤采用更熟悉的高剂量放疗以在局部消灭癌细胞。第三,患者接受PD‑1抑制药,一种解除T细胞抑制的免疫疗法。通过将这三部分结合,团队旨在既控制可见肿瘤,又激活全身性的免疫防御。
在晚期肺癌中显示出令人鼓舞的生存结果
在一项I期临床试验中,29名晚期非小细胞肺癌患者(既往未接受治疗且肿瘤表达PD‑L1)在未用化疗的情况下接受了TRIDENT治疗。随访超过五年,中位总生存期为51.3个月——远超单用免疫疗法或免疫疗法加化疗通常见到的约15–23个月。另一个采用TRIDENT类似方法的97人现实世界队列也显示出类似令人鼓舞的生存结果。多名患者无进展生存超过五年,提示该治疗能激发对肿瘤的持久免疫记忆。
低剂量放疗如何助力免疫系统
为了解该组合疗法为何有效,研究团队使用在身体两侧均有肿瘤的小鼠模型,模拟多灶转移。只有当低剂量放疗、高剂量放疗和PD‑1抑制同时使用时,肿瘤才不仅在高剂量照射部位缩小,远处病灶也出现缩小,表明发生了全身免疫应答。详细的单细胞分析显示,这一方案显著增加了进入远处肿瘤的中性粒细胞数量。与通常支持肿瘤的中性粒细胞不同,这些细胞产生炎性信号TNF‑α,并表现出专业免疫刺激子的特征,包括能够将肿瘤抗原呈递给T细胞并提供促进攻击的“启动”信号的分子。
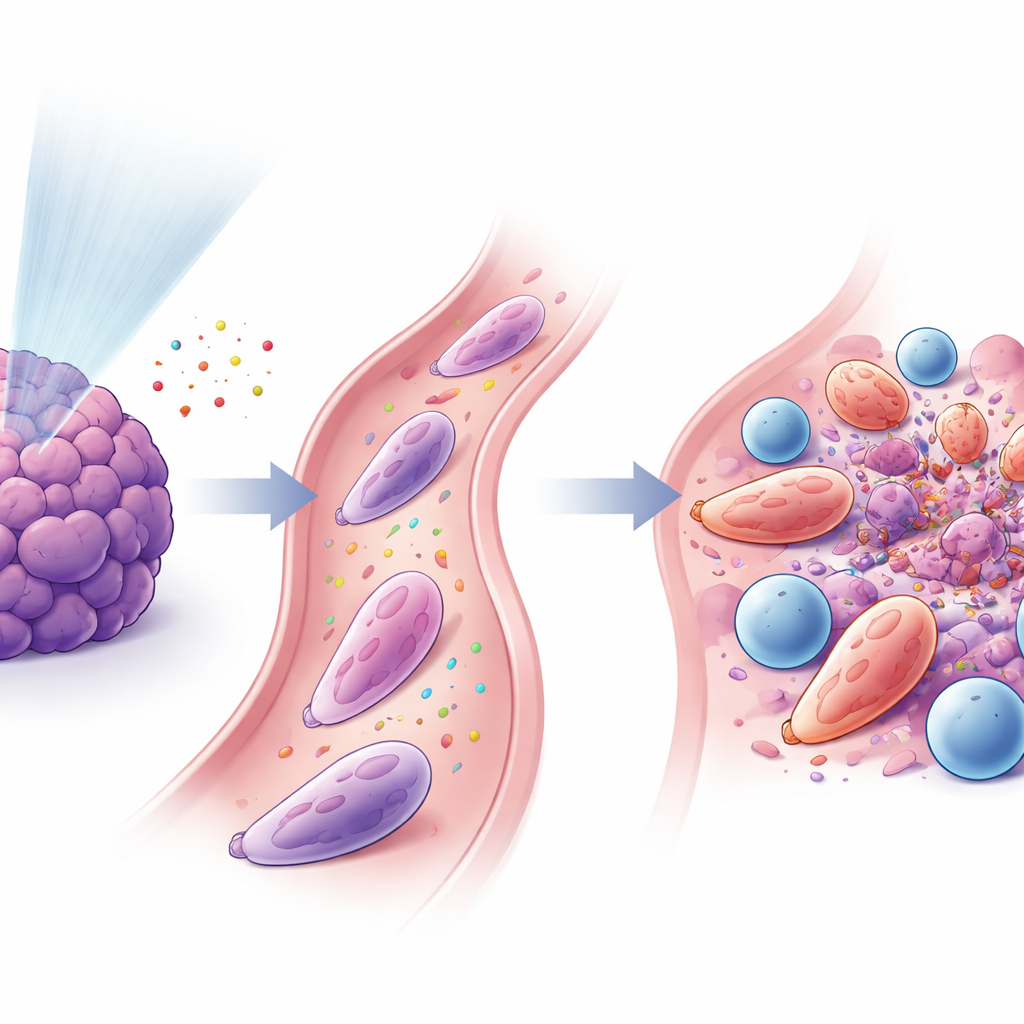
中性粒细胞与T细胞联手作战
研究发现,这些被重编程的中性粒细胞与杀伤性CD8+ T细胞密切相关。低剂量放疗后释放的信号通过称为CXCL–CXCR2的通路吸引中性粒细胞,其他因子包括GM‑CSF和干扰素‑γ有助于将其转化为抗肿瘤状态。被激活后,中性粒细胞表达黏附性表面蛋白(如ICAM‑1),与携带配对分子LFA‑1的T细胞紧密结合,形成类似“免疫突触”的近距离接触界面。在体外培养中,这些中性粒细胞增强了T细胞的激活与增殖,并帮助T细胞更有效地杀死癌细胞。当研究者将这些特化的中性粒细胞转移到带瘤小鼠体内,尤其是与PD‑1抑制联合使用时,肿瘤缩小且生存改善。
来自病人肿瘤和血液的证据
团队还使用先进的空间基因映射工具检查了患者在TRIDENT治疗前后的肿瘤样本。治疗后,肿瘤出现了这些富含TNF‑α的中性粒细胞与活化的CD8+ T细胞聚集的区域,并伴有强烈的抗原处理与免疫激活相关信号。在多组接受免疫疗法的肺癌患者数据集中,与这些中性粒细胞相关的基因特征更高者通常具有更长的无进展时间。在一小组接受放疗与PD‑1抑制联合治疗的观察性患者中,治疗应答者血液中的活化中性粒细胞明显增加,而无应答者则无此变化。
对肺癌患者意味着什么
对于晚期肺癌患者而言,这些发现表明放疗的给法可能与放疗的剂量一样重要。通过将对大肿瘤施以小剂量、调节免疫的照射与标准高剂量放疗及PD‑1抑制结合,TRIDENT似乎能将中性粒细胞从可能的肿瘤帮凶转变为T细胞的强大伙伴。这种中性粒细胞—T细胞的协同工作与持久的肿瘤控制和更好的生存相关,使TRIDENT成为目前正进入更大规模随机试验验证的有前景策略。该研究还提示,活化的中性粒细胞本身可能成为未来的治疗靶点,并可作为简单的血液生物标志物,帮助预测谁最可能从放射免疫联合疗法中受益。
引用: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
关键词: 肺癌, 放疗, 免疫疗法, 中性粒细胞, PD-1抑制