Clear Sky Science · he
קרינה במינון נמוך מסנכרנת עם חסימת PD-1 להשגת הישרדות ממושכת בסרטן ריאה לא‑קטיני מתקדם באמצעות תכנות נויטרופילים אנטי‑גידוליים
להפנות את המגיבים הראשונים של הגוף נגד סרטן הריאה
רוב האנשים נוטים לראות בקרינה ובאימונותרפיה כלי נשק נפרדים במאבק בסרטן. המחקר הזה מראה כיצד כיוונון מדוד של מינוני הקרינה ויצירת שילוב עם תרופת אימונותרפיה נפוצה יכולים לתכנת מחדש בעל ברית מפתיע — נויטרופילים, סוג של תאי דם לבנים — כדי לעזור לחולים עם סרטן ריאה מתקדם לחיות זמן רב יותר.
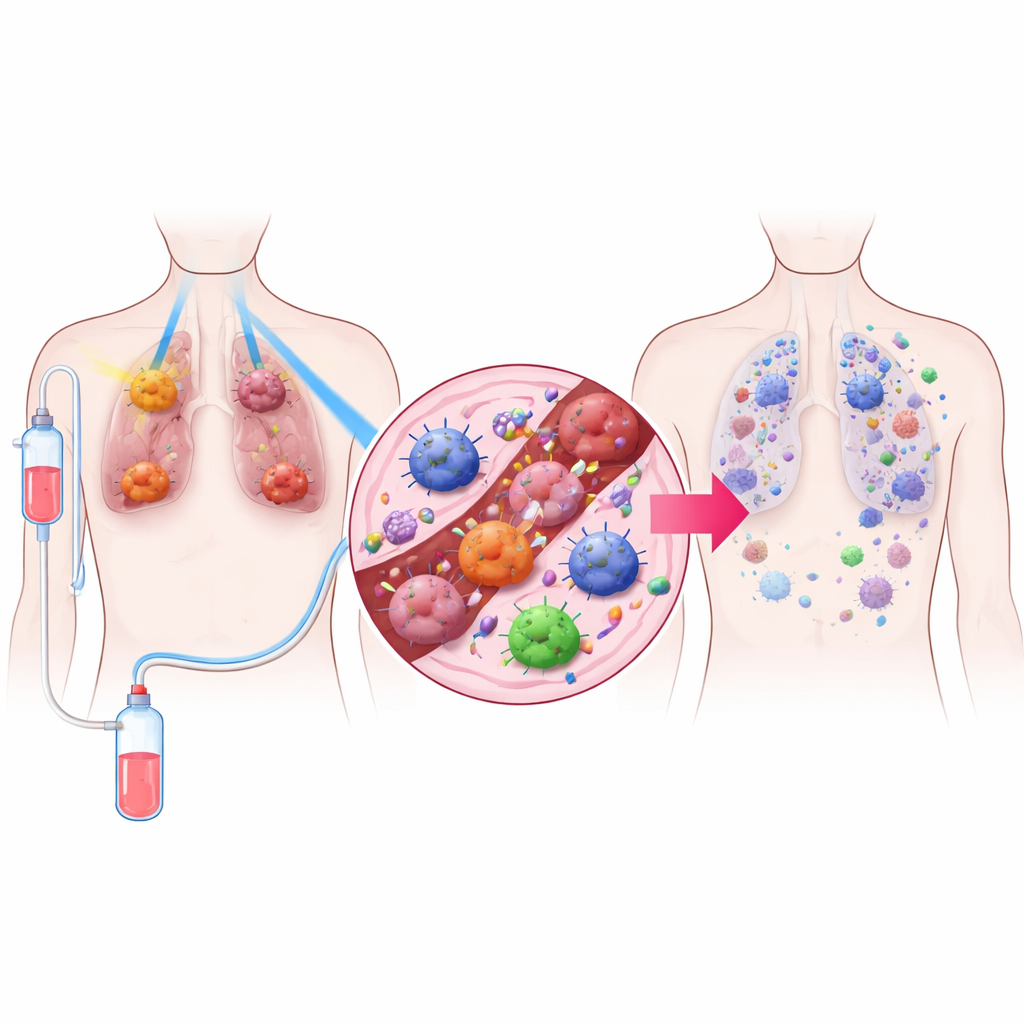
אסטרטגיית טיפול בשלושה חלקים
החוקרים תיכננו טיפול שהם מכנים TRIDENT, שמשלב שלושה מרכיבים. ראשית, גידולים ריאתיים גדולים מקבלים מינונים נמוכים מאוד של קרינה, חלשים מדי כדי להרוג תאים רבים ישירות אך מספקים שינוי בהתנהגות סביבת הגידול. שנית, גידולים קטנים יותר מופגזים בקרינה במינון גבוה יותר, המוכרת להשמדה מקומית של סרטן. שלישית, המטופלים מקבלים תרופה החוסמת PD‑1, סוג של אימונותרפיה שמסירה את הבלמים מהתאים הטי של המערכת החיסונית. על ידי שילוב שלושת החלקים האלה, הצוות שאף לשלוט בגידולים הנראים ולהעיר את ההגנות החיסוניות בכל הגוף.
הישרדות מבטיחה בסרטן ריאה מתקדם
בניסוי קליני פאזה I טופלו 29 בני אדם עם סרטן ריאה לא‑קטיני מתקדם שלא קיבלו טיפול קודם וגידולם הביטח את חלבון PD‑L1, בקבלת TRIDENT ללא כימותרפיה. עם יותר מחמש שנות מעקב, הישרדות אמצעית כוללת עמדה על 51.3 חודשים — הרבה יותר מהכ־15–23 חודשים שמקובל לראות עם אימונותרפיה בלבד או אימונותרפיה פלוס כימותרפיה. קבוצת עולם‑שמני נפרדת של 97 מטופלים שקיבלו גישה דומה ל‑TRIDENT הראתה הישרדות מעודדת דומה. כמה מטופלים נותרו ללא התקדמות במשך למעלה מחמש שנים, מה שמרמז שהטיפול יכול להצית זיכרון חיסוני מתמשך נגד הסרטן.
כיצד קרינה במינון נמוך מסייעת למערכת החיסון
כדי להבין מדוע השילוב הזה עובד, הצוות פנה למודלים בעכברים עם גידולים בשני צדי הגוף, המדמים התפשטות לאתרים מרובים. רק כששולבו יחד קרינה במינון נמוך, קרינה במינון גבוה וחסימת PD‑1 נצפו הקטנות של גידולים לא רק באתרים שקיבלו את המינון הגבוה, אלא גם באתרים רחוקים — סימן לתגובה חיסונית מערכתית. ניתוחים תאי‑יחיד מפורטים הראו שהמערכת הזו הגדילה במידה ניכרת את מספר הנויטרופילים שנכנסו לגידולים מרוחקים אלה. בשוני מהנויטרופילים התומכים הרגילים בגידול, תאים אלה ייצרו את האות הדלקתי TNF‑α והציגו תכונות של מאיצי חיסון מקצועיים, כולל מולקולות שמאפשרות להם להציג חלקי גידול לתאי T ולספק אותות "צא" להתקפה.
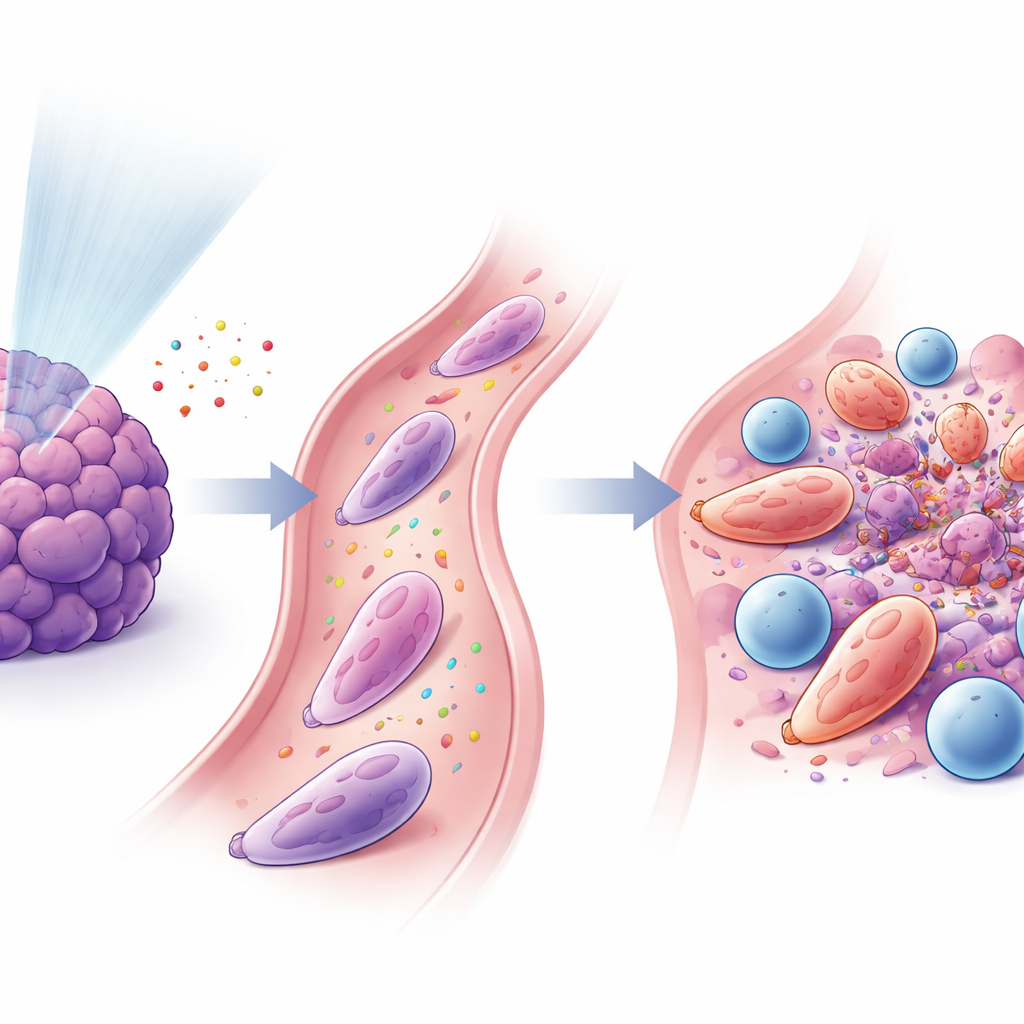
נויטרופילים ותאי T חוברים לכוח
המחקר מצא שנויטרופילים מתוכנתים מחדש אלה ותאי CD8+ קטלניים היו קשורים זה בזה באופן הדוק. אותות שמשתחררים לאחר קרינה במינון נמוך משכו נויטרופילים דרך מסלול הידוע כ‑CXCL–CXCR2, ופקטורים נוספים, כולל GM‑CSF ואינטרפרון‑γ, סייעו להפכם למצב אנטי‑גידולי. לאחר הפעלה, נויטרופילים הביטאו חלבוני משטח דביקים (כמו ICAM‑1) שאילצו אותם להיאחז עם תאי T (הנושאים את השותף התואם LFA‑1), ויצרו ממשקי מגע צמודים בדומה ל"סינפסות חיסוניות". במנות מעבדה, נויטרופילים אלה הגבירו את הפעלת תאי T, את חלוקתם וסייעו לתאי T להרוג תאי סרטן ביעילות רבה יותר. כאשר מדענים העבירו נויטרופילים מתמחים אלה לעכברים נושאי גידולים, במיוחד יחד עם חסימת PD‑1, הגידולים התקטנו וההישרדות השתפרה.
עדויות מתוך גידולים ודם של חולים
הצוות גם בחן דגימות גידול של מטופלים לפני ואחרי TRIDENT באמצעות כלי מיפוי גנים מרחביים מתקדמים. לאחר הטיפול הופיעו בגידולים מקבצים שבהם נויטרופילים עשירים ב‑TNF‑α ותאי CD8+ פעילים התקבצו יחד, יחד עם אותות חזקים הקשורים לעיבוד אנטיגן ולפעילות חיסונית. במסדי נתונים מרובים של חולי ריאה שטופלו באימונותרפיה, רמות גבוהות יותר של חתימת גנים הקשורה לנויטרופילים אלה היו משויכות לזמן ארוך יותר לפני החמרת המחלה. בקבוצה תצפיתית קטנה של מטופלים שקיבלו קרינה משולבת וחסימת PD‑1, המגיבים הראו עליות ברורות בנויטרופילים מactווים בדם שלהם, בעוד שלא‑מגיבים לא הראו שינויים כאלה.
מה משמעות הדבר עבור חולי סרטן ריאה
עבור אדם עם סרטן ריאה מתקדם, הממצאים האלה מרמזים שיותר חשוב לא פחות מאיך קרינה ניתנת — כלומר האופן והחלוקה שלה — מאשר רק הכמות. על‑ידי שילוב מינונים קטנים המכוונים לכוונון המערכת החיסונית בגידולים גדולים עם קרינה סטנדרטית במינון גבוה וחסימת PD‑1, נראה כי TRIDENT הופך את הנויטרופילים מייחידים פוטנציאליים של הגידול לשותפים רבי עוצמה של תאי T. שיתוף הפעולה הזה בין נויטרופילים ותאי‑T מקושר לשליטה ממושכת בגידול ולהישרדות טובה יותר, מה שהופך את TRIDENT לאסטרטגיה מבטיחה הנבחנת כיום בניסויים אקראיים רחבי היקף. העבודה גם מצביעה על נויטרופילים מופעלים כמטרות טיפול עתידיות אפשריות וכמדדים פשוטים מבוססי דם לחיזוי מי צפוי להרוויח מהרדיואימונותרפיה.
ציטוט: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
מילות מפתח: סרטן ריאה, רדיותרפיה, אימונותרפיה, נויטרופילים, חסימת PD-1