Clear Sky Science · es
La radioterapia de baja dosis actúa en sinergia con el bloqueo de PD-1 para lograr una supervivencia duradera en NSCLC avanzado mediante la reprogramación antitumoral de neutrófilos
Convertir a las primeras defensas del cuerpo contra el cáncer de pulmón
La mayoría de la gente piensa en la radiación y la inmunoterapia como armas separadas contra el cáncer. Este estudio muestra cómo ajustar con cuidado las dosis de radiación y combinarlas con un fármaco inmunoterapéutico popular puede reprogramar a un aliado inesperado: los neutrófilos, un tipo de glóbulo blanco, para ayudar a que pacientes con cáncer de pulmón avanzado vivan mucho más tiempo.
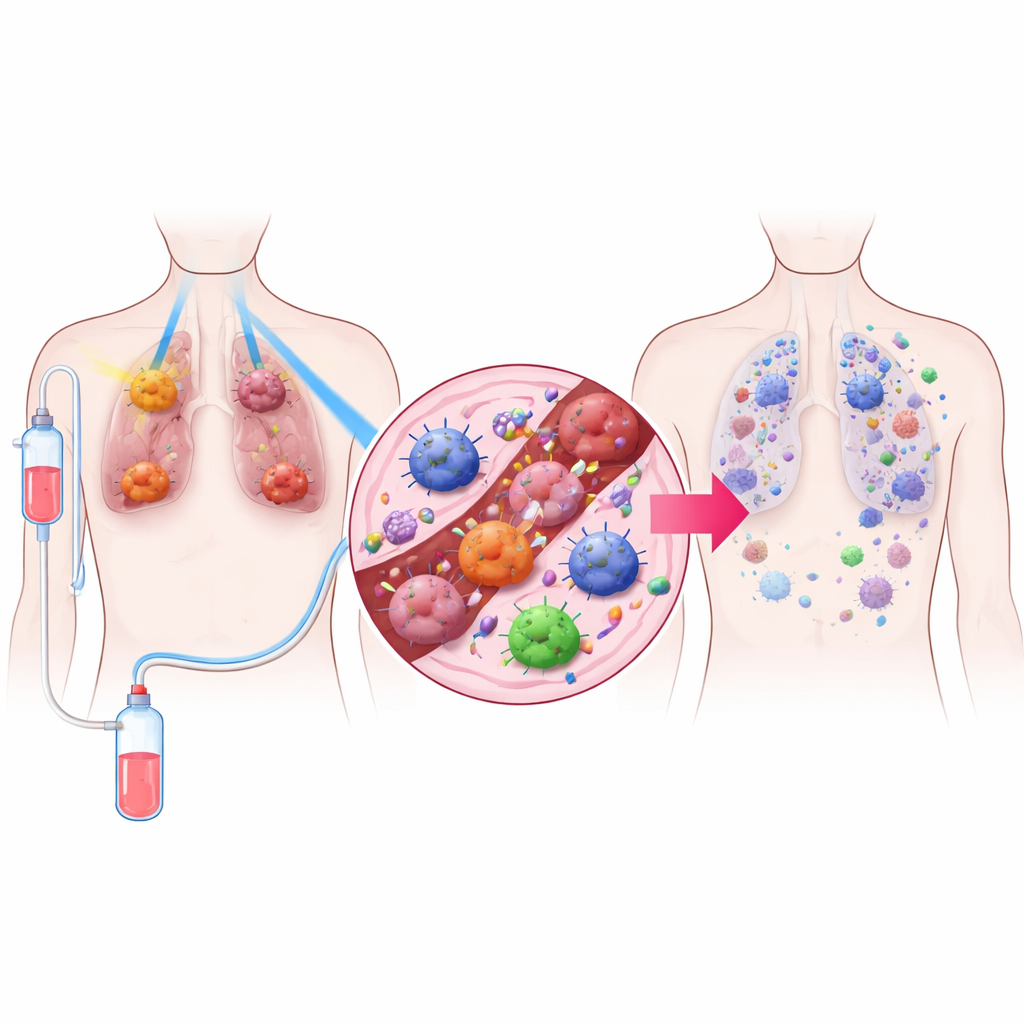
Una estrategia de tratamiento en tres partes
Los investigadores diseñaron un tratamiento que denominan TRIDENT, que combina tres elementos. Primero, los tumores pulmonares grandes reciben dosis muy bajas de radiación que son demasiado débiles para matar muchas células de forma directa, pero que pueden cambiar el comportamiento del microambiente tumoral. Segundo, los tumores más pequeños se tratan con la radiación de alta dosis más conocida, usada para destruir el cáncer de forma local. Tercero, los pacientes reciben un fármaco que bloquea PD‑1, un tipo de inmunoterapia que quita los frenos a las células T del sistema inmune. Al mezclar estas tres partes, el equipo pretendía controlar los tumores visibles y, al mismo tiempo, activar las defensas inmunitarias del cuerpo a lo largo de todo el organismo.
Supervivencia prometedora en cáncer de pulmón avanzado
En un ensayo clínico de fase I, 29 personas con cáncer de pulmón no microcítico avanzado que no habían recibido tratamiento previo y cuyos tumores expresaban la proteína PD‑L1 recibieron TRIDENT sin quimioterapia. Con más de cinco años de seguimiento, la supervivencia global mediana fue de 51,3 meses, mucho más larga que los aproximadamente 15–23 meses que se suelen observar con inmunoterapia estándar sola o con inmunoterapia más quimioterapia. Un grupo adicional de la práctica clínica real, de 97 pacientes tratados con un enfoque similar a TRIDENT, mostró una supervivencia igualmente alentadora. Varios pacientes permanecieron libres de progresión por más de cinco años, lo que sugiere que el tratamiento puede inducir memoria inmune duradera contra el cáncer.
Cómo la radiación de baja dosis ayuda al sistema inmune
Para entender por qué funciona esta combinación, el equipo recurrió a modelos murinos con tumores en ambos lados del cuerpo, imitando la diseminación a múltiples sitios. Solo cuando se usaron conjuntamente radiación de baja dosis, radiación de alta dosis y bloqueo de PD‑1, los tumores se redujeron no solo donde se aplicaron las dosis altas, sino también en sitios distantes, lo que indica una respuesta inmune sistémica. Los análisis detallados de una sola célula revelaron que este régimen aumentó considerablemente el número de neutrófilos que penetraban en esos tumores distantes. A diferencia de los neutrófilos que suelen apoyar al tumor, estas células producían la señal inflamatoria TNF‑α y mostraban rasgos de estimuladores inmunitarios profesionales, incluidas moléculas que les permiten presentar fragmentos del tumor a las células T y proporcionar señales de “adelante” para el ataque.
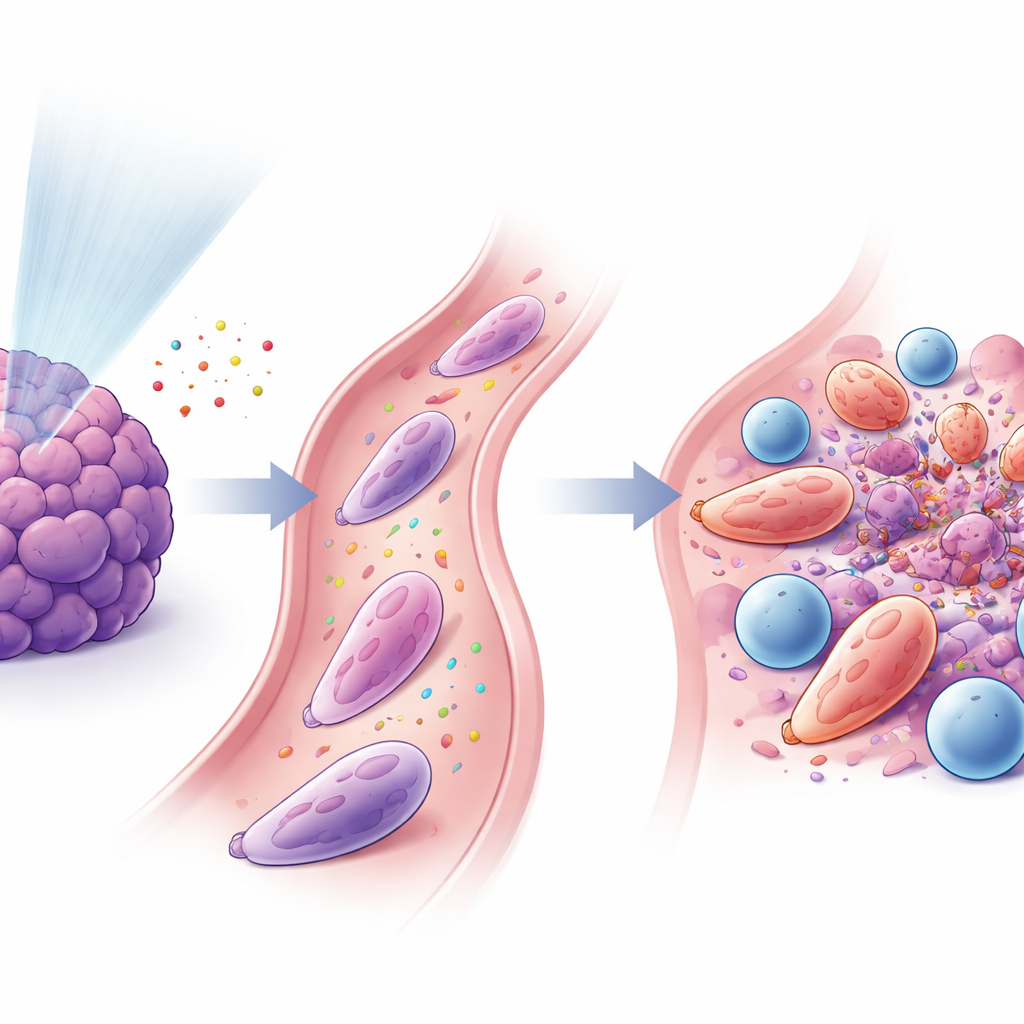
Neutrófilos y células T unen fuerzas
El estudio halló que estos neutrófilos reprogramados y las células T CD8+ citotóxicas estaban estrechamente relacionados. Las señales liberadas tras la radiación de baja dosis atrajeron neutrófilos mediante una vía conocida como CXCL–CXCR2, y otros factores, incluidos GM‑CSF e interferón‑γ, ayudaron a convertirlos a un estado antitumoral. Una vez activados, los neutrófilos expresaron proteínas adhesivas en la superficie (como ICAM‑1) que los unían a las células T (que portan la pareja correspondiente LFA‑1), formando interfaces de contacto estrecho similares a sinapsis inmunes. En placas de laboratorio, estos neutrófilos potenciaron la activación y proliferación de las células T y ayudaron a las células T a matar las células cancerosas con mayor eficacia. Cuando los científicos transfirieron esos neutrófilos especializados a ratones portadores de tumores, especialmente junto con el bloqueo de PD‑1, los tumores se redujeron y mejoró la supervivencia.
Pruebas a partir de tumores y sangre de pacientes
El equipo también examinó muestras tumorales de pacientes antes y después de TRIDENT usando herramientas avanzadas de cartografía espacial de genes. Tras el tratamiento, los tumores mostraron focos donde estos neutrófilos ricos en TNF‑α y células T CD8+ activas se agrupaban, junto con señales fuertes relacionadas con el procesamiento de antígenos y la activación inmune. En múltiples conjuntos de datos de pacientes con cáncer de pulmón tratados con inmunoterapia, niveles más altos de una firma génica vinculada a estos neutrófilos se asociaron con un tiempo más largo antes del empeoramiento del cáncer. En un pequeño grupo observacional de pacientes que recibieron radiación combinada y bloqueo de PD‑1, los respondedores mostraron incrementos claros de neutrófilos activados en su sangre, mientras que los no respondedores no lo hicieron.
Qué significa esto para las personas con cáncer de pulmón
Para alguien con cáncer de pulmón avanzado, estos hallazgos sugieren que la forma en que se administra la radiación puede ser tan importante como la cantidad. Al combinar dosis pequeñas que ajustan la respuesta inmune en tumores grandes con la radiación estándar de alta dosis y el bloqueo de PD‑1, TRIDENT parece convertir a los neutrófilos de posibles cómplices del tumor en poderosos compañeros de las células T. Esta colaboración entre neutrófilos y células T se vincula con un control tumoral duradero y una mejor supervivencia, lo que convierte a TRIDENT en una estrategia prometedora que ahora se está probando en ensayos aleatorizados más amplios. El trabajo también señala a los neutrófilos activados como posibles futuros dianas terapéuticas y como marcadores sencillos basados en sangre para ayudar a predecir quién es más probable que se beneficie de la radioinmunoterapia.
Cita: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
Palabras clave: cáncer de pulmón, radioterapia, inmunoterapia, neutrófilos, bloqueo de PD-1