Clear Sky Science · ru
Низкодозная лучевая терапия синергирует с блокадой PD-1, обеспечивая долговечное выживание при позднем НМРЛ за счёт программирования противоопухолевых нейтрофилов
Обращая первых реагентов организма против рака легких
Большинство людей воспринимают радиацию и иммунотерапию как отдельные средства борьбы с раком. Это исследование показывает, как тщательная настройка доз облучения и сочетание их с широко применяемым иммунотерапевтическим препаратом может перепрограммировать неожиданного союзника — нейтрофилы, тип лейкоцитов — чтобы помочь пациентам с распространённым раком легких жить значительно дольше.
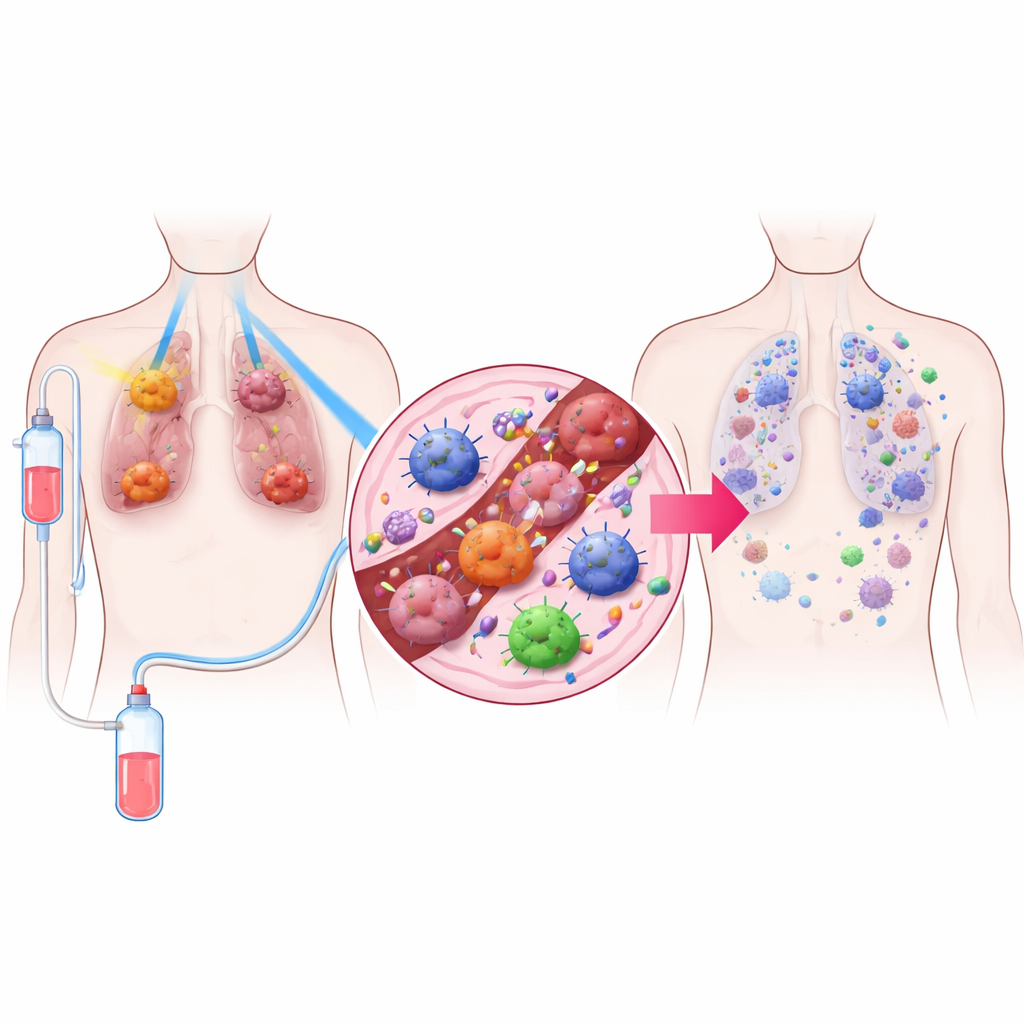
Трёхкомпонентная стратегия лечения
Исследователи разработали лечение, которое называют TRIDENT, объединяющее три элемента. Во-первых, крупные легочные опухоли получают очень низкие дозы облучения, которые слишком слабы, чтобы напрямую убивать большое число клеток, но способны изменить поведение опухолевого микроокружения. Во-вторых, более мелкие опухоли облучают привычными высокими дозами, используемыми для локального разрушения рака. В-третьих, пациенты получают препарат, блокирующий PD‑1, вид иммунотерапии, снимающей «тормоза» с Т-клеток. Сочетая эти три компонента, команда стремилась как контролировать видимые опухоли, так и пробудить иммунную защиту по всему организму.
Многообещающее выживание при распространённом раке легких
В фазе I клинического исследования 29 человек с распространённым немелкоклеточным раком легкого, ранее не получавших лечение и чьи опухоли экспрессировали белок PD‑L1, получили TRIDENT без химиотерапии. При наблюдении свыше пяти лет медиана общей выживаемости составила 51,3 месяца — значительно больше по сравнению с примерно 15–23 месяцами, обычно наблюдаемыми при стандартной иммунотерапии или иммунотерапии в сочетании с химиотерапией. Отдельная реальная когорта из 97 пациентов, лечившихся по схеме, похожей на TRIDENT, показала аналогично обнадёживающие результаты по выживанию. Некоторые пациенты оставались без прогрессирования более пяти лет, что указывает на способность лечения вызывать долговременную иммунную память против рака.
Как низкая доза облучения помогает иммунной системе
Чтобы понять, почему это сочетание работает, команда обратилась к модельным мышам с опухолями по обе стороны тела, имитируя распространение в несколько очагов. Только при совместном применении низкодозного облучения, высокодозного облучения и блокады PD‑1 опухоли уменьшались не только в местах, облучённых высокими дозами, но и в отдалённых очагах, что указывает на системный иммунный ответ. Детальные одноклеточные анализы показали, что эта схема значительно увеличивала количество нейтрофилов, проникающих в отдалённые опухоли. В отличие от обычно поддерживающих опухоль нейтрофилов, эти клетки продуцировали провоспалительный сигнал TNF‑α и проявляли признаки профессиональных стимуляторов иммунитета, включая молекулы, позволяющие им представлять фрагменты опухоли Т‑клеткам и подавать «сигналы на атаку».
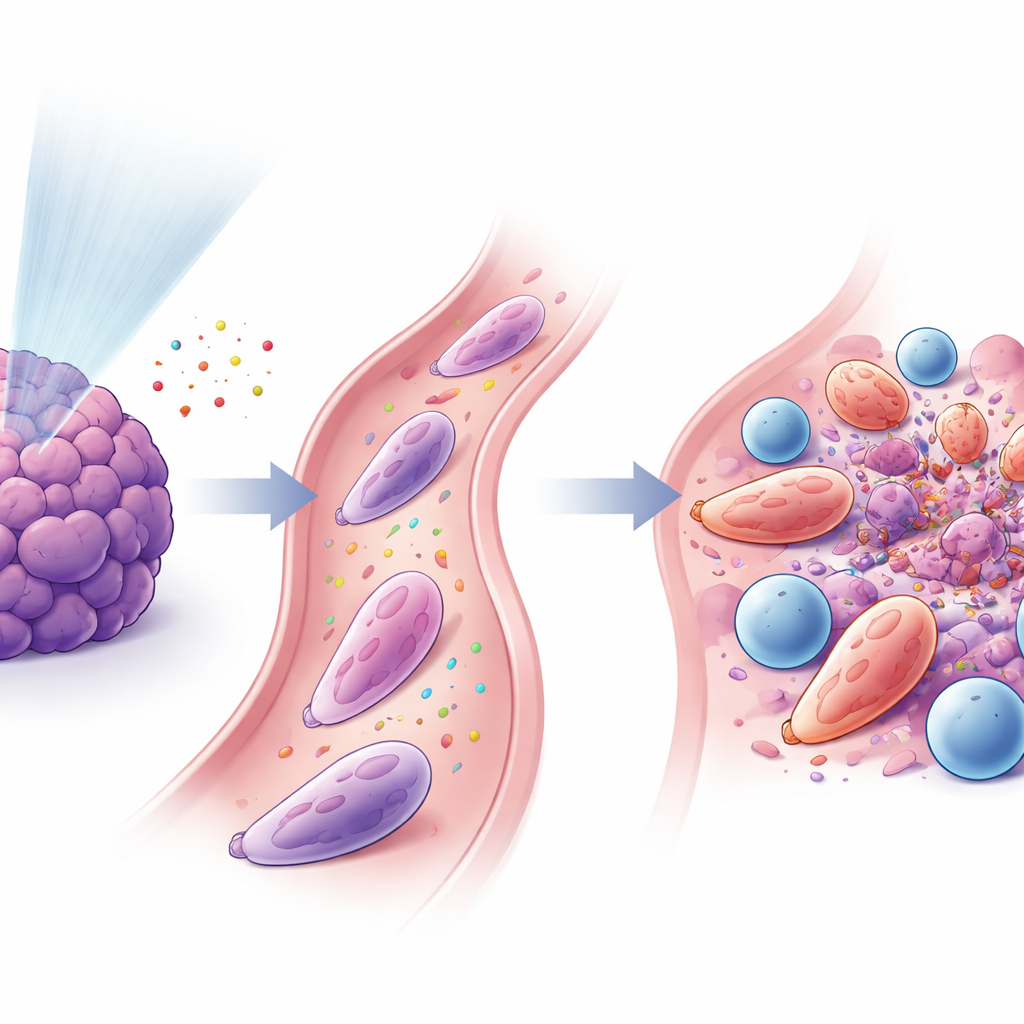
Нейтрофилы и Т‑клетки действуют сообща
Исследование показало, что перепрограммированные нейтрофилы и цитотоксические CD8+ Т‑клетки тесно связаны. Сигналы, высвобождаемые после низкодозного облучения, привлекали нейтрофилы через путь CXCL–CXCR2, а другие факторы, включая GM‑CSF и интерферон‑γ, способствовали их переходу в противоопухолевое состояние. После активации нейтрофилы экспрессировали адгезивные поверхностные белки (такие как ICAM‑1), которые соединяли их с Т‑клетками (несущими соответствующий партнёр LFA‑1), формируя плотные контакты, похожие на «иммунные синапсы». В культуре эти нейтрофилы усиливали активацию и пролиферацию Т‑клеток и повышали их способность убивать раковые клетки. При пересадке таких специализированных нейтрофилов мышам с опухолями, особенно в сочетании с блокадой PD‑1, опухоли уменьшались, а выживаемость улучшалась.
Данные из опухолей и крови пациентов
Команда также исследовала образцы опухолей пациентов до и после TRIDENT с помощью современных пространственных методов картирования экспрессии генов. После лечения в опухолях появились очаги, где кластерами располагались эти TNF‑α–богатые нейтрофилы и активные CD8+ Т‑клетки, сопровождались сильными сигналами, связанными с обработкой антигенов и иммунной активацией. В нескольких наборах данных пациентов с раком легкого, леченных иммунотерапией, более высокий уровень генной подписи, связанной с этими нейтрофилами, коррелировал с более длительным временем до прогрессирования. В небольшой наблюдательной группе пациентов, получавших сочетание облучения и блокады PD‑1, у ответивших на лечение наблюдались заметные увеличения активированных нейтрофилов в крови, тогда как у неответивших таких изменений не было.
Что это означает для людей с раком легких
Для человека с распространённым раком легкого эти результаты указывают, что способ доставки облучения может быть так же важен, как и его доза. Сочетая небольшие, нацеленные на модуляцию иммунитета дозы к крупным опухолям с обычным высокодозным облучением и блокадой PD‑1, TRIDENT, по-видимому, переводит нейтрофилы из возможных пособников опухоли в сильных партнёров Т‑клеток. Это взаимодействие нейтрофилов и Т‑клеток связано с долговременным контролем опухоли и улучшением выживаемости, поэтому TRIDENT представляет собой перспективную стратегию, сейчас проверяемую в больших рандомизированных испытаниях. Работа также выдвигает активированные нейтрофилы как потенциальные мишени для будущих терапий и как простые маркеры в крови для прогнозирования, кто с наибольшей вероятностью извлечёт пользу из радиационно-иммунотерапевтического подхода.
Цитирование: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
Ключевые слова: раковые заболевания легких, лучевая терапия, иммунотерапия, нейтрофилы, блокада PD-1