Clear Sky Science · pl
Radioterapia w niskich dawkach synergizuje z blokadą PD-1, zapewniając trwałe przeżycie w zaawansowanym niedrobnokomórkowym raku płuca poprzez programowanie neutrofili przeciwko nowotworowi
Wykorzystanie pierwszych strażników organizmu przeciw rakowi płuca
Większość osób traktuje radioterapię i immunoterapię jako oddzielne narzędzia walki z rakiem. To badanie pokazuje, że starannie dobrane dawki promieniowania w połączeniu z popularnym lekiem immunoterapeutycznym mogą przeprogramować zaskakującego sojusznika — neutrofile, rodzaj białych krwinek — by pomóc pacjentom z zaawansowanym rakiem płuca żyć znacznie dłużej.
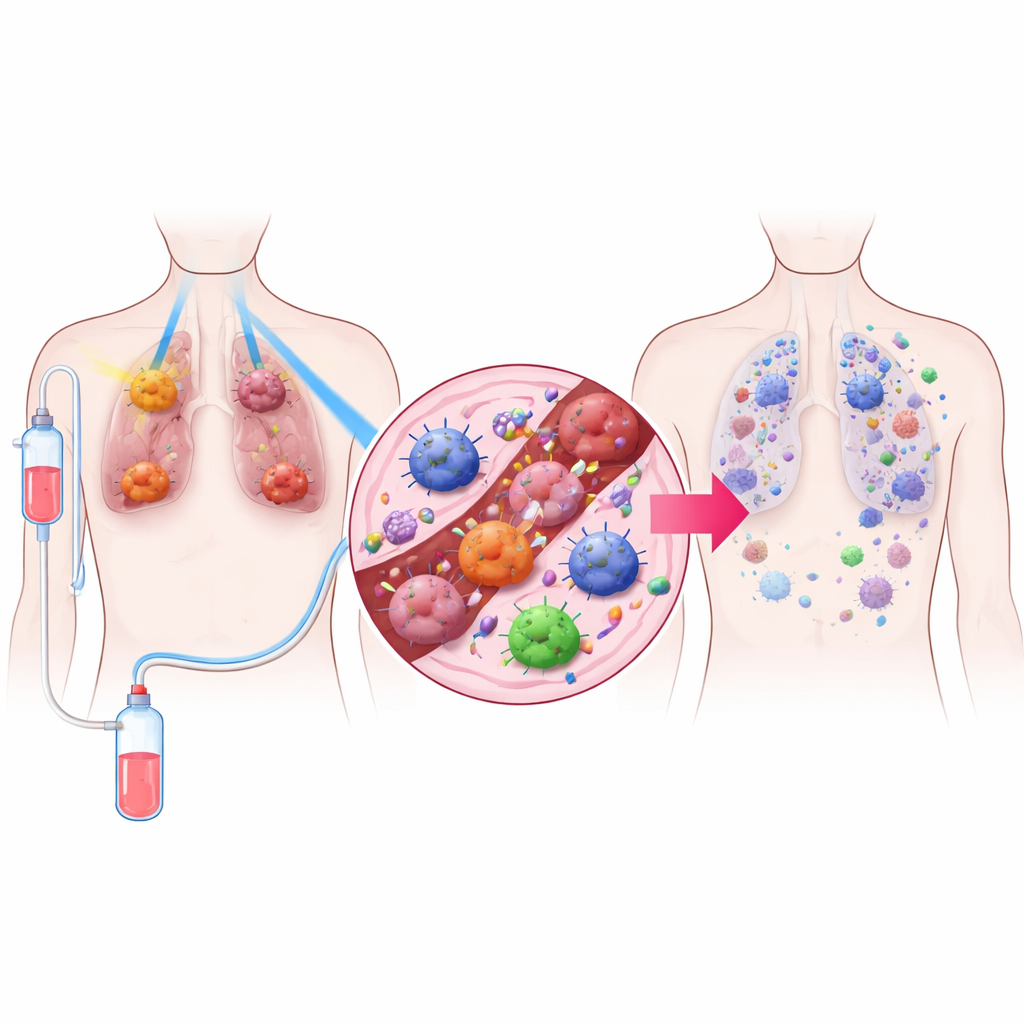
Strategia leczenia składająca się z trzech elementów
Naukowcy opracowali terapię nazwaną TRIDENT, łączącą trzy składniki. Po pierwsze, duże guzy płuca otrzymują bardzo niskie dawki promieniowania, zbyt słabe, by od razu zabić wiele komórek, ale wystarczające, by zmienić środowisko guza. Po drugie, mniejsze guzy są napromieniane wysokimi dawkami stosowanymi do lokalnego niszczenia nowotworu. Po trzecie, pacjenci otrzymują lek blokujący PD‑1 — rodzaj immunoterapii odblokowującej limfocyty T. Mieszając te trzy elementy, zespół dążył zarówno do kontroli widocznych guzów, jak i do pobudzenia układu odpornościowego w całym organizmie.
Obiecujące przeżycia w zaawansowanym raku płuca
W badaniu klinicznym fazy I 29 osób z zaawansowanym niedrobnokomórkowym rakiem płuca, które nie otrzymały wcześniej leczenia i których guzy wykazywały ekspresję białka PD‑L1, otrzymało TRIDENT bez chemioterapii. Przy ponad pięciu latach obserwacji mediana całkowitego przeżycia wyniosła 51,3 miesiąca — znacznie dłużej niż około 15–23 miesięcy zwykle obserwowanych przy samej immunoterapii lub immunoterapii z chemioterapią. Osobna, realistyczna kohorta 97 pacjentów leczonych podejściem podobnym do TRIDENT wykazała podobnie zachęcające przeżycia. Kilku pacjentów pozostawało bez progresji choroby ponad pięć lat, co sugeruje, że terapia może wywołać długotrwałą pamięć odpornościową przeciwko nowotworowi.
Jak niskie dawki promieniowania wspierają układ odpornościowy
Aby zrozumieć, dlaczego to połączenie działa, zespół sięgnął po modele mysie z guzami po obu stronach ciała, naśladując przerzuty do wielu miejsc. Tylko przy jednoczesnym zastosowaniu niskiej dawki promieniowania, wysokiej dawki i blokady PD‑1 guzy zmniejszały się nie tylko tam, gdzie skierowano wysokie dawki, lecz także w odległych miejscach — co wskazuje na odpowiedź immunologiczną obejmującą cały organizm. Szczegółowe analizy pojedynczych komórek wykazały, że to leczenie znacznie zwiększało liczbę neutrofili napływających do tych odległych guzów. W odróżnieniu od zwykle wspierających guz neutrofili, komórki te wytwarzały prozapalny sygnał TNF‑α i wykazywały cechy profesjonalnych stymulatorów odpornościowych, w tym cząsteczki umożliwiające prezentowanie fragmentów guza limfocytom T oraz dostarczanie sygnałów "do ataku".
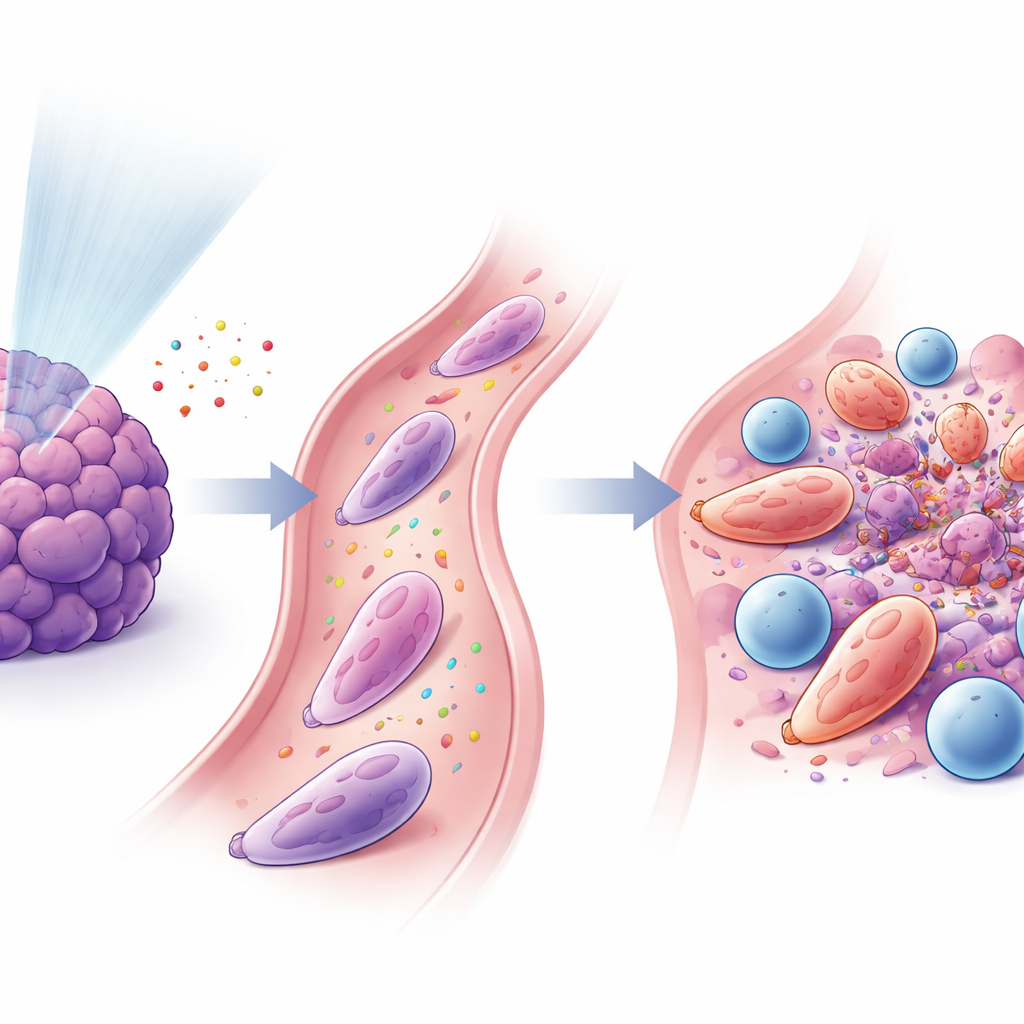
Neutrofile i limfocyty T łączą siły
Badanie wykazało silne powiązanie między tymi przeprogramowanymi neutrofilami a zabójczymi limfocytami CD8+. Sygnały uwalniane po niskodawkowym napromienianiu przyciągały neutrofile poprzez szlak CXCL–CXCR2, a inne czynniki, w tym GM‑CSF i interferon‑γ, pomagały przekształcić je w stan przeciw nowotworowy. Po aktywacji neutrofile wyrażały lepkie białka powierzchniowe (takie jak ICAM‑1), które wiązały je z limfocytami T (niosącymi dopasowany receptor LFA‑1), tworząc bliskie interfejsy przypominające synapsy immunologiczne. W hodowlach komórkowych neutrofile te wzmacniały aktywację i proliferację limfocytów T oraz usprawniały ich zdolność do zabijania komórek nowotworowych. Gdy naukowcy przeszczepili te wyspecjalizowane neutrofile do myszy z guzami, szczególnie w połączeniu z blokadą PD‑1, guzy zmniejszały się, a przeżycie poprawiało.
Dane z guzów i krwi pacjentów
Zespół przeanalizował także próbki guzów od pacjentów przed i po TRIDENT przy użyciu zaawansowanych narzędzi mapowania przestrzennego ekspresji genów. Po leczeniu w guzach pojawiły się skupiska neutrofili bogatych w TNF‑α i aktywnych limfocytów CD8+, wraz z silnymi sygnałami dotyczącymi przetwarzania antygenów i aktywacji odporności. W wielu zbiorach danych dotyczących raka płuca leczonego immunoterapią wyższy poziom sygnatury genowej powiązanej z tymi neutrofilami korelował z dłuższym czasem do progresji choroby. W małej obserwacyjnej grupie pacjentów otrzymujących połączone napromienianie i blokadę PD‑1 respondenci wykazywali wyraźny wzrost aktywowanych neutrofili we krwi, podczas gdy niereagujący nie.
Co to oznacza dla osób z rakiem płuca
Dla pacjenta z zaawansowanym rakiem płuca wyniki te sugerują, że sposób podania promieniowania może być równie istotny jak jego dawka. Łącząc niewielkie, modulujące odporność dawki do dużych guzów z klasycznym wysokodawkowym napromienianiem i blokadą PD‑1, TRIDENT wydaje się przekształcać neutrofile z potencjalnych współwinnych guza w silnych partnerów limfocytów T. Ta współpraca neutrofili i limfocytów T wiąże się z długotrwałą kontrolą guza i lepszym przeżyciem, co czyni TRIDENT obiecującą strategią obecnie testowaną w większych, randomizowanych badaniach. Praca wskazuje także na aktywowane neutrofile jako potencjalne cele terapeutyczne i proste markery we krwi, które mogą pomóc przewidzieć, kto najprawdopodobniej skorzysta z radio‑immunoterapii.
Cytowanie: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
Słowa kluczowe: rak płuca, radioterapia, immunoterapia, neutrofile, blokada PD-1