Clear Sky Science · ar
العلاج الإشعاعي بجرعات منخفضة يتآزر مع حجب PD-1 لتحقيق بقاء طويل الأمد في سرطان الرئة غير صغير الخلايا المتقدم من خلال برمجة العدلات المضادة للأورام
توجيه أول المستجيبين في الجسم ضد سرطان الرئة
يفكر معظم الناس في الإشعاع والعلاج المناعي كأداتين منفصلتين ضد السرطان. تُظهر هذه الدراسة كيف أن ضبط جرعات الإشعاع بعناية وإقرانها بدواء مناعِي شائع يمكن أن يعيد برمجة حليف مفاجئ — العدلات، نوع من خلايا الدم البيضاء — لمساعدة مرضى سرطان الرئة المتقدم على العيش لفترة أطول بكثير.
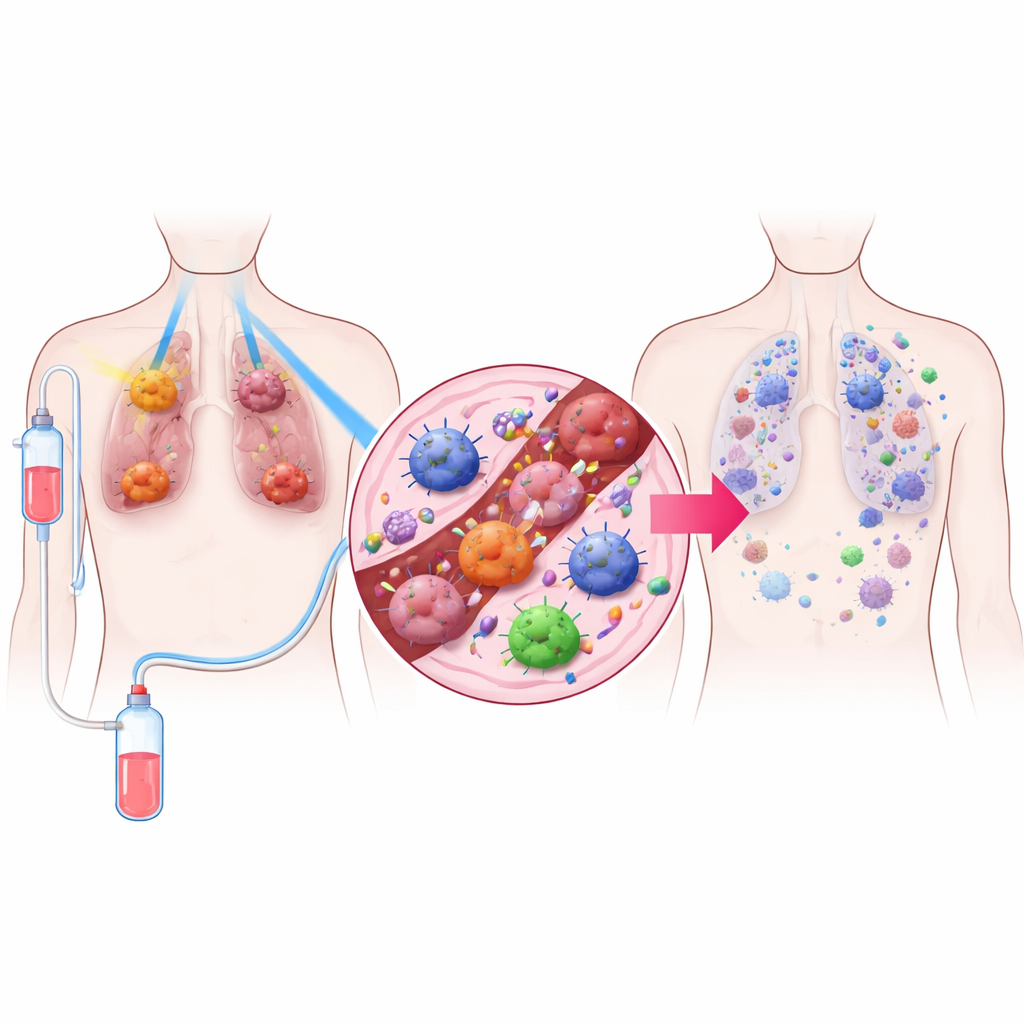
استراتيجية علاجية ثلاثية المكونات
صمم الباحثون علاجًا أطلقوا عليه اسم TRIDENT يجمع بين ثلاث عناصر. أولاً، تتعرض الأورام الرئوية الكبيرة لجرعات منخفضة جدًا من الإشعاع تكون ضعيفة جدًا بحيث لا تقتل الكثير من الخلايا مباشرة لكنها يمكن أن تغير سلوك بيئة الورم. ثانيًا، تُستهدف الأورام الأصغر بالإشعاع عالي الجرعة الأكثر شيوعًا المستخدم لتدمير السرطان موضعيًا. ثالثًا، يتلقى المرضى دواءً يثبط PD‑1، وهو نوع من العلاج المناعي يرفع القيود عن الخلايا التائية في الجهاز المناعي. من خلال مزج هذه الأجزاء الثلاثة، سعى الفريق إلى السيطرة على الأورام المرئية وإيقاظ دفاعات الجهاز المناعي في أنحاء الجسم كلها.
بقاء واعد في سرطان الرئة المتقدم
في تجربة سريرية من المرحلة الأولى، خضع 29 شخصًا مصابًا بسرطان الرئة غير صغير الخلايا المتقدم والذين لم يتلقوا علاجًا سابقًا وكانت أورامهم تعبر عن بروتين PD‑L1 إلى علاج TRIDENT دون علاج كيميائي. مع متابعة تجاوزت خمس سنوات، بلغ الوسيط الزمني للبقاء العام 51.3 شهرًا — أطول بكثير من نحو 15–23 شهرًا الذي يُرى عادةً مع العلاج المناعي وحده أو العلاج المناعي مع العلاج الكيميائي. أظهرت مجموعة حقيقية منفصلة مكونة من 97 مريضًا عولجت بنهج مشابه لِـTRIDENT بقاء مشجعًا مماثلًا. ظل عدد من المرضى دون تقدم لأكثر من خمس سنوات، مما يشير إلى أن العلاج قد يثير ذاكرة مناعية طويلة الأمد ضد السرطان.
كيف يساعد الإشعاع منخفض الجرعة الجهاز المناعي
لفهم سبب فاعلية هذا المزيج، لجأ الفريق إلى نماذج فأرية حاملة لأورام على جانبي الجسم، مقلدين الانتشار إلى مواقع متعددة. لم تتقلص الأورام بعيدًا عن مواضع الإشعاع عالي الجرعة إلا عندما استُخدم معًا الإشعاع منخفض الجرعة، والإشعاع عالي الجرعة، وحجب PD‑1، مما يشير إلى استجابة مناعية على مستوى الجسم. كشفت تحليلات الخلايا المفردة التفصيلية أن هذا النظام زاد بشكل كبير عدد العدلات التي تدخل هذه الأورام البعيدة. على عكس العدلات المعتادة الداعمة للورم، أنتجت هذه الخلايا الإشارة الالتهابية TNF‑α وأظهرت سمات منشطات مناعية محترفة، بما في ذلك جزيئات تتيح لها عرض أجزاء من الورم للخلايا التائية وتقديم إشارات "انطلق" للهجوم.
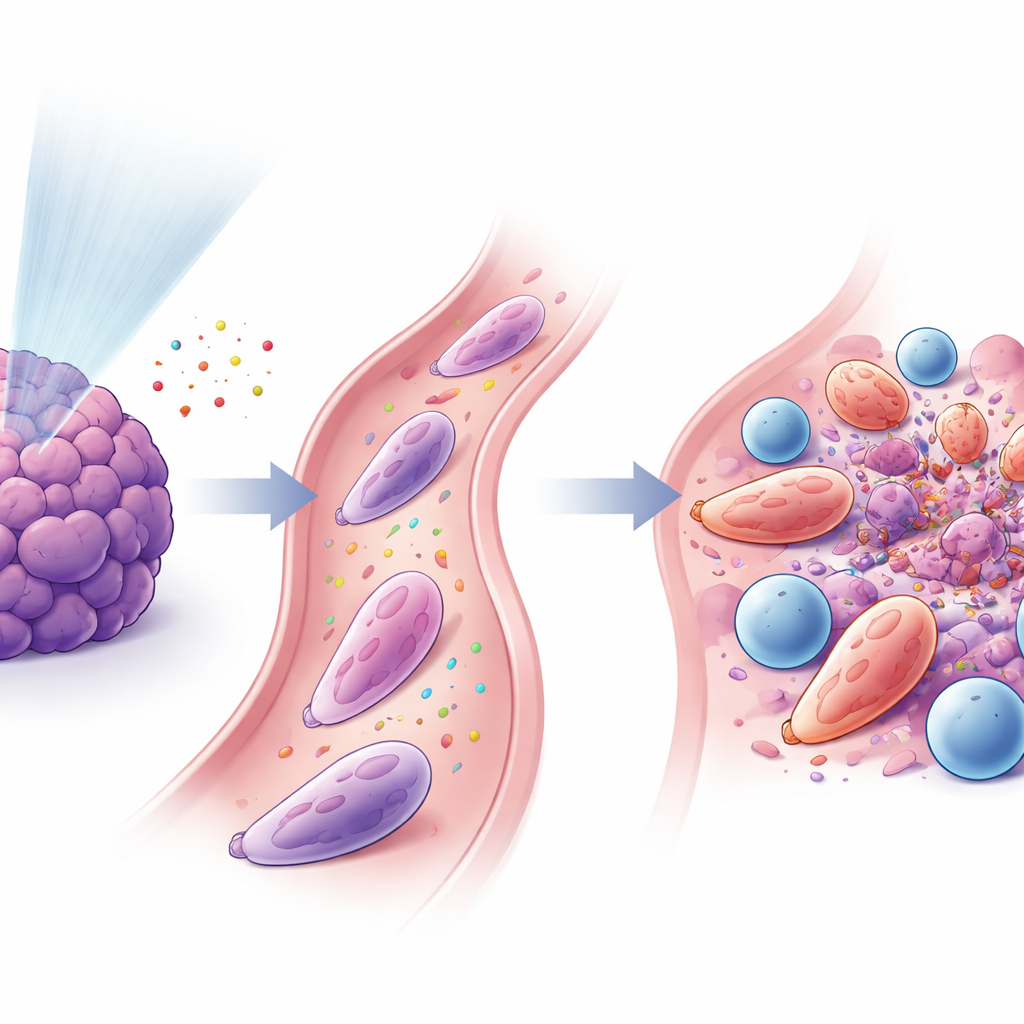
تكاتف العدلات والخلايا التائية
وجدت الدراسة أن هذه العدلات المعاد برمجتها والخلايا التائية القاتلة CD8+ كانتا مرتبطتين ارتباطًا وثيقًا. جذبت الإشارات المُفرَزة بعد الإشعاع منخفض الجرعة العدلات عبر مسار معروف باسم CXCL–CXCR2، وساهمت عوامل أخرى، بما في ذلك GM‑CSF والإنترفيرون‑γ، في تحويلها إلى حالة مضادة للورم. بعد تنشيطها، عبّرت العدلات عن بروتينات سطحية لزجة (مثل ICAM‑1) ربطتها بالخلايا التائية (التي تحمل الشريك المطابق LFA‑1)، فشكلت واجهات تلامس وثيقة تشبه المشابك المناعية. في الأطباق المخبرية، عززت هذه العدلات تنشيط وتكاثر الخلايا التائية وساعدت الخلايا التائية على قتل الخلايا السرطانية بكفاءة أكبر. عند نقل هذه العدلات المتخصصة إلى فئران حاملة للأورام، خصوصًا مع حجب PD‑1، تقلصت الأورام وتحسن البقاء.
دليل من أورام ودم المرضى
فحص الفريق أيضًا عينات أورام من المرضى قبل وبعد TRIDENT باستخدام أدوات رسم خرائط جينية مكانية متقدمة. بعد العلاج، أظهرت الأورام جيوبًا حيث تجمعت هذه العدلات الغنية بـTNF‑α والخلايا التائية CD8+ النشطة معًا، إلى جانب إشارات قوية متعلقة بمعالجة المستضد والتنشيط المناعي. في مجموعات بيانات مرضى متعددة لسرطان الرئة المعالج بالعلاج المناعي، ارتبطت مستويات أعلى لتوقيع جيني مرتبط بهذه العدلات بزمن أطول قبل تدهور السرطان. في مجموعة مراقبة صغيرة من المرضى الذين تلقوا إشعاعًا مضافًا إلى حجب PD‑1، أظهر المستجيبون زيادات واضحة في العدلات المنشطة في دمهم، بينما لم يظهر ذلك لدى غير المستجيبين.
ماذا يعني هذا للأشخاص المصابين بسرطان الرئة
بالنسبة لشخص مصاب بسرطان الرئة المتقدم، تشير هذه النتائج إلى أن طريقة إعطاء الإشعاع قد تكون مهمة بقدر كمية الإشعاع نفسها. من خلال الجمع بين جرعات صغيرة تعدل المناعة للأورام الكبيرة، والإشعاع القياسي عالي الجرعة، وحجب PD‑1، يبدو أن TRIDENT يحول العدلات من شركاء محتملين للورم إلى شركاء أقوياء مع الخلايا التائية. يرتبط هذا التعاون بين العدلات والخلايا التائية بسيطرة طويلة الأمد على الورم وبقاء محسن، مما يجعل TRIDENT استراتيجية واعدة تُختبر الآن في تجارب عشوائية أكبر. كما يشير العمل إلى العدلات المنشطة نفسها كأهداف علاجية محتملة في المستقبل وكعلامات بسيطة قائمة على الدم للمساعدة في التنبؤ بمن هم الأكثر احتمالًا للاستفادة من العلاج الإشعاعي المناعي.
الاستشهاد: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
الكلمات المفتاحية: سرطان الرئة, العلاج بالإشعاع, العلاج المناعي, العدلات, حجب PD-1