Clear Sky Science · nl
Laaggedoseerde radiotherapie werkt samen met PD-1-blokkade om duurzame overleving bij gevorderde NSCLC te bereiken via antitumorprogrammering van neutrofielen
Het inzetten van de eerste responders van het lichaam tegen longkanker
De meeste mensen zien bestraling en immunotherapie als afzonderlijke wapens tegen kanker. Deze studie toont aan hoe het zorgvuldig afstemmen van bestralingsdoses en het combineren met een veelgebruikt immunotherapie-middel een verrassende bondgenoot — neutrofielen, een type witte bloedcellen — kan herprogrammeren om patiënten met gevorderde longkanker veel langer te laten leven.
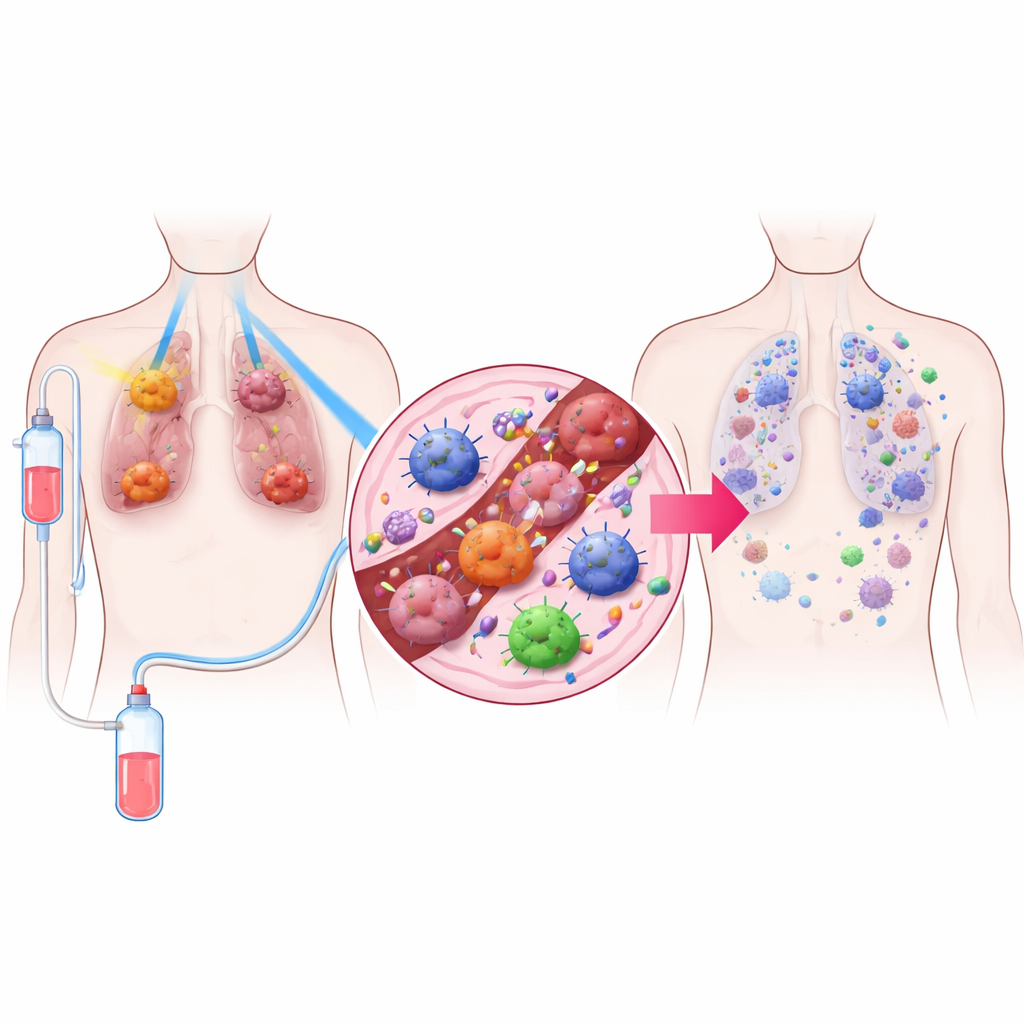
Een driedelige behandelstrategie
De onderzoekers ontwierpen een behandeling die zij TRIDENT noemen, die drie elementen combineert. Ten eerste krijgen grote longtumoren zeer lage stralingsdoses die te zwak zijn om veel cellen direct te doden maar wel het gedrag van de tumorumgeving kunnen veranderen. Ten tweede worden kleinere tumoren bestraald met de meer bekende hoge dosis die bedoeld is om lokaal kanker te vernietigen. Ten derde ontvangen patiënten een PD‑1–blokkerend middel, een vorm van immunotherapie die de rem van de T‑cellen van het immuunsysteem wegneemt. Door deze drie onderdelen te combineren, wilde het team zowel zichtbare tumoren onder controle krijgen als het immuunsysteem door het hele lichaam activeren.
Veelbelovende overleving bij gevorderde longkanker
In een fase I-klinische studie kregen 29 mensen met gevorderde niet-kleincellige longkanker die geen eerdere behandeling hadden ontvangen en waarvan de tumoren PD‑L1 produceerden, TRIDENT zonder chemotherapie. Met meer dan vijf jaar follow-up was de mediane totale overleving 51,3 maanden — aanzienlijk langer dan de ongeveer 15–23 maanden die gewoonlijk worden gezien bij standaardimmunotherapie alleen of immunotherapie plus chemotherapie. Een aparte real-world groep van 97 patiënten behandeld met een TRIDENT-achtige benadering liet vergelijkbare veelbelovende overleving zien. Verschillende patiënten bleven langer dan vijf jaar zonder progressie, wat suggereert dat de behandeling langdurig immuungeheugen tegen de kanker kan opwekken.
Hoe laaggedoseerde bestraling het immuunsysteem helpt
Om te begrijpen waarom deze combinatie werkt, gebruikte het team muismodellen met tumoren aan beide zijden van het lichaam, om uitzaaiing naar meerdere locaties na te bootsen. Alleen wanneer laaggedoseerde bestraling, hooggedoseerde bestraling en PD‑1-blokkade samen werden toegepast, krompen tumoren niet alleen op de plekken waar hoge doses waren gericht, maar ook op afstand gelegen locaties, wat wijst op een lichaamsbrede immuunrespons. Gedetailleerde single-cell-analyses toonden aan dat dit regime het aantal neutrofielen dat deze verre tumoren binnendrong sterk verhoogde. In tegenstelling tot de gebruikelijke tumorsupportende neutrofielen produceerden deze cellen het ontstekingssignaal TNF‑α en toonden ze kenmerken van professionele immuunstimulatoren, inclusief moleculen die hen in staat stellen stukjes tumor aan T‑cellen te presenteren en ‘ga’-signalen voor aanval te geven.
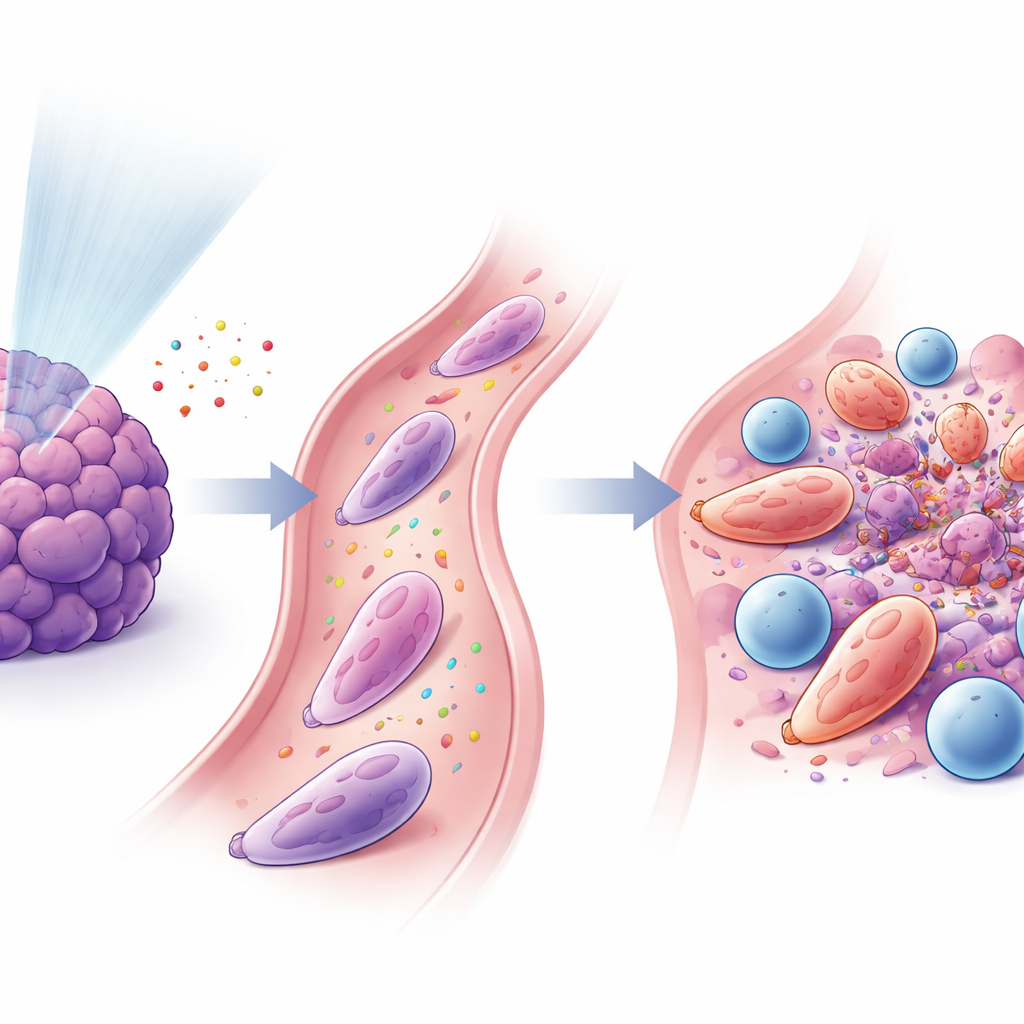
Neutrofielen en T‑cellen slaan de handen ineen
De studie vond dat deze hergeprogrammeerde neutrofielen en cytotoxische CD8+ T‑cellen nauw met elkaar verbonden waren. Signalen die vrijkwamen na laaggedoseerde bestraling trokken neutrofielen aan via een pad dat bekendstaat als CXCL–CXCR2, en andere factoren, waaronder GM‑CSF en interferon‑γ, hielpen hen in een antitumorstatus om te zetten. Eenmaal geactiveerd, uitten neutrofielen kleverige oppervlakte-eiwitten (zoals ICAM‑1) die hen vastkoppelden aan T‑cellen (die het corresponderende LFA‑1 dragen), waardoor nauwe contactplaatsen ontstonden die op immuunsynapsen leken. In kweekexperimenten stimuleerden deze neutrofielen T‑celactivatie en proliferatie en hielpen ze T‑cellen kankercellen efficiënter te doden. Wanneer wetenschappers deze gespecialiseerde neutrofielen in tumordragende muizen transfereerden, vooral in combinatie met PD‑1-blokkade, krompen tumoren en verbeterde de overleving.
Bewijs uit patiëntentumoren en bloed
Het team onderzocht ook tumormonsters van patiënten voor en na TRIDENT met behulp van geavanceerde ruimtelijke gen-kaartvormingstechnieken. Na behandeling toonden tumoren gebieden waar deze TNF‑α-rijke neutrofielen en actieve CD8+ T‑cellen samenklonterden, samen met sterke signalen gerelateerd aan antigeenverwerking en immuunactivatie. In meerdere patiëntendatasets van longkanker behandeld met immunotherapie waren hogere niveaus van een genhandtekening gekoppeld aan deze neutrofielen geassocieerd met een langere tijd tot voortgang van de ziekte. In een kleine observationele groep patiënten die gecombineerde bestraling en PD‑1-blokkade kregen, vertoonden responders duidelijke toename van geactiveerde neutrofielen in hun bloed, terwijl non-responders dat niet deden.
Wat dit betekent voor mensen met longkanker
Voor iemand met gevorderde longkanker suggereren deze bevindingen dat de manier waarop bestraling wordt gegeven mogelijk net zo belangrijk is als de dosis zelf. Door kleine, immuun-afstemmende doses naar grote tumoren te combineren met standaard hoge-dosis bestraling en PD‑1-blokkade, lijkt TRIDENT neutrofielen te veranderen van potentiële medeplichtigen van de tumor in krachtige partners van T‑cellen. Deze samenwerking tussen neutrofielen en T‑cellen hangt samen met langdurige tumorcontrole en betere overleving, waardoor TRIDENT een veelbelovende strategie is die nu in grotere gerandomiseerde onderzoeken wordt getest. Het werk wijst ook op geactiveerde neutrofielen zelf als mogelijke toekomstige behandeldoelen en als eenvoudige bloedgebaseerde markers om te helpen voorspellen wie het meest waarschijnlijk baat heeft bij radio-immunotherapie.
Bronvermelding: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
Trefwoorden: longkanker, radiotherapie, immunotherapie, neutrofielen, PD-1-blokkade