Clear Sky Science · it
La radioterapia a basse dosi sinergizza con il blocco di PD-1 per ottenere una sopravvivenza duratura nel NSCLC avanzato tramite riprogrammazione antitumorale dei neutrofili
Rivoltare i primi soccorritori del corpo contro il cancro polmonare
La maggior parte delle persone considera radiazione e immunoterapia armi distinte contro il cancro. Questo studio mostra come modulare con cura le dosi di radiazione e abbinarle a un farmaco immunoterapico comune possa riprogrammare un alleato inaspettato — i neutrofili, un tipo di globuli bianchi — per aiutare i pazienti con cancro polmonare avanzato a vivere molto più a lungo.
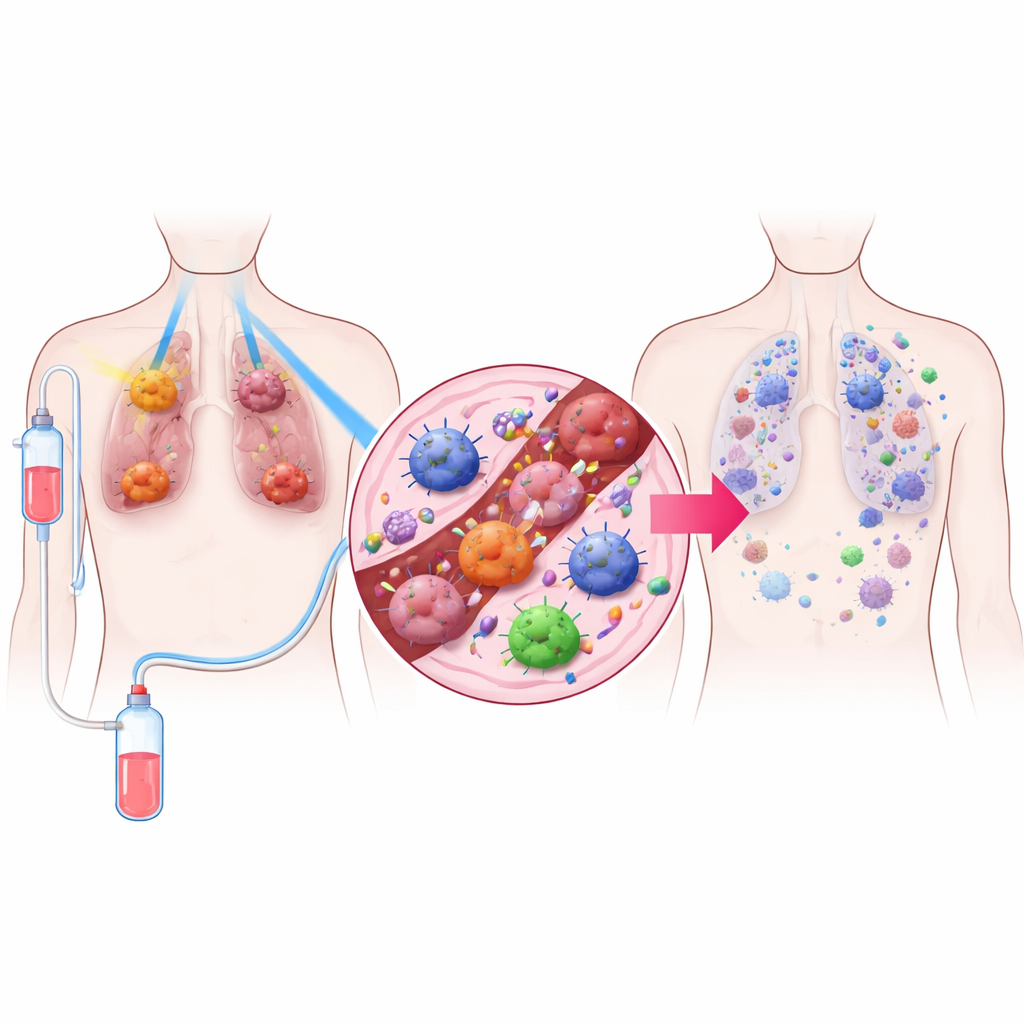
Una strategia terapeutica in tre parti
I ricercatori hanno ideato un trattamento chiamato TRIDENT, che combina tre elementi. Primo, ai grossi tumori polmonari vengono somministrate dosi molto basse di radiazione, troppo deboli per uccidere molte cellule direttamente ma in grado di modificare il comportamento del microambiente tumorale. Secondo, i tumori più piccoli vengono trattati con la radiazione ad alta dose più familiare, usata per distruggere il tumore localmente. Terzo, i pazienti ricevono un farmaco inibitore di PD‑1, una forma di immunoterapia che toglie i freni alle cellule T del sistema immunitario. Mescolando queste tre componenti, il team mirava sia a controllare i tumori visibili sia a risvegliare le difese immunitarie in tutto l’organismo.
Sopravvivenza promettente nel cancro polmonare avanzato
In uno studio clinico di fase I, 29 persone con carcinoma polmonare non a piccole cellule avanzato, non precedentemente trattate e con tumori esprimenti la proteina PD‑L1, hanno ricevuto TRIDENT senza chemioterapia. Con più di cinque anni di follow-up, la mediana della sopravvivenza globale è stata di 51,3 mesi — molto più lunga rispetto ai circa 15–23 mesi generalmente osservati con sola immunoterapia standard o immunoterapia più chemioterapia. Un gruppo separato di pratica clinica reale composto da 97 pazienti trattati con un approccio simile a TRIDENT ha mostrato una sopravvivenza altrettanto incoraggiante. Diversi pazienti sono rimasti liberi da progressione per più di cinque anni, suggerendo che il trattamento può innescare una memoria immunitaria duratura contro il tumore.
Come la radioterapia a basse dosi aiuta il sistema immunitario
Per capire perché questa combinazione funziona, il team si è rivolto a modelli murini con tumori su entrambi i lati del corpo, a imitazione della diffusione a più sedi. Solo quando sono state usate insieme radiazione a bassa dose, radiazione ad alta dose e blocco di PD‑1 i tumori si sono ridotti non solo dove erano dirette le alte dosi, ma anche in sedi distanti, indicando una risposta immunitaria sistemica. Analisi dettagliate a singola cellula hanno rivelato che questo schema aumentava notevolmente il numero di neutrofili che penetravano in questi tumori distanti. Diversamente dai neutrofili che di solito supportano il tumore, queste cellule producevano il segnale infiammatorio TNF‑α e mostravano caratteristiche di potenti stimolatori immunitari, inclusi molecole che permettono loro di esporre frammenti tumorali alle cellule T e fornire segnali di “via libera” per l’attacco.
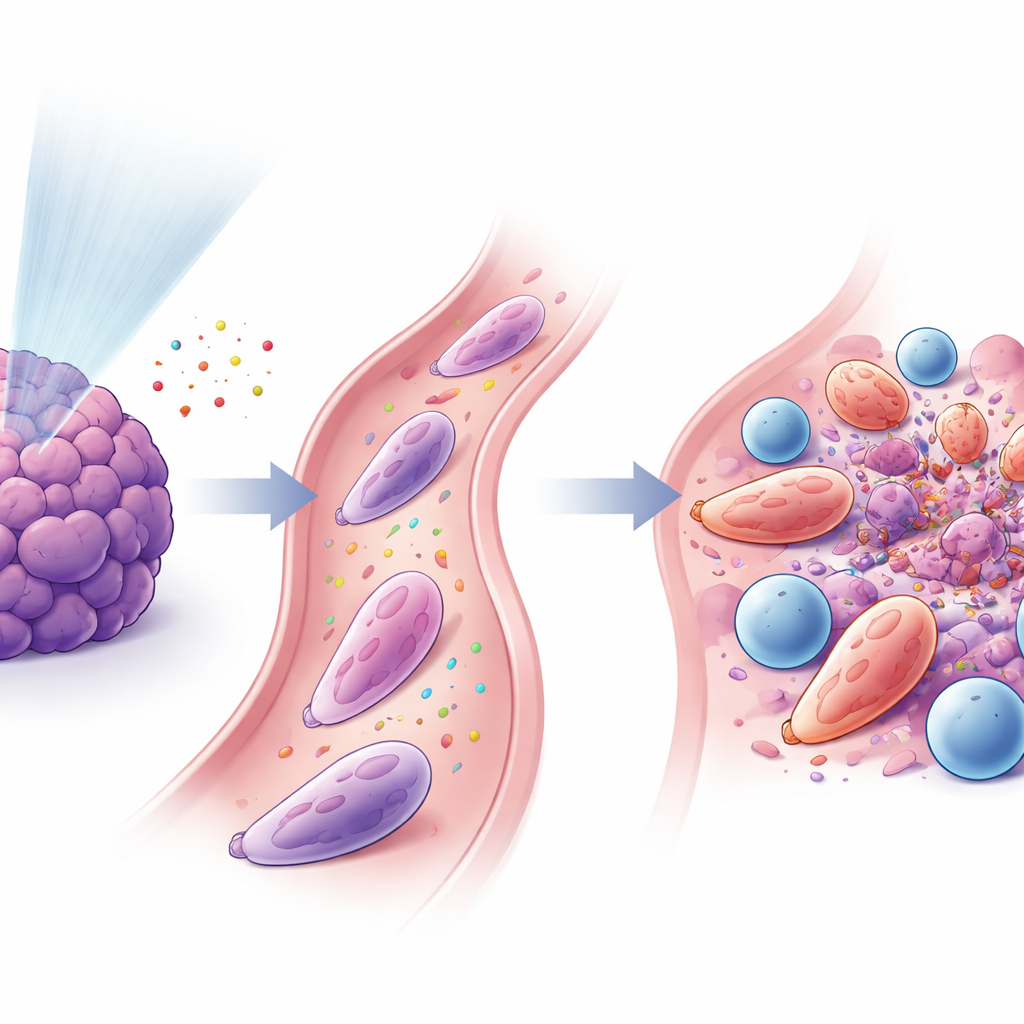
Neutrofili e cellule T uniscono le forze
Lo studio ha rilevato che questi neutrofili riprogrammati e le cellule T CD8+ citotossiche erano strettamente collegati. I segnali rilasciati dopo la radioterapia a basse dosi attiravano i neutrofili tramite una via nota come CXCL–CXCR2, e altri fattori, tra cui GM‑CSF e interferone‑γ, contribuivano a convertirli in uno stato antitumorale. Una volta attivati, i neutrofili esprimevano proteine adesive di superficie (come ICAM‑1) che li ancoravano alle cellule T (che portano il partner corrispondente LFA‑1), formando interfacce a contatto ravvicinato simili a sinapsi immunitarie. In colture cellulari, questi neutrofili potenziavano l’attivazione e la proliferazione delle cellule T e aiutavano le cellule T a uccidere le cellule tumorali in modo più efficiente. Quando gli scienziati trasferivano questi neutrofili specializzati in topi portatori di tumore, specialmente insieme al blocco di PD‑1, i tumori si riducevano e la sopravvivenza migliorava.
Prove da tumori e sangue dei pazienti
Il team ha anche esaminato campioni tumorali dei pazienti prima e dopo TRIDENT usando avanzati strumenti di mappatura genica spaziale. Dopo il trattamento, nei tumori sono emerse nicchie in cui questi neutrofili ricchi di TNF‑α e le cellule CD8+ attive si raggruppavano, insieme a forti segnali legati all’elaborazione degli antigeni e all’attivazione immunitaria. In più dataset di pazienti con cancro polmonare trattati con immunoterapia, livelli più alti di una firma genica associata a questi neutrofili erano correlati a un tempo più lungo prima della progressione della malattia. In un piccolo gruppo osservazionale di pazienti che ricevevano radiazione combinata con blocco di PD‑1, i responder mostrano chiari aumenti di neutrofili attivati nel sangue, mentre i non-responder no.
Cosa significa per le persone con cancro polmonare
Per una persona con cancro polmonare avanzato, questi risultati suggeriscono che il modo in cui la radiazione viene somministrata può essere importante quanto la quantità somministrata. Combinando piccole dosi di modulazione immunitaria ai grandi tumori con la radiazione standard ad alta dose e il blocco di PD‑1, TRIDENT sembra trasformare i neutrofili da potenziali complici del tumore in potenti partner delle cellule T. Questo lavoro collega il lavoro di squadra neutrofili–cellule T al controllo tumorale duraturo e a una migliore sopravvivenza, rendendo TRIDENT una strategia promettente attualmente in fase di sperimentazione in studi randomizzati più ampi. Lo studio indica inoltre i neutrofili attivati come possibili target terapeutici futuri e come marcatori semplici basati sul sangue per prevedere chi è più probabile che tragga beneficio dalla radio-immunoterapia.
Citazione: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
Parole chiave: cancro polmonare, radioterapia, immunoterapia, neutrofili, blocco di PD-1