Clear Sky Science · tr
Düşük doz radyoterapi, PD-1 blokajı ile sinerji yaparak ileri evre AKHH’de tümör karşıtı nötrofil programlaması yoluyla kalıcı sağkalım sağlıyor
Vücudun İlk Müdahale Edenlerini Akciğer Kanserine Karşı Çevirmek
Çoğu kişi radyasyon ve immünoterapinin kanserle mücadelede ayrı silahlar olduğunu düşünür. Bu çalışma, radyasyon dozlarını dikkatle ayarlamanın ve bunları yaygın bir immünoterapi ilacıyla eşleştirmenin, beklenmedik bir müttefiki—beyaz kan hücresi türü nötrofilleri—yeniden programlayarak ileri evre akciğer kanseri olan hastaların çok daha uzun yaşamasına nasıl yardımcı olabileceğini gösteriyor.
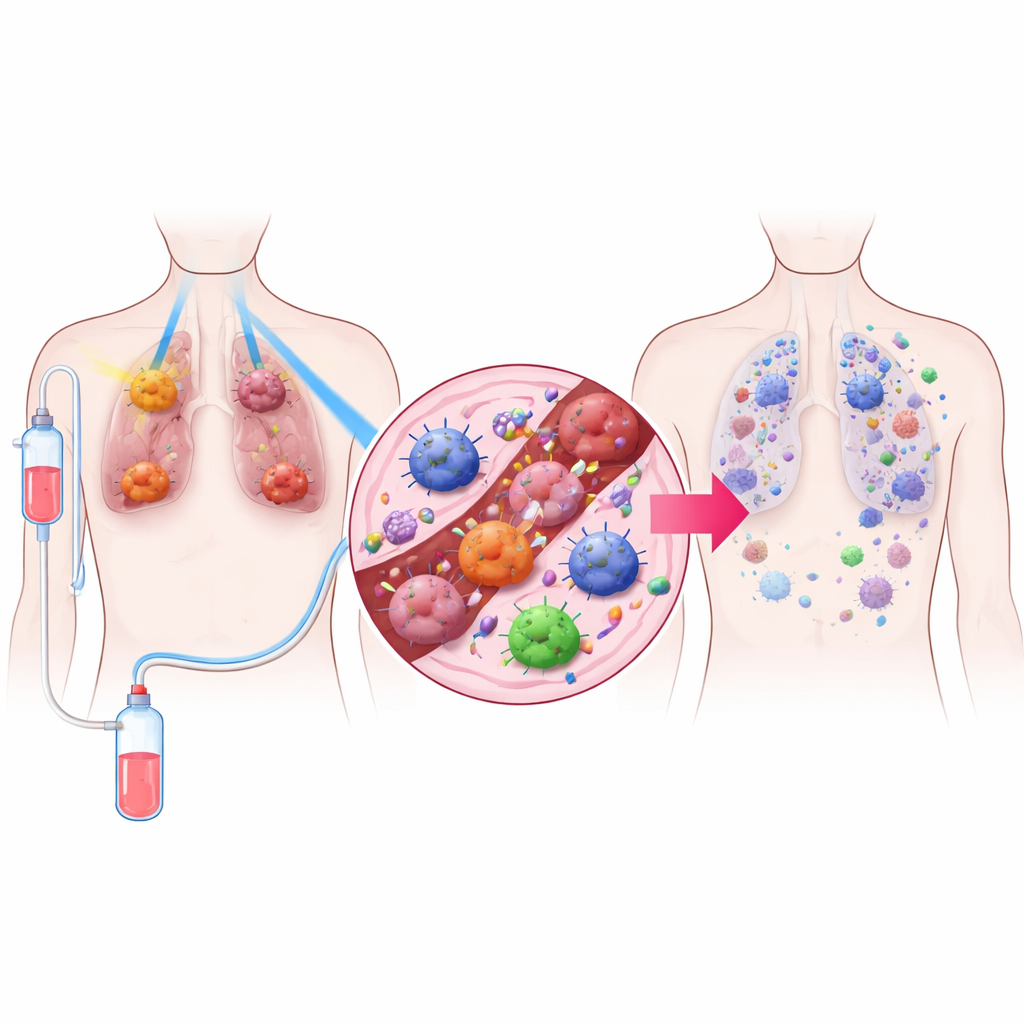
Üç Bölümlü Bir Tedavi Stratejisi
Araştırmacılar TRIDENT adını verdikleri bir tedavi tasarladılar; bu tedavi üç öğeyi birleştiriyor. Birincisi, büyük akciğer tümörlerine hücreleri doğrudan yok etmeye yeterli olmayan ancak tümör mikroyarışımını değiştirebilen çok düşük dozlarda radyasyon uygulanıyor. İkincisi, küçük tümörlere lokal olarak yok etmeyi amaçlayan alışık olunan yüksek doz radyasyon uygulanıyor. Üçüncüsü, hastalara immün sistemin T hücrelerindeki frenleri kaldıran bir tür immünoterapi olan PD‑1 bloke eden bir ilaç veriliyor. Bu üç öğeyi karıştırarak ekip, hem görülebilen tümörleri kontrol altına almayı hem de vücudun bağışıklık savunmasını genel olarak uyandırmayı hedefledi.
İleri Evre Akciğer Kanserinde Umut Veren Sağkalım
Bir faz I klinik çalışmada, önceden tedavi almamış ve tümörleri PD‑L1 proteini üreten ileri evre küçük hücre dışı akciğer kanseri olan 29 kişiye kemoterapi olmadan TRIDENT verildi. Beş yılı aşkın takiple, medyan genel sağkalım 51,3 ay olarak bulundu—standart immünoterapi tek başına veya immünoterapi artı kemoterapi ile genellikle görülen yaklaşık 15–23 ayın çok üzerinde. TRIDENT benzeri bir yaklaşımla tedavi edilen ayrı bir gerçek dünya kohortu olan 97 hasta da benzer şekilde cesaret verici sağkalım gösterdi. Birkaç hasta beş yıldan fazla ilerlemesiz kaldı; bu da tedavinin kanserle karşı uzun süreli immün hafıza başlatabileceğini düşündürüyor.
Düşük Doz Radyasyonun Bağışıklık Sistemine Yardımı
Bu kombinasyonun neden işe yaradığını anlamak için ekip, vücudun her iki tarafında tümörler bulunan fare modellerine yöneldi; bu, birden çok bölgeye yayılımı taklit ediyordu. Sadece düşük doz radyasyon, yüksek doz radyasyon ve PD‑1 blokajı birlikte kullanıldığında tümörler yalnızca yüksek dozun hedeflendiği yerlerde değil, uzak bölgelerde de küçüldü; bu, bütün vücutta bir bağışıklık yanıtına işaret ediyordu. Ayrıntılı tek hücre analizleri, bu rejimin uzak tümörlere giren nötrofil sayısını büyük ölçüde artırdığını ortaya koydu. Olağan, tümörü destekleyici nötrofillerin aksine, bu hücreler TNF‑α adlı inflamatuar sinyali üretiyor ve tümör parçacıklarını T hücrelerine sunmalarını ve saldırı için “gidebilir” sinyalleri vermelerini sağlayan moleküller de dahil olmak üzere profesyonel bağışıklık uyarıcılarının özelliklerini gösteriyordu.
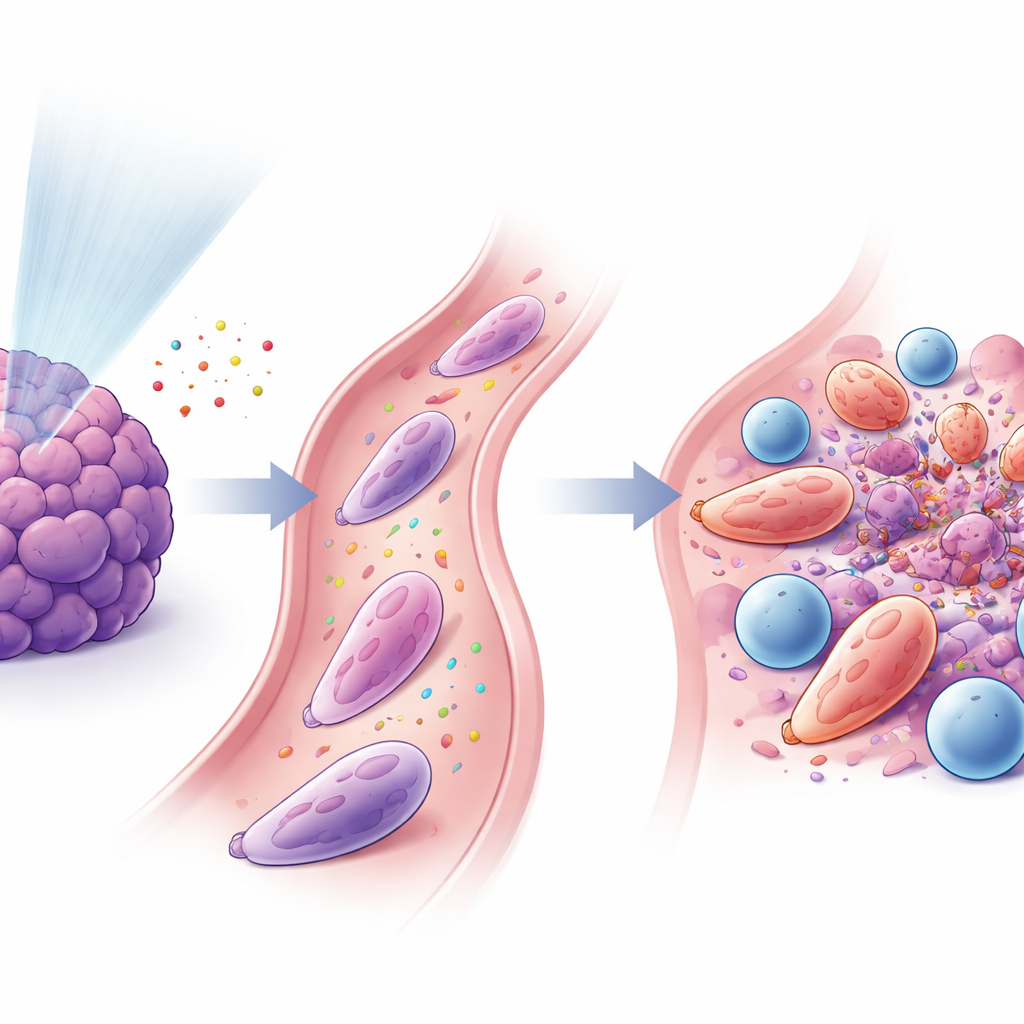
Nötrofiller ve T Hücreleri Güçlerini Birleştiriyor
Çalışma, bu yeniden programlanmış nötrofiller ile öldürücü CD8+ T hücreleri arasında sıkı bir bağ olduğunu buldu. Düşük doz radyasyon sonrası salınan sinyaller, CXCL–CXCR2 olarak bilinen bir yol aracılığıyla nötrofilleri çekti ve GM‑CSF ile interferon‑γ gibi diğer faktörler onları tümör karşıtı bir duruma dönüştürmeye yardımcı oldu. Bir kez aktive olduklarında, nötrofiller yapışkan yüzey proteinleri (ICAM‑1 gibi) ifade ederek onları T hücreleriyle (uyumlu partneri LFA‑1’i taşıyan) kilitliyor ve yakın temas “bağışıklık sinapsı benzeri” arayüzler oluşturuyordu. Laboratuvar kaplarında bu nötrofiller T hücresi aktivasyonunu ve proliferasyonunu artırdı ve T hücrelerinin kanser hücrelerini daha verimli öldürmesine yardımcı oldu. Bilim insanları bu özel nötrofilleri tümör taşıyan farelere, özellikle PD‑1 blokajı ile birlikte transfer ettiklerinde, tümörler küçüldü ve sağkalım iyileşti.
Hastaların Tümörleri ve Kanından Elde Edilen Kanıtlar
Ekip ayrıca TRIDENT öncesi ve sonrası hasta tümör örneklerini ileri düzey uzamsal gen haritalama araçlarıyla inceledi. Tedavi sonrası tümörlerde TNF‑α açısından zengin bu nötrofiller ile etkin CD8+ T hücrelerinin birlikte kümelendiği bölgeler ve antijen işleme ile bağışıklık aktivasyonu ile ilgili güçlü sinyaller görüldü. İmmünoterapi ile tedavi edilen akciğer kanserine ait birden çok hasta veri kümesinde, bu nötrofil ile ilişkili bir gen imzasının daha yüksek düzeyleri, kanserin kötüleşmesi öncesi daha uzun süre ile ilişkiliydi. Radyasyon ve PD‑1 blokajının kombinasyonunu alan küçük bir gözlemsel hasta grubunda, yanıt verenlerde kandaki aktive olmuş nötrofil düzeylerinde belirgin artışlar görüldü; yanıt vermeyenlerde ise böyle bir artış yoktu.
Akciğer Kanseri Olan İnsanlar İçin Ne Anlama Geliyor
İleri evre akciğer kanseri olan bir kişi için bu bulgular, radyasyonun nasıl verildiğinin miktarı kadar önemli olabileceğini öne sürüyor. Büyük tümörlere küçük, bağışıklığı ayarlayan dozlar ile standart yüksek doz radyasyon ve PD‑1 blokajını birleştirerek TRIDENT, nötrofilleri tümörün potansiyel işbirlikçilerinden T hücrelerinin güçlü ortaklarına dönüştürüyor gibi görünüyor. Bu nötrofil–T hücresi işbirliği kalıcı tümör kontrolü ve daha iyi sağkalımla ilişkilendiriliyor; TRIDENT şu anda daha büyük randomize çalışmalarda test edilen umut verici bir strateji. Çalışma ayrıca aktive olmuş nötrofilleri gelecekteki tedavi hedefleri ve radyo‑immünoterapiden en çok kimlerin yararlanacağını tahmin etmeye yardımcı olabilecek basit kan tabanlı belirteçler olarak işaret ediyor.
Atıf: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
Anahtar kelimeler: akciğer kanseri, radyoterapi, immünoterapi, nötrofiller, PD-1 blokajı