Clear Sky Science · sv
Lågdosstrålning samverkar med PD-1‑blockad för att uppnå varaktig överlevnad vid avancerad NSCLC genom antitumöral programmering av neutrofiler
Förvandla kroppens första försvarslinje mot lungcancer
De flesta tänker på strålning och immunterapi som separata vapen mot cancer. Denna studie visar hur man genom noggrann avvägning av stråldoser och kombination med en vanlig immunterapidrog kan programmera om en överraskande allierad — neutrofiler, en typ av vita blodkroppar — så att de hjälper patienter med avancerad lungcancer att leva betydligt längre.
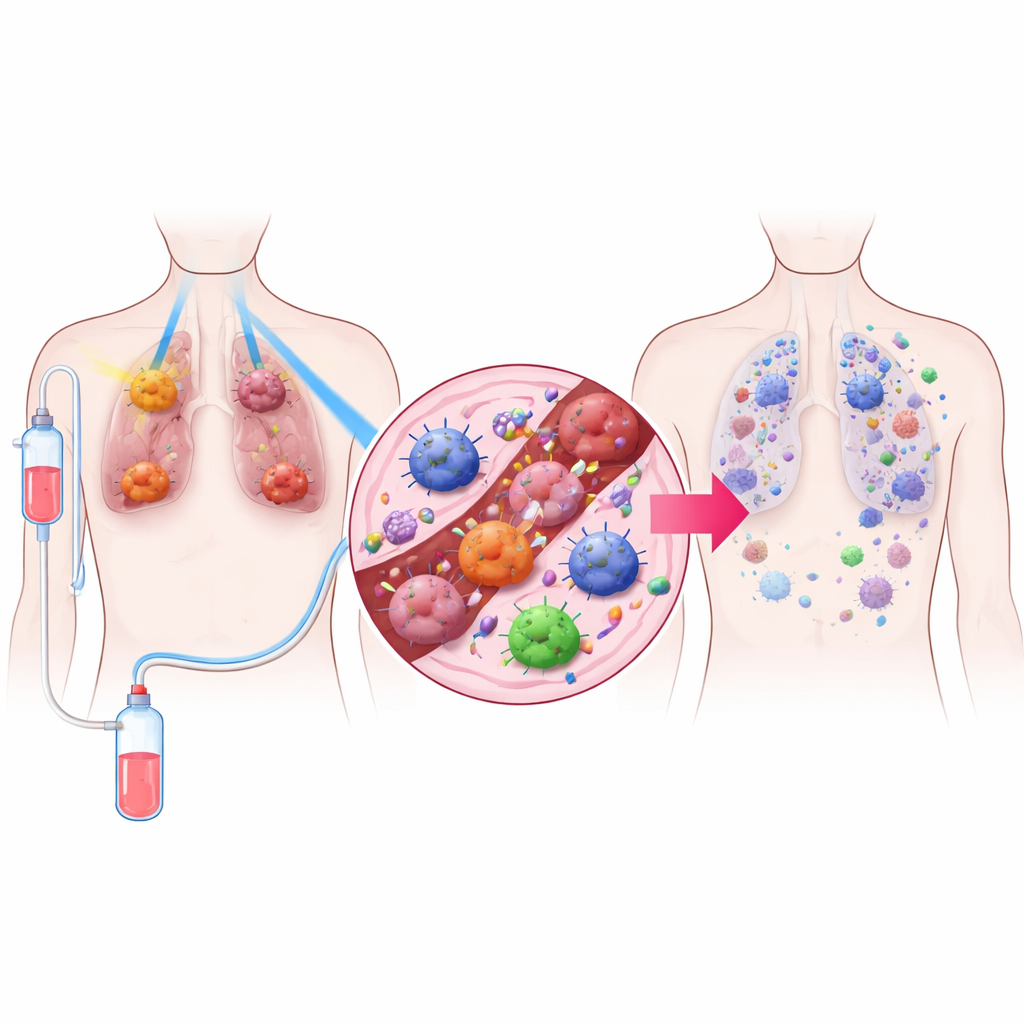
En trestegsbehandling
Forskarna utformade en behandling de kallar TRIDENT, som kombinerar tre komponenter. För det första får stora lungtumörer mycket låga doser strålning som är för svaga för att direkt döda många celler men som kan förändra tumörmiljön. För det andra bestrålas mindre tumörer med den mer bekanta högdosstrålningen som används för att lokalt förstöra cancer. För det tredje får patienterna en PD‑1‑blockerare, en sorts immunterapi som tar bort bromsen från immunsystemets T‑celler. Genom att kombinera dessa tre delar syftade teamet till både att kontrollera synliga tumörer och att väcka kroppens immunsvar över hela kroppen.
Löften om förbättrad överlevnad vid avancerad lungcancer
I en fas I‑klinisk prövning fick 29 personer med avancerad icke-småcellig lungcancer, som inte tidigare fått behandling och vars tumörer uttryckte PD‑L1‑proteinet, TRIDENT utan kemoterapi. Med mer än fem års uppföljning var medianöverlevnaden 51,3 månader — avsevärt längre än de ungefär 15–23 månader som vanligtvis ses vid standardimmunterapi ensam eller immunterapi plus kemoterapi. En separat real‑world‑grupp med 97 patienter behandlade med en TRIDENT‑liknande strategi visade liknande lovande överlevnad. Flera patienter var fria från sjukdomsprogress i mer än fem år, vilket tyder på att behandlingen kan framkalla långvarigt immunologiskt minne mot cancern.
Hur lågdosstrålning hjälper immunsystemet
För att förstå varför denna kombination fungerar använde teamet musemodeller med tumörer på båda sidor av kroppen, för att efterlikna spridning till flera platser. Endast när lågdosstrålning, högdosstrålning och PD‑1‑blockad användes tillsammans krympte tumörerna inte bara där högdoser riktades, utan även på avlägsna platser, vilket indikerar ett helkroppsligt immunsvar. Detaljerade single‑cell‑analyser visade att denna regim kraftigt ökade antalet neutrofiler som invaderade dessa avlägsna tumörer. Till skillnad från de vanliga tumörstöttande neutrofilerna producerade dessa celler det inflammatoriska signalämnet TNF‑α och uppvisade egenskaper hos professionella immunstimulerare, inklusive molekyler som gör att de kan visa upp tumörfragment för T‑celler och ge ”gå‑signal” för att attackera.
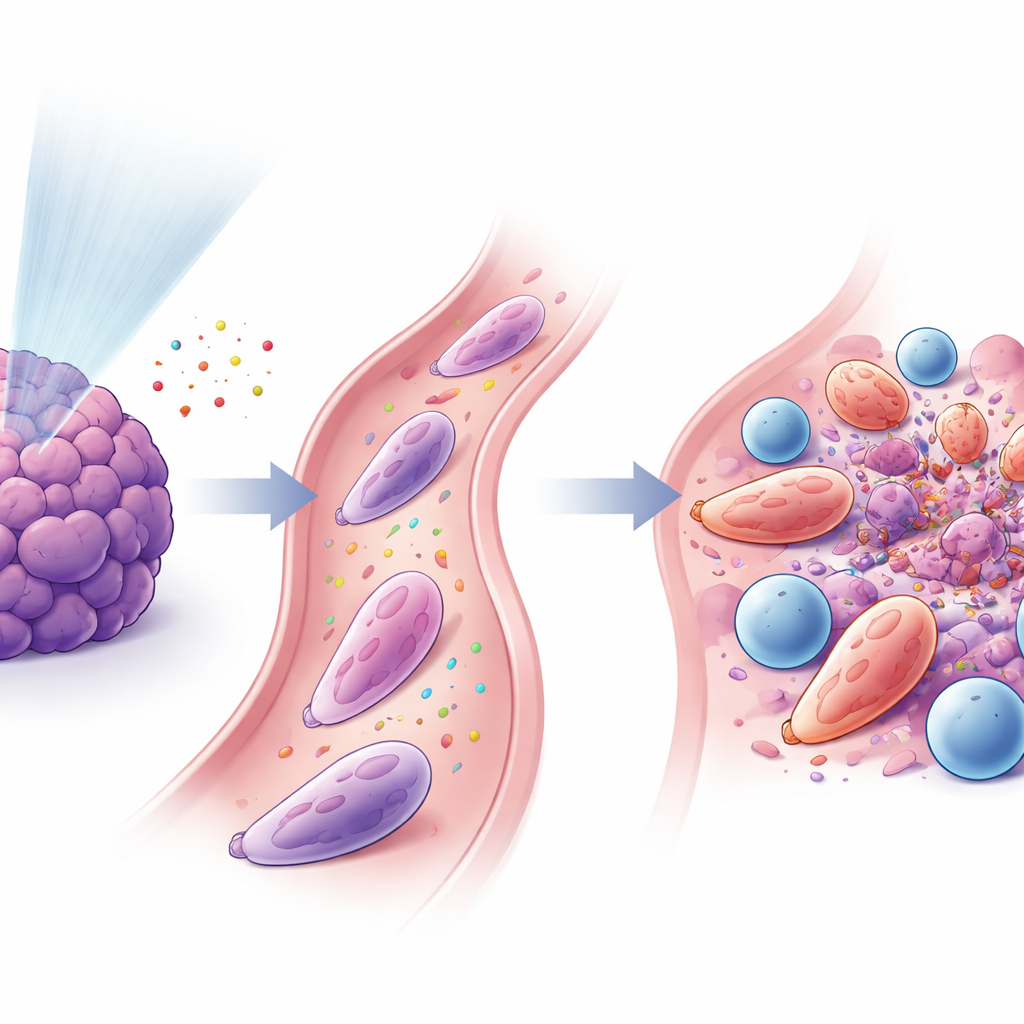
Neutrofiler och T‑celler går ihop
Studien fann att dessa omprogrammerade neutrofiler och mördande CD8+ T‑celler var tätt sammankopplade. Signaler som frigjordes efter lågdosstrålning lockade neutrofiler via en bana känd som CXCL–CXCR2, och andra faktorer, inklusive GM‑CSF och interferon‑γ, hjälpte till att omvandla dem till ett antitumört tillstånd. När de aktiverats uttryckte neutrofiler klibbiga ytmolekyler (såsom ICAM‑1) som förankrade dem tillsammans med T‑celler (som bär den matchande partnern LFA‑1), och bildade nära kontakt‑liknande ”immunsynaps”-gränssnitt. I cellkulturer stärkte dessa neutrofiler T‑cellsaktivering och proliferationen och hjälpte T‑celler att döda cancerceller mer effektivt. När forskare överförde dessa specialiserade neutrofiler till tumörbärande möss, särskilt tillsammans med PD‑1‑blockad, krympte tumörerna och överlevnaden förbättrades.
Bevis från patienttumörer och blod
Teamet undersökte också tumörprover från patienter före och efter TRIDENT med avancerade verktyg för spatial genkartering. Efter behandling visade tumörerna områden där dessa TNF‑α‑rika neutrofiler och aktiva CD8+ T‑celler klustrade ihop sig, tillsammans med starka signaler relaterade till antigenbearbetning och immu‑aktivering. I flera patientdatamängder av lungcancer behandlad med immunterapi var högre nivåer av en genprofil kopplad till dessa neutrofiler förknippad med längre tid innan sjukdomen försämrades. I en liten observationsgrupp av patienter som fick kombinerad strålning och PD‑1‑blockad visade respondenter tydliga ökningar av aktiverade neutrofiler i sitt blod, medan icke‑respondenter inte gjorde det.
Vad detta betyder för personer med lungcancer
För en person med avancerad lungcancer tyder dessa fynd på att hur strålningen ges kan vara lika viktigt som hur mycket som ges. Genom att kombinera små, immun‑finjusterande doser till stora tumörer med standard högdosstrålning och PD‑1‑blockad verkar TRIDENT förvandla neutrofiler från potentiella medhjälpare åt tumören till kraftfulla partner åt T‑celler. Detta neutrofil–T‑cells‑samarbete är kopplat till långvarig tumörkontroll och bättre överlevnad, vilket gör TRIDENT till en lovande strategi som nu prövas i större randomiserade försök. Arbetet pekar också ut aktiverade neutrofiler som möjliga framtida behandlingsmål och som enkla blodbaserade markörer för att förutsäga vilka som sannolikt gynnas av radio‑immunterapi.
Citering: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
Nyckelord: lungcancer, strålbehandling, immunterapi, neutrofiler, PD-1‑blockad