Clear Sky Science · de
Niedrigdosierte Strahlentherapie wirkt synergetisch mit PD-1-Blockade und erreicht dauerhafte Überlebensvorteile bei fortgeschrittenem NSCLC durch antitumorale Programmierung von Neutrophilen
Die Ersthelfer des Körpers gegen Lungenkrebs einsetzen
Die meisten Menschen denken an Strahlentherapie und Immuntherapie als getrennte Waffen gegen Krebs. Diese Studie zeigt, wie eine sorgfältige Abstimmung der Strahlendosen und die Kombination mit einem gängigen Immuntherapeutikum überraschenderweise eine Verbündete umprogrammieren kann — die Neutrophilen, eine Art weißer Blutkörperchen — sodass sie Patienten mit fortgeschrittenem Lungenkrebs deutlich längeres Überleben ermöglichen.
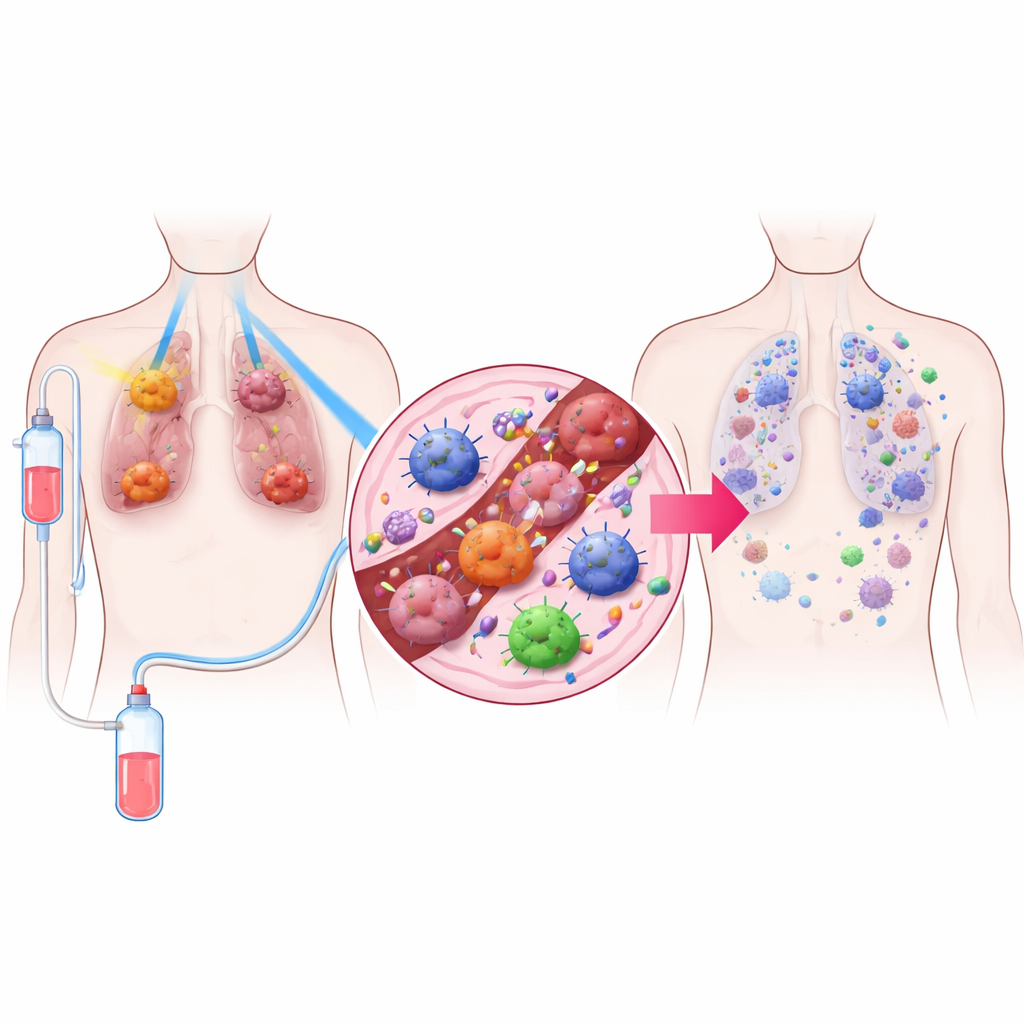
Eine dreiteilige Behandlungsstrategie
Die Forschenden entwickelten eine Behandlung namens TRIDENT, die drei Elemente kombiniert. Erstens erhalten große Lungentumoren sehr niedrige Strahlendosen, die zu schwach sind, um viele Zellen direkt abzutöten, aber das Tumormikromilieu verändern können. Zweitens werden kleinere Tumoren mit der bekannteren Hochdosisstrahlung behandelt, die lokal Krebs zerstört. Drittens erhalten die Patient*innen ein PD‑1‑blockierendes Medikament, eine Form der Immuntherapie, die den Bremsen an den T‑Zellen des Immunsystems löst. Durch die Kombination dieser drei Komponenten wollten die Forschenden sichtbare Tumoren kontrollieren und zugleich die körpereigenen Abwehrkräfte im gesamten Körper aktivieren.
Ermutigende Überlebensdaten bei fortgeschrittenem Lungenkrebs
In einer Phase‑I‑Studie erhielten 29 unbehandelte Patient*innen mit fortgeschrittenem nicht‑kleinzelligem Lungenkrebs und PD‑L1‑positiven Tumoren TRIDENT ohne Chemotherapie. Mit mehr als fünf Jahren Nachbeobachtung lag das mediane Gesamtüberleben bei 51,3 Monaten — deutlich länger als die etwa 15–23 Monate, die üblicherweise mit alleiniger Immuntherapie oder Immuntherapie plus Chemotherapie erzielt werden. Eine separate Real‑World‑Kohorte von 97 Patient*innen, die mit einem TRIDENT‑ähnlichen Ansatz behandelt wurden, zeigte ähnlich ermutigende Überlebensraten. Mehrere Patient*innen blieben länger als fünf Jahre progressionsfrei, was darauf hindeutet, dass die Behandlung eine langlebige immunologische Gedächtnisreaktion gegen den Tumor auslösen kann.
Wie niedrigdosierte Strahlung dem Immunsystem hilft
Um zu verstehen, warum diese Kombination wirkt, nutzte das Team Mausmodelle mit Tumoren auf beiden Körperseiten, die einer Ausbreitung an mehreren Stellen ähnelten. Nur wenn niedrigdosierte Strahlung, hochdosierte Strahlung und PD‑1‑Blockade zusammen eingesetzt wurden, schrumpften Tumoren nicht nur an den Stellen mit Hochdosisbestrahlung, sondern auch an entfernten Stellen — ein Hinweis auf eine systemische Immunantwort. Detaillierte Einzelzellanalysen zeigten, dass dieses Regime die Zahl der Neutrophilen, die in diese entfernten Tumoren eindrangen, stark erhöhte. Im Gegensatz zu den sonst tumorunterstützenden Neutrophilen produzierten diese Zellen das entzündliche Signal TNF‑α und zeigten Merkmale professioneller Immunstimulatoren, einschließlich Molekülen, die es ihnen ermöglichen, Tumorfragmente T‑Zellen zu präsentieren und „Angriffs“-Signale zu geben.
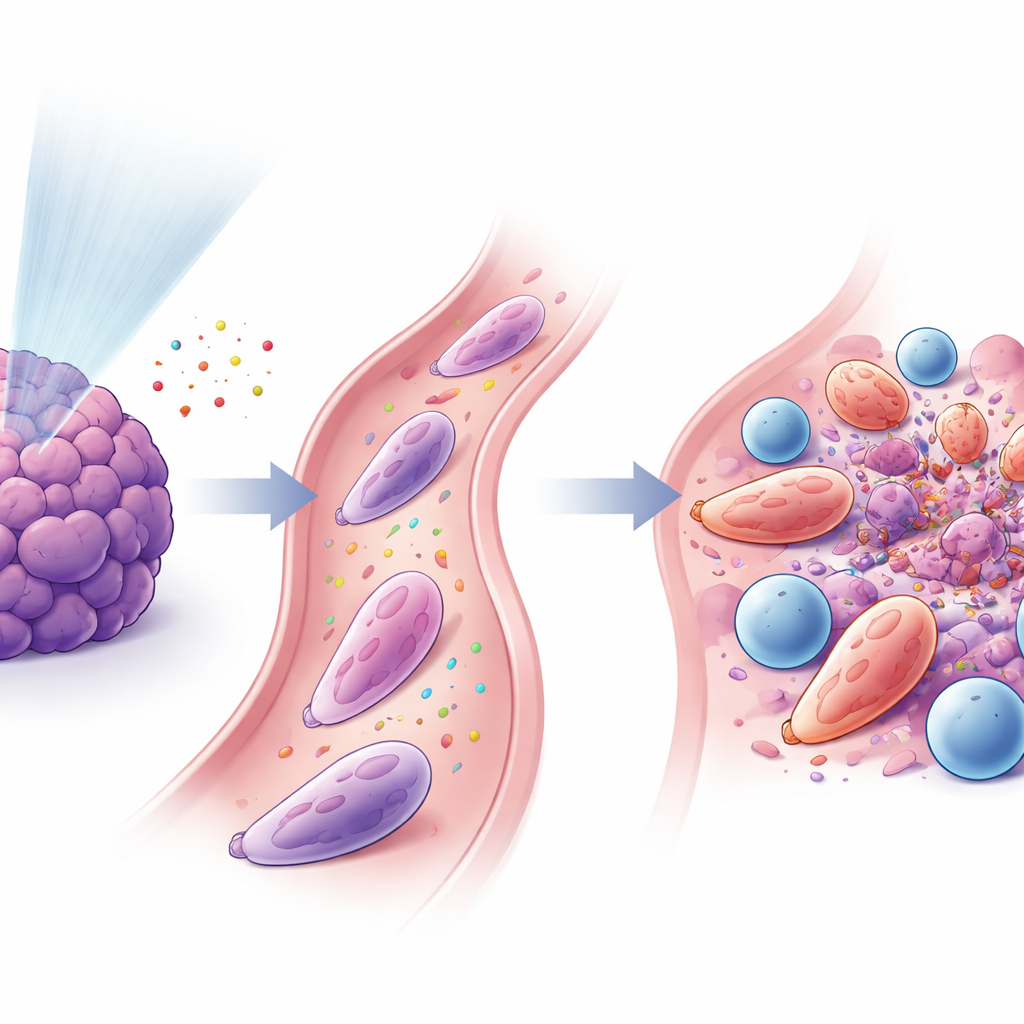
Neutrophile und T‑Zellen arbeiten zusammen
Die Studie fand, dass diese umprogrammierten Neutrophilen und die zytotoxischen CD8+‑T‑Zellen eng miteinander verknüpft waren. Nach niedrigdosierter Strahlung freigesetzte Signale lockten Neutrophile über einen Weg, der als CXCL–CXCR2 bekannt ist, an, und andere Faktoren, einschließlich GM‑CSF und Interferon‑γ, halfen, sie in einen antitumoralen Zustand zu überführen. Nach Aktivierung exprimierten Neutrophile haftende Oberflächenproteine (wie ICAM‑1), die sie mit den T‑Zellen (die das passende Gegenstück LFA‑1 tragen) verbanden und enge „immun‑synapsenähnliche“ Kontaktstellen bildeten. In Zellkultur förderten diese Neutrophilen die Aktivierung und Proliferation von T‑Zellen und unterstützten die T‑Zell‑vermittelte Vernichtung von Krebszellen effizienter. Beim Transfer dieser spezialisierten Neutrophilen in tumorbefallene Mäuse schrumpften die Tumoren und das Überleben verbesserte sich, besonders in Kombination mit PD‑1‑Blockade.
Hinweise aus Tumoren und Blut von Patient*innen
Das Team untersuchte zudem Tumorproben von Patient*innen vor und nach TRIDENT mithilfe fortschrittlicher räumlicher Genkartierungswerkzeuge. Nach der Behandlung zeigten Tumoren Bereiche, in denen TNF‑α‑reiche Neutrophile und aktive CD8+‑T‑Zellen zusammenkamen, begleitet von starken Signalen zur Antigenverarbeitung und Immunaktivierung. In mehreren Patient*innendatensätzen zu Lungenkrebs, die mit Immuntherapie behandelt wurden, war ein höheres Vorkommen einer Gen‑Signatur, die mit diesen Neutrophilen verknüpft ist, mit einer längeren Zeit bis zur Krankheitsverschlechterung assoziiert. In einer kleinen Beobachtungsgruppe von Patient*innen, die kombinierte Strahlentherapie und PD‑1‑Blockade erhielten, zeigten Ansprechende deutliche Zunahmen aktivierter Neutrophiler im Blut, während Nicht‑Ansprechende dies nicht taten.
Was das für Menschen mit Lungenkrebs bedeutet
Für Menschen mit fortgeschrittenem Lungenkrebs deuten diese Ergebnisse darauf hin, dass die Art und Weise, wie Strahlung verabreicht wird, genauso wichtig sein kann wie die Dosis selbst. Durch die Kombination kleiner, immun‑modulierender Dosen an großen Tumoren mit standardmäßiger Hochdosisbestrahlung und PD‑1‑Blockade scheint TRIDENT Neutrophile von potenziellen Komplizen des Tumors in kraftvolle Partner der T‑Zellen zu verwandeln. Diese Neutrophil‑T‑Zell‑Zusammenarbeit steht im Zusammenhang mit langanhaltender Tumorkontrolle und verbessertem Überleben und macht TRIDENT zu einer vielversprechenden Strategie, die nun in größeren randomisierten Studien geprüft wird. Die Arbeit weist außerdem darauf hin, dass aktivierte Neutrophile selbst mögliche zukünftige therapeutische Ziele und einfache blutbasierte Marker sein könnten, um vorherzusagen, wer am ehesten von Radio‑Immuntherapie profitiert.
Zitation: Zhou, L., Liu, Y., Xing, Z. et al. Low-dose radiotherapy synergizes with PD-1 blockade to achieve durable survival in advanced NSCLC through antitumor neutrophil programming. Sig Transduct Target Ther 11, 170 (2026). https://doi.org/10.1038/s41392-026-02712-6
Schlüsselwörter: Lungenkrebs, Strahlentherapie, Immuntherapie, Neutrophile, PD-1-Blockade