Clear Sky Science · zh
胰腺导管腺癌:整合分子洞见以实现靶向干预
为什么这种癌症关系到我们每个人
胰腺导管腺癌是最致命的常见癌症之一,大多数患者确诊后生存不到两年。化疗和放疗等标准治疗仅取得有限进展,而在黑色素瘤和肺癌中取得突破性成果的许多免疫治疗,在这里大多未能奏效。本文综述汇集了科学家近期对胰腺肿瘤及其周围环境生物学的新认识,并探讨这些知识如何最终为更有效、个体化的治疗打开大门。
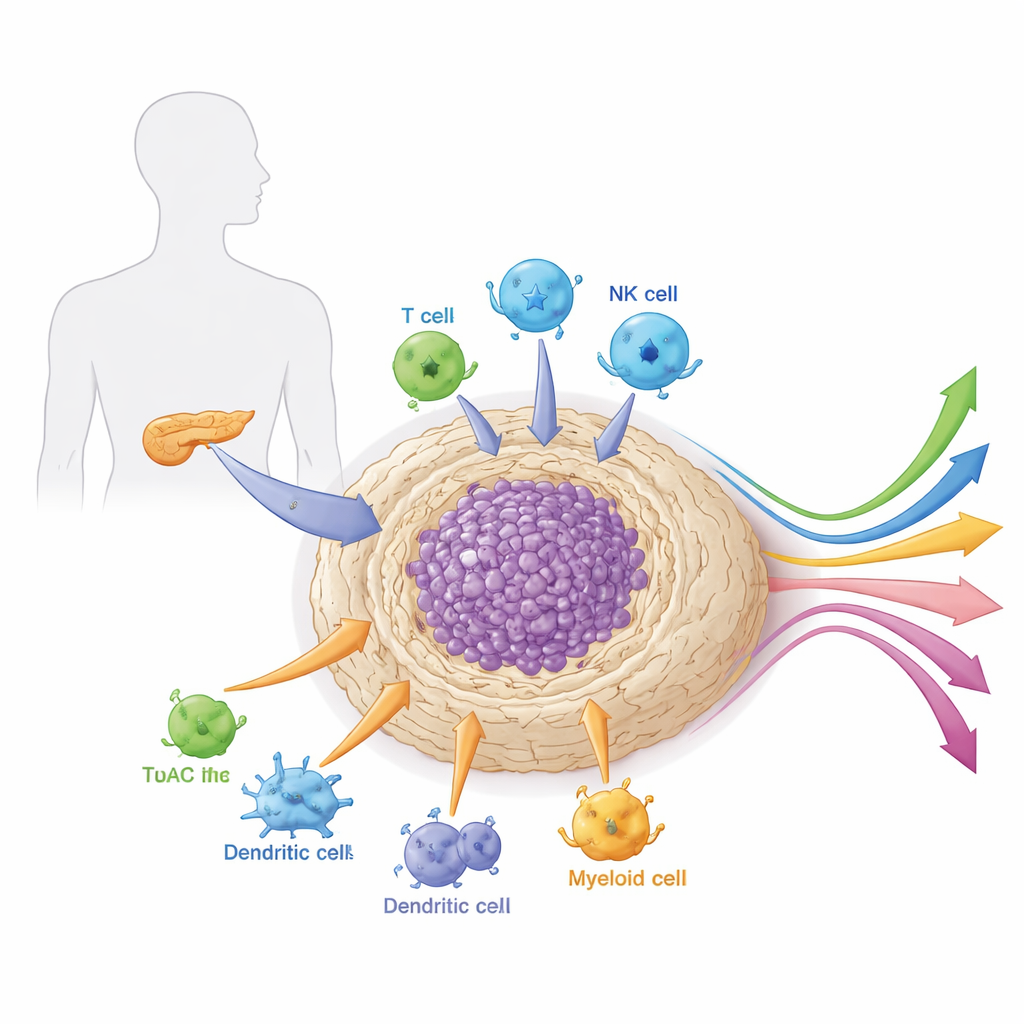
肿瘤周围的“社区”
胰腺肿瘤并非孤立生长。它们嵌入在一种致密、类似瘢痕的组织中,称为基质,内含支持细胞、免疫细胞、血管和结缔物质。这个局部“社区”或微环境异常坚固且免疫抑制性强。它既像盔甲又像生命支持系统,为癌细胞物理屏蔽药物和免疫细胞,同时提供生长信号和营养。文章解释了微环境中不同细胞类型——尤其是癌症相关成纤维细胞、髓系细胞和特化淋巴细胞——如何协同工作,保护肿瘤免受攻击并影响其对治疗的响应。
支持细胞的多重面貌
综述的核心聚焦于一类多样的细胞——癌症相关成纤维细胞。曾被认为是单一类型的结构性“辅助”细胞,这类成纤维细胞现在被识别为具有不同功能的多个亚群。有些快速增殖,构筑使肿瘤变硬并阻挡药物渗透的纤维外壳;另一些通过收缩并沉积胶原,进一步收紧这一屏障。炎性成纤维细胞分泌大量信号蛋白,吸引并重编程免疫细胞,常常使其趋向耐受而非攻击。还有些成纤维细胞改变自身代谢以供养肿瘤,甚至将肿瘤蛋白片段呈递给T细胞,有时支持免疫反应,有时促成免疫抑制。这种丰富的混合意味着粗暴地清除所有成纤维细胞可能适得其反;未来的治疗需选择性地解除有害亚型的功能,同时保留或增强保护性亚型。
被“无意中”变成盟友的免疫细胞
胰腺肿瘤内的免疫系统同样复杂。髓系来源的抑制细胞和肿瘤相关巨噬细胞受成纤维细胞和癌细胞释放的信号吸引进入肿瘤。到位后,它们剥夺杀手T细胞所需的营养物质,释放抑制免疫活性的因子,并帮助构建为癌细胞提供养分的新血管。关键的淋巴细胞群体也被重塑。调节性T细胞在细胞毒性T细胞附近聚集,通过检查点分子和代谢手段抑制其功能。树突状细胞——本应激活抗肿瘤免疫的细胞——被僵硬的基质阻隔并因脂肪酸累积而被重编程,因此对肿瘤物质的呈递能力受损。自然杀伤细胞本来擅长识别受压迫的细胞,却被肿瘤和基质信号沉默。总体而言,这些变化将原本可能具有敌意的免疫浸润转变为耐受性状态,解释了为何单独使用常规检查点抑制剂在胰腺癌中很少有效。
基因、信号通路与疗法失败的原因
在基因和分子层面,胰腺肿瘤由一组典型的改变驱动,尤其是KRAS、TP53、CDKN2A和SMAD4的突变。拷贝数改变和表观遗传变化进一步重接生长通路、细胞周期控制和DNA修复。这些改变汇入主要信号级联反应——例如MAPK和PI3K–AKT–mTOR通路——驱动增殖并在某一路径被阻断时帮助肿瘤适应。它们还影响癌细胞如何修复受损DNA,为具有特定修复缺陷的肿瘤使用PARP抑制剂等药物提供了可能。与此同时,致密的基质、异常代谢和类癌干细胞使肿瘤对化疗和靶向药物具有内在耐药性,并能快速产生获得性耐药。
新策略与未来方向
文章认为,与其依赖单一“神奇子弹”,更应采用合理的组合策略,同时针对癌细胞及其保护性环境。这些策略包括将检查点抑制剂与重塑成纤维细胞或清除抑制性髓系细胞的药物配对,改造T细胞或自然杀伤细胞以定向纤维化肿瘤,使用疫苗和基于信使RNA的方法增强对肿瘤特异性靶点的识别,以及利用DNA修复或KRAS信号通路的弱点。这类组合的早期临床试验,配合精细的遗传和免疫分型,正在开始识别哪些患者可能从哪种策略中受益。对普通读者而言,核心信息是谨慎的乐观:通过将胰腺癌理解为一个复杂的生态系统——而非仅仅是一团恶性细胞——研究者们终于在组装多管齐下的治疗方案,这些方案可能将这一历来难以对付的癌症转变为对治疗更敏感的疾病。
引用: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
关键词: 胰腺癌, 肿瘤微环境, 免疫治疗, 癌症相关成纤维细胞, KRAS 突变