Clear Sky Science · it
Adenocarcinoma duttale pancreatico: integrare conoscenze molecolari per interventi mirati
Perché questo tumore ci riguarda tutti
L’adenocarcinoma duttale pancreatico è uno dei tumori comuni più letali: la maggior parte dei pazienti vive meno di due anni dalla diagnosi. Trattamenti standard come chemioterapia e radioterapia hanno ottenuto solo miglioramenti modesti, e molte delle rivoluzioni immunoterapiche che hanno trasformato il melanoma e il cancro del polmone qui hanno in gran parte fallito. Questa rassegna mette insieme ciò che gli scienziati hanno recentemente scoperto sulla biologia dei tumori pancreatici e del loro intorno, e come queste conoscenze possano finalmente aprire la strada a terapie più efficaci e mirate.
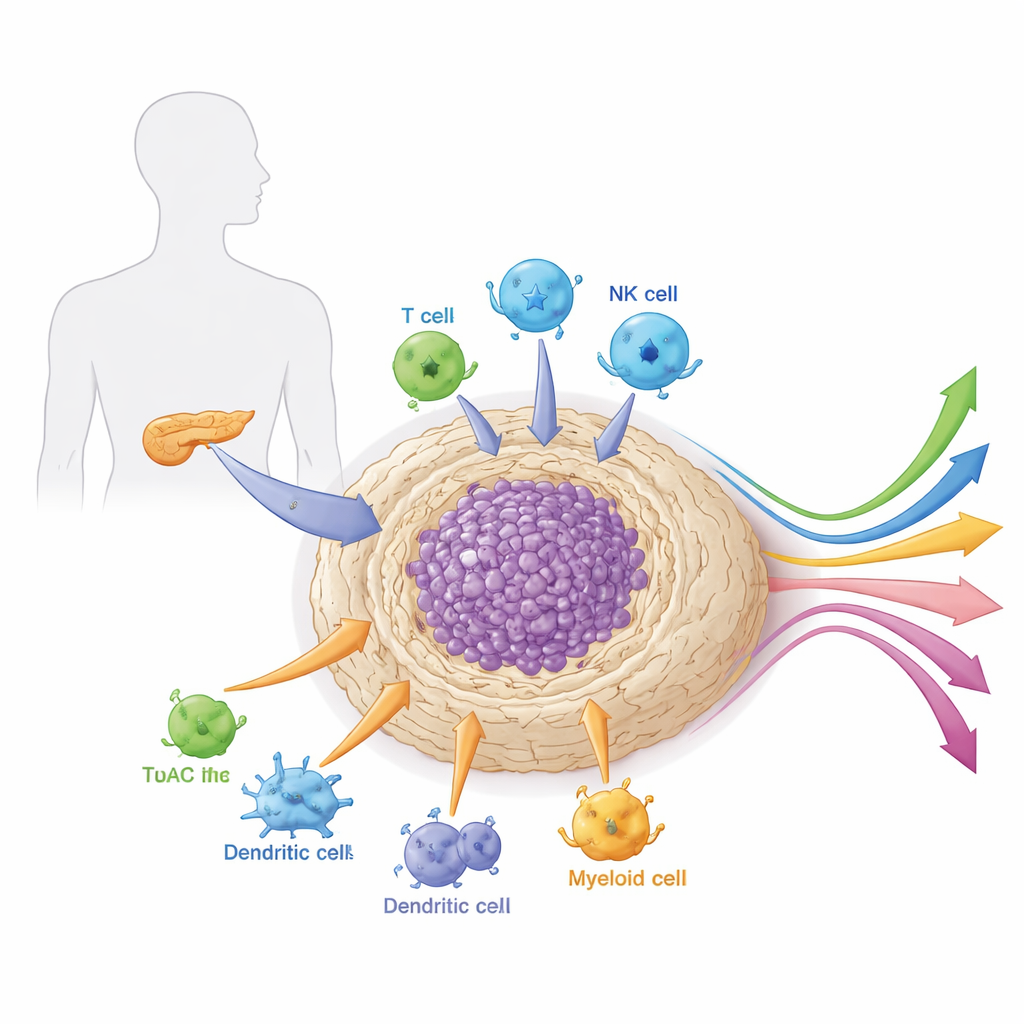
Il quartiere intorno al tumore
I tumori pancreatici non crescono isolati. Sono immersi in un tessuto denso, simile a una cicatrice, chiamato stroma, ricco di cellule di supporto, cellule immunitarie, vasi sanguigni e materiale connettivo. Questo “quartiere” locale, o microambiente, è straordinariamente compatto e immunosoppressivo. Funziona sia da armatura sia da sistema di sostegno per il cancro, ostacolando fisicamente farmaci e cellule immunitarie e al tempo stesso fornendo segnali di crescita e nutrienti. L’articolo spiega come i diversi tipi cellulari di questo microambiente — in particolare i fibroblasti associati al cancro, le cellule mieloidi e linfociti specializzati — collaborino per proteggere il tumore dall’attacco e influenzare la sua risposta alle terapie.
Le molte facce delle cellule di supporto
Un punto centrale della rassegna è una famiglia eterogenea di cellule chiamate fibroblasti associati al cancro. Un tempo considerati un unico tipo di cellule «di aiuto» strutturali, oggi si riconoscono più sottogruppi con ruoli distinti. Alcuni proliferano rapidamente e costruiscono il guscio fibroso che irrigidisce il tumore e ostacola la penetrazione dei farmaci. Altri si contraggono e depositano collagene, stringendo ulteriormente questa barriera. I fibroblasti infiammatori secernono nuvole di proteine segnale che attraggono e riprogrammano le cellule immunitarie, spesso spingendole verso la tolleranza anziché l’attacco. Altri fibroblasti alterano il proprio metabolismo per nutrire il tumore o persino presentano frammenti di proteine tumorali alle cellule T, talvolta sostenendo l’immunità e talvolta promuovendo l’immunosoppressione. Questa ricca mescolanza significa che eliminare in modo indiscriminato tutti i fibroblasti può essere controproducente; le future terapie dovranno disarmare selettivamente i sottotipi dannosi preservando o persino potenziando quelli protettivi.
Cellule immunitarie trasformate in alleati involontari
Il sistema immunitario all’interno dei tumori pancreatici è altrettanto complesso. Le cellule soppressive derivate da mieloidi e i macrofagi associati al tumore sono richiamati nel tumore da segnali prodotti da fibroblasti e cellule cancerose. Una volta lì, privano le cellule T citotossiche dei nutrienti di cui hanno bisogno, rilasciano fattori che attenuano l’attività immunitaria e contribuiscono a costruire nuovi vasi sanguigni che nutrono il cancro. Anche le popolazioni linfocitarie chiave vengono rimodellate. Le cellule T regolatorie si raggruppano vicino alle cellule T citotossiche e ne smorzano la funzione tramite molecole di checkpoint e astuzie metaboliche. Le cellule dendritiche, che dovrebbero innescare l’immunità antitumorale, vengono ostacolate dallo stroma rigido e riprogrammate dall’accumulo di acidi grassi, presentando quindi male il materiale tumorale. Le cellule natural killer, normalmente abili a riconoscere cellule stressate, vengono silenziate dai segnali tumorali e stromali. Insieme, questi cambiamenti trasformano un’infiltrazione immunitaria potenzialmente ostile in una tollerante, spiegando perché i farmaci checkpoint standard raramente funzionano da soli nel cancro pancreatico.
Geni, segnali e perché le terapie falliscono
A livello genetico e molecolare, i tumori pancreatici sono guidati da un insieme caratteristico di alterazioni, in particolare mutazioni in KRAS, TP53, CDKN2A e SMAD4. Alterazioni del numero di copie ed episodi epigenetici riorientano ulteriormente le vie di crescita, il controllo del ciclo cellulare e la riparazione del DNA. Queste modifiche alimentano grandi cascate di segnalazione — come le vie MAPK e PI3K–AKT–mTOR — che guidano la proliferazione e aiutano i tumori ad adattarsi quando una via viene bloccata. Influenzano anche come le cellule cancerose riparano il DNA danneggiato, aprendo la porta a farmaci come gli inibitori di PARP in tumori con difetti specifici di riparazione. Allo stesso tempo, lo stroma denso, il metabolismo anomalo e le cellule con caratteristiche di staminali tumorali rendono i tumori intrinsecamente resistenti a chemioterapia e farmaci mirati, e rapidi nello sviluppare resistenze acquisite.
Nuove strategie e cosa verrà dopo
Piuttosto che affidarsi a un unico «proiettile magico», la rassegna sostiene combinazioni razionali che affrontino sia le cellule tumorali sia il loro ambiente protettivo. Queste includono l’abbinamento degli inibitori di checkpoint con farmaci che rimodellano i fibroblasti o depletano le cellule mieloidi soppressive, l’ingegnerizzazione di cellule T o natural killer per consentire loro di raggiungere tumori fibróticos, l’uso di vaccini e approcci a base di mRNA per potenziare il riconoscimento di bersagli specifici tumorali e lo sfruttamento delle debolezze nella riparazione del DNA o nella segnalazione KRAS. I primi trial clinici di tali combinazioni, insieme a profili genetici e immunitari sofisticati, stanno cominciando a identificare quali pazienti potrebbero beneficiare di quale strategia. Per il lettore non specialistico, il messaggio chiave è cautamente ottimista: comprendendo il cancro pancreatico come un ecosistema complesso — piuttosto che solo una massa di cellule maligne — i ricercatori stanno finalmente assemblando piani terapeutici multifrontali che potrebbero trasformare questo tumore storicamente ostico in uno più rispondente alle terapie.
Citazione: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Parole chiave: cancro del pancreas, microambiente tumorale, immunoterapia, fibroblasti associati al cancro, mutazioni KRAS