Clear Sky Science · ru
Аденокарцинома протоков поджелудочной железы: интеграция молекулярных данных для целевых вмешательств
Почему этот рак важен для всех нас
Аденокарцинома протоков поджелудочной железы — один из наиболее смертельных из распространённых видов рака: у большинства пациентов продолжительность жизни после диагноза составляет менее двух лет. Стандартные методы лечения, такие как химио- и радиотерапия, принесли лишь скромный прогресс, а многие прорывы в иммунотерапии, поменявшие подход к меланоме и раку лёгкого, здесь в целом не сработали. В этом обзоре подводятся итоги недавних достижений в понимании биологии панкреатических опухолей и их окружения, и объясняется, как эти знания могут наконец открыть путь к более эффективным, персонализированным методам лечения.
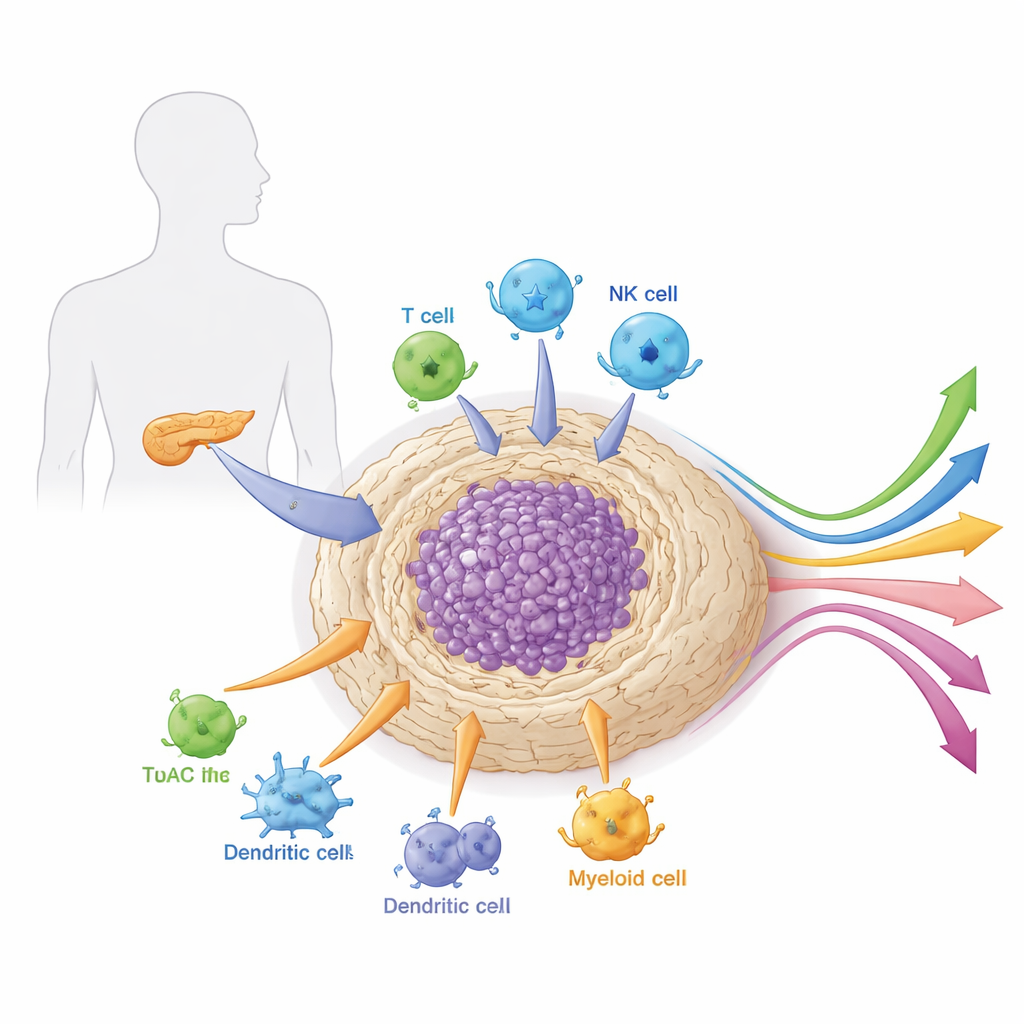
Окружение вокруг опухоли
Панкреатические опухоли не растут в одиночестве. Они находятся в плотной, похожей на рубцовую ткань строме, насыщенной вспомогательными клетками, иммунными клетками, кровеносными сосудами и соединительной матрицей. Эта локальная «околожилая» среда, или микросреда, необычно жёсткая и иммуносупрессивная. Она служит и бронёй, и системой жизнеобеспечения для рака: физически блокирует препараты и иммунные клетки, одновременно обеспечивая сигналы роста и питательные вещества. В статье рассказывается, как разные типы клеток внутри этой микросреды — особенно фибробласты, связанные с раком, миелоидные клетки и специализированные лимфоциты — взаимодействуют, чтобы защитить опухоль от атаки и формировать её реакцию на терапию.
Многообразие опорных клеток
Один из центральных акцентов обзора — разнообразная группа клеток, называемых фибробластами, связанными с раком. Ранее их рассматривали как единый тип структурных «помощников», но сейчас их признают набором подгрупп с разными функциями. Одни быстро пролиферируют и формируют волокнистую оболочку, которая уплотняет опухоль и блокирует проникновение лекарств. Другие сокращаются и откладывают коллаген, ещё больше усиливая этот барьер. Воспалительные фибробласты выделяют облака сигнальных белков, которые привлекают и перепрограммируют иммунные клетки, часто направляя их на терпимость вместо атаки. Ещё какие‑то фибробласты меняют собственный метаболизм, чтобы подпитывать опухоль, или даже представляют фрагменты опухолевых белков Т‑клеткам, что иногда поддерживает иммунитет, а иногда усиливает иммунное подавление. Такое богатое разнообразие означает, что грубое удаление всех фибробластов может дать обратный эффект; будущие подходы должны выборочно нейтрализовать вредные подтипы, сохраняя или даже усиливая защитные.
Иммунные клетки, ставшие невольными союзниками
Иммунная система внутри панкреатических опухолей столь же сложна. Миелоидно‑производные супрессорные клетки и макрофаги, ассоциированные с опухолью, притягиваются в опухоль сигналами от фибробластов и самих раковых клеток. Оказавшись там, они лишают цитотоксические Т‑клетки необходимых нутриентов, выделяют факторы, притупляющие иммунную активность, и способствуют формированию новых сосудов, питающих рак. Ключевые популяции лимфоцитов тоже перестраиваются: регуляторные Т‑клетки скапливаются рядом с цитотоксическими Т‑клетками и подавляют их через контрольные молекулы и метаболические трюки. Дендритные клетки, которые должны активировать антиопухолевый иммунитет, блокируются жёсткой стромой и перепрограммируются из‑за накопления жирных кислот, поэтому плохо представляют опухолевый материал. Естественные киллеры, обычно умеющие распознавать стрессированные клетки, заглушаются сигналами опухоли и стромы. Все эти изменения превращают потенциально враждебный иммунный инфильтрат в терпимый, что объясняет, почему одни только ингибиторы контрольных точек редко работают при раке поджелудочной железы.
Гены, сигналы и почему терапии не дают результата
На генетическом и молекулярном уровне панкреатические опухоли управляются характерным набором изменений, особенно мутациями в KRAS, TP53, CDKN2A и SMAD4. Изменения числа копий генов и эпигенетические перестройки дополнительно перенастраивают пути роста, контроль клеточного цикла и репарацию ДНК. Эти изменения вливаются в основные сигнальные каскады — такие как MAPK и PI3K–AKT–mTOR — которые стимулируют пролиферацию и помогают опухолям адаптироваться, когда блокируется один путь. Они также влияют на механизмы ремонта повреждений ДНК, открывая возможности для препаратов вроде ингибиторов PARP в опухолях с определёнными дефектами репарации. Одновременно плотная строма, аномальный метаболизм и клетки с признаками стволов делают опухоли априорно устойчивыми к химиотерапии и таргетным препаратам и способствуют быстрому формированию приобретённой резистентности.
Новые стратегии и что дальше
Вместо надежды на единую «волшебную пулю» обзор предлагает рациональные комбинации, которые атакуют и раковые клетки, и их защитное окружение. К ним относятся сочетания ингибиторов контрольных точек со средствами, перестраивающими фибробласты или истощающими супрессивные миелоидные клетки; инженерия Т‑клеток или естественных киллеров для нацеливания на фиброзные опухоли; использование вакцин и мРНК‑подходов для усиления распознавания опухолевых мишеней; а также эксплуатация уязвимостей в репарации ДНК или сигнальной активности KRAS. Ранние клинические испытания таких комбинированных подходов вместе с продвинутым генетическим и иммунным профилированием начинают выявлять, какие пациенты могут выигрывать от конкретной стратегии. Для непрофессионального читателя ключевое послание осторожно обнадёживающее: понимая рак поджелудочной железы как сложную экосистему — а не просто скопление злокачественных клеток — исследователи наконец создают многогранные планы лечения, которые могут сделать этот исторически трудноизлечимый рак более отзывчивым на терапию.
Цитирование: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Ключевые слова: рак поджелудочной железы, микросреда опухоли, иммунотерапия, фибробласты, связанные с раком, мутaции KRAS